1과목: 화공열역학
1. 21℃, 1.4atm에서 250L의 부피를 갖고 있는 이상기체가 49℃에서 300L의 부피를 가질 때의 압력은 약 몇 atm 인가?
- 0.9
- 1.3
- 1.7
- 2.1
2. 1mole의 이상기체가 1기압 0℃에서 10기압으로 압축되었다. 다음 중 어느 과정을 경유하였을 때 압축 후의 온도가 가장 높겠는가?
- 등온 압축(isothermal)
- 정용 압축(isometric)
- 단열 압축(adiabatic)
- 비가역 압축(irreversible)
3. 다음 중 공기표준 오토사이클에 대한 설명으로 옳은 것은?
- 2개의 단열과정과 2개의 정적과정으로 이루어진 불꽃 점화 기관의 이상사이클이다.
- 정압, 정적, 단열 과정으로 이루어진 압축점화 기관의 이상사이클이다.
- 2개의 단열과정과 2개의 정압과정으로 이루어진 가스터빈의 이상사이클이다.
- 2개의 정압과정과 2개의 정적과정으로 이루어진 증기원동기의 이상사이클이다.
4. 10kPa인 이상기체 1mol이 등온하에서 1kPa로 팽창될 때 엔트로피의 변화는 약 몇 J/mol·K인가?
- -4.58
- 4.58
- -19.14
- 19.14
5. 500℃에서 1000kcal의 열을 받고, 100℃에서 남은 열을 방출하는 카르노(carnot) 동력 사이클이 열효율은 약 얼마인가?
- 80.0%
- 51.7%
- 48.3%
- 20.1%
6. 반응상수의 온도에 따른 변화를 알기 위하여 필요한 물성은 무엇인가?
- 반응에 관여된 물질의 증기암
- 반응에 관여된 물질이 확산계수
- 반응에 관여된 물질의 임계상수
- 반응에 수반되는 엔탈피 변화량
7. 다음 같은 반응이 일어나는 계에 대해 처음에 CH4 2mol, H2O 1mol, CO 1mol, H2 4mol이 있었다고 한다. 평형몰분율 yi를 반응좌표 ε의 함수로 표시하려고 할 때 총 몰수(∑ni)를 ε의 함수로 옳게 나타낸 것은?
- ∑ni = 2ε
- ∑ni = 2 + ε
- ∑ni = 4 + 3ε
- ∑ni = 8 + 2ε
8. 수증기와 질소의 혼합기체가 물과 평형에 있을 때 자유도수는?
- 0
- 1
- 2
- 3
9. A함량 30mol%인 A와 B의 혼합용액이 A함량 60mol%인 A와 B의 혼합증기와 평형상태에 있을 때 순수 A증기압/순수 B증기압 비는?
- 6/4
- 3/7
- 78/28
- 7/2
10. 실험실에서 부동액으로서 30mol% 메탄올 수용액 4L를 만들려고 한다. 25℃의 물과 메탄올을 각각 몇 L씩 섞어야 하는가?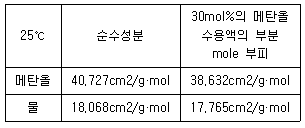
- 메탄올 = 2.000L, 물 = 2.000L
- 메탄올 = 2.034L, 물 = 2.106L
- 메탄올 = 2.064L, 물 = 1.936L
- 메탄올 = 2.100L, 물 = 1.900L
11. 다음의 관계식을 이용하여 기체의 정압 열용량과 정적 열용량 사이의 일반식을 구하면?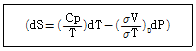
12. 성분1과 성분2가 기-액 평형을 이루는 계에 대하여 라울(Raoult)의 법칙을 만족하는 기포점 압력 계산을 수행하였다. 계산결과에 대한 설명 중 틀린 것은?
- 기포점 입력계산으로 P-x-y 선도를 나타낼 수 있다.
- 기포점 압력 계산 결과에서 기상의 조성선은 직선이다.
- 성분 1의 조성이 1일 때의 압력은 성분 1의 증기압이다.
- 공비점의 형성을 나타낼 수 없다.
13. 화학반응이 자발적으로 일어날 때 깁스(Gibbs)에너지와 엔트로피의 변화량을 옳게 표시한 것은? (단, △G계 : 계의 깁스자유에너지 변화, △Stotal : 계와 주위 전체의 엔트로피 변화)
- (△G계)T.P < 0, △Stotal > 0
- (△G계)T.P > 0, △Stotal > 0
- (△G계)T.P = 0, △Stotal = 0
- (△G계)T.P > 0, △Stotal < 0
14. 어떤 화학반응에서 평형상수의 온도에 대한 미분계수는 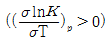 으로 표시된다. 이 반응에 대한 설명으로 옳은 것은?
으로 표시된다. 이 반응에 대한 설명으로 옳은 것은?
- 이 반응은 흡열반응이며 온도상승에 따라 K값은 커진다.
- 이 반응은 흡열반응이며 온도상승에 따라 K값은 작아진다.
- 이 반응은 발열반응이며 온도상승에 따라 K값은 커진다.
- 이 반응은 발열반응이며 온도상승에 따라 K값은 작아진다.
15. 벤젠과 툴루엔은 이상용액에 가까운 용액을 만든다. 80℃에서 벤젠의 증기압은 753mmHg, 톨루엔의 증기압은 290mmHg 이다. 벤젠과 톨루엔의 몰비율이 1 : 1인 혼합용액의 80℃에서의 증기의 전압은 약 몇 mmHg 인가?
- 700
- 500
- 300
- 100
16. 2성분계 공비 혼합물에서 성분 A, B의 활동도 계수를 γA와 γB, 증기압을 PA 및 PB라하고 이 계의 전압을 PT라 할 때 γB를 옳게 나타낸 것은? (단, B성분의 기상 및 액상에서의 몰분율은 yB와 XB이며, 퓨개시티계수 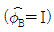 이라 가정한다.)
이라 가정한다.)
- γB= PT/PB
- γB= P1/PB(1-XA)
- γB= P1yB/PB
- γB= PT/PBXB
17. 다음 그림은 순수한 성분의 온도-압력의 관계를 나타낸 그림이다. 이 그림에서 유체의 초임계영역은 어디인가?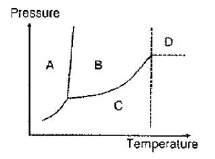
- A 영역
- B 영역
- C 영역
- D 영역
18. 다음 그림은 A, B-2 성분계 용액에 대한 1기압 하에서의 온도-농도간의 평행관계를 나타낸 것이다. A의 몰분율이 0.4인 용액을 1기압 하에서 가열할 경우, 이 용액의 끓는 온도는 몇 ℃인가? (단, XA는 액상 몰분률이고, yA는 기상 몰분률이다.)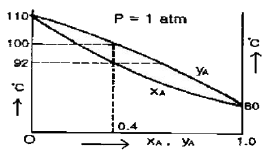
- 80℃
- 80℃부터 92℃까지
- 92℃부터 100℃까지
- 110℃
19. 다음 그림은 A, B 2성분 용액의 H-X 선도이다. XA=0.4 일 때의 A의 부분몰 엔탈피 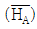 는 몇 cal/mol 인가?
는 몇 cal/mol 인가?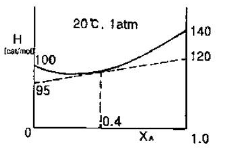
- 95
- 100
- 120
- 140
20. 기체터빈 동력장치가 압축비 PA : PB=1 : 6에서 운전되며 γ=1.4인 경우 이상기체의 사이클 효율 η는?
- 0.2
- 0.4
- 0.6
- 0.8
2과목: 단위조작 및 화학공업양론
21. 다음 중 Hess의 법칙과 가장 관련이 있는 함수는?
- 비열
- 열용량
- 엔트로피
- 반응열
22. 반데르발스(van der Waals) 상태방정식을 다음과 같이 나타내었다. P의 단위 N/m2, n의 단위 kmol, V의 단위 m3, T의 단위 K로 표시하였을 때 상수 a의 단위는?
23. 1기압 20℃의 공기가 10L의 용기에 들어있다. 공기 중 산소만 제거하여 전체 체적을 질소만 차지한다면 압력은 약 몇 mmHg 가 되는가? (단, 공기는 질소 79%, 산소 21%로 되어 있다.)
- 160
- 510
- 600
- 760
24. 450K, 500kPa 에서의 공기 밀도로 옳은 값은? (단, 공기의 평균 분자량은 29이다.)
- 3.877 kg/m3
- 0.126 kg/m3
- 1.126 g/cm3
- 3877 g/cm3
25. 20wt%소금수용액의 밀도가 10℃에서 1.20g/mL 이다. 소금의 몰분율과 노르말농도는 각각 얼마인가? (단, NaCl 분자량은 58이다.)
- 0.072, 4.31N
- 0.38, 4.31N
- 0.072, 4.14N
- 0.38, 4.14N
26. 1atm, 25℃에서 상대습도가 50%인 공기 1m3 중에 포함되어 있는 수중기의 양은? (단, 25℃에서의 수증기압은 24mmHg이다.)
- 11.6g
- 12.5g
- 28.8g
- 51.5g
27. 같은 온도에서 같은 부피를 가진 수소와 산소의 무게의 측정값이 같았다. 수소의 압력이 4atm 이라면 산소의 압력은 몇 atm 인가?
- 4
- 1
- 1/4
- 1/8
28. 에탄과 메탄으로 혼합된 연료가스가 산소와 질소 각각 50mol%씩 포함된 공기로 연소된다. 연소 후 연소가스 조성은 CO2 25mol%, N2 60mol%, O2 15mol% 이었다. 이때 연료가스 중 메탄의 mol%는 얼마인가?
- 25.0
- 33.3
- 50.0
- 66.4
29. 양대수좌표(log-log graph)에서 직선이 되는 식은?
- Y = bxa
- Y = bexa
- Y = bx + a
- logY = logb + ax
30. 82℃에서 벤젠의 증기압은 811mmHg이고 톨루엔의 증기압은 314mmHg이다. 벤젠과 톨루엔의 혼합용액은 이상용액이라면 벤젠 20mol%와 톨루엔 80mol%를 포함하는 용액을 증발시켰을 때 증기 중의 벤젠의 몰분율은?
- 0.362
- 0.372
- 0.382
- 0.392
31. 노벽과 두께가 200mm이고, 그 외측은 75mm의 석면판으로 보온되어 있다. 노벽의 내부온도가 400℃이고, 외측온도가 38℃일 경우 노벽의 면적이 10m2라면 열손실은 약 몇 kcal/h인가? (단, 노벽과 석면판의 평균 열전도도는 각각 3.3, 0.13kcal/m·h·℃이다.)
- 3070
- 5678
- 15300
- 30600
32. 자유표면이 있는 액체가 경사면을 흘러가고 있다. 속도구배가 완전히 발달한 층류로 층의 두께가 일정하다고 할 떄의 층의 두께는 1mm이다. 액체부하를 포함하여 다른 조건이 동일하고 유체의 밀도만 2배가 될 때의 층의 두께는 약 얼마인가?
- 0.53mm
- 0.63mm
- 1.59mm
- 2.59mm
33. 다음 중 일반적으로 가장 작은 크기로 입자를 축소시킬 수 있는 장치는?
- 칼날 절단기(knife cutter)
- 죠파쇄기(jaw crusher)
- 선회파쇄기(gyratory crusher)
- 유체-에너지 밀(fluid-energy mill)
34. 40℃의 물의 점도는 0.00654g/cm·s이고 열전도도는 0.539kcal/m·h·℃이다. 이 때 물의 Prandtl number 는?
- 2.34
- 4.37
- 5.14
- 9.58
35. A와 B의 혼합용액에서 r를 활동도 계수라 할 때 최고 공비 혼합물이 가지는 r값의 범위를 옳게 나타낸 것은?
- rA=1, rB=1
- rA<1, rB>1
- rA<1, rB<1
- rA>1, rB>1
36. 다음 효용 증발조직의 목적으로 다음 중 가장 중요한 것은?
- 열을 경제적으로 이용하기 위한 것이다.
- 제품의 순도를 높이기 위한 것이다.
- 작업을 용이하게 하기 위한 것이다.
- 장치비를 절약하기 위한 것이다.
37. 그림과 같은 3성분계에서의 평형곡선에 대한 설명으로 옳은 것은?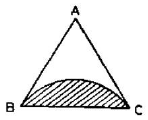
- A와 B는 잘 섞이지 않는다.
- B와 C는 잘 섞이지 않는다.
- C와 A는 잘 섞이지 않는다.
- 빗금친 부분에서 A, B, C 는 완전혼합이다.
38. 진공 증발을 사용하는 이유로 가장 거리가 먼 것은?
- 증발기의 크기를 증가시킨다.
- 비점을 내려가게 한다.
- 증기를 경제적으로 이용할 수 있게 한다.
- 열민감 제품의 변질을 방지한다.
39. 기포탑(bubble tower)과 비교한 충전탑의 특성과 거리가 먼 것은?
- 구조가 간단하다.
- 편류가 형성되는 단점이 있다.
- 부식 및 압력에 의한 문제점이 크다.
- 충전물에 오염물이 부착될 수 있는 단점이 있다.
40. 건조조작에서 임계함수율(critical moisture content)을 옳게 설명한 것은?
- 건조 속도가 0 일 때의 함수율이다.
- 감률 건조기간이 끝날 때의 함수율이다.
- 함률 건조기간에서 감률 건조기간으로 바뀔 때의 함수율이다.
- 건조조작이 끝날 때의 함수율이다.
3과목: 공정제어
41. 전달함수 G(s)=e-2s에 대한 주파수 응답에 있어 위상지연각(phase lag)은? (단, radian frequency(w)=1[rad/time] 이다.)
- 28.7°
- 57.3°
- 114.6°
- 287.0°
42. 전달함수가 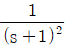 인 2차계이 단위충격응답(unitimpuise response)에서 1분 후의 값은 2분 후의 값의 몇 배인가?
인 2차계이 단위충격응답(unitimpuise response)에서 1분 후의 값은 2분 후의 값의 몇 배인가?
- e
- e/2
- e2/2
- 2e2
43. 그림 (a)와 (b)가 등가이기 위한 블록선도 (b)에서의 m의 값은?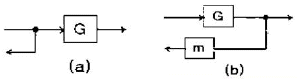
- G
- 1/G
- G2
- 1-G
44. 다음 중 제어계의 안전성을 판별하는 방법과 가장 관련이 없는 것은?
- Bode 선도
- Routh array
- Nyquist 선도
- Analog 회로
45. Routh array에 의한 안전성 판별법 중 옳지 않은 것은?
- 특성방정식의 계수가 다른 부호를 가지면 불안정하다.
- Routh array의 첫 번째 컬럼의 부호가 바뀌면 불안정하다.
- Routh array test를 통해 불안정한 Pole의 개수도 알 수 있다.
- Routh array의 첫 번째 컬럼에 0이 존재하면 불안정하다.
46. PID 제어기에 관한 설명 중 옳지 않은 것은?
- Reset windup 현상은 I-모드를 사용할 때 발생하며 자동 모드로 Startup 할 때 많이 발생한다.
- 제어출력이 증가할 때 공정출력이 감소하는 공정일 경우, 비례이득의 부호는 양이 되어야 한다.
- Bumpless transfer란 수동에서 자동으로 또 자동에서 수동으로 변환될 때 제어기 출력의 bias value를 현재 MV값으로 바꾸어 주는 동작을 말한다.
- Derivative kick은 오차에 대한 미분(de/dt)을 측정변수의 이분(-dy/dt)으로 대체하면 제거할 수 있다.
47. 다음 중 폐회로 응답에서 PD제어보다는 overshoot이 크지만 다른 양식보다는 작고, 잔류편차가 완전히 제거되는 제어양식은?
- P 방식제어
- PI 방식제어
- PID 방식제어
- I 방식제어
48. 다음 중 Ziegler-Nichols 제어기 조율법에 관한 설명으로 가장 옳은 것은?
- 폐회로의 계단응답이 대략 1/4 DR(decay ratio)를 갖도록 설계된 조율법으로, 화학공정제어에서 지나치게 큰 진동을 주는 경우가 있다.
- 공정의 정상상태 이득을 아는 것은 제어기 조율의 정확성을 증진시킨다.
- 공정 G(s)에 사용할 PI 제어기
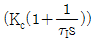 를 조율하는 경우
를 조율하는 경우 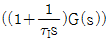 의 임계이득(ultimate gain)과 임계주파수(ultimate frequency)를 구하여 활용한다.
의 임계이득(ultimate gain)과 임계주파수(ultimate frequency)를 구하여 활용한다. - 같은 차수의 공정은 동일한 Z-N 조율 값을 보인다.
49. 그림과 같이 표시되는 함수의 Laplace 변환은?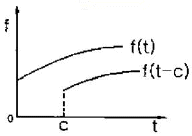
- e-csL[f]
- ecsL[f]
- L[f(s-c)]
- L[f(s+c)]
50. 시간상수 τ가 3초이고 이득 Kp가 1이며 1차공정의 특성을 지닌 온도계가 초기에 20℃를 유지하고 있다. 이 온도계를 100℃의 물속에 넣었을 때 3초 후의 온도계 읽음은?
- 68.4℃
- 70.6℃
- 72.3℃
- 81.9℃
51. 안정한 1차계의 계단응답에서 시간이 시정수(time constant)의 3배가 되면 응답은 최대 값의 몇 %에 도달되는가?
- 83.2%
- 89.2%
- 92.3%
- 95%
52. 전달함수가 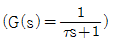 인 1차계에 크기 M인 계단변화가 도입되었을 때의 응답은? (단, 정상상태는 0으로 간주한다.)
인 1차계에 크기 M인 계단변화가 도입되었을 때의 응답은? (단, 정상상태는 0으로 간주한다.)
53. 다음 중 ATO(Air-To-Open) 제어밸브가 사용되어야 하는 경우는?
- 저장 탱크 내 위험물질의 증발을 방지하기 위해 설치된 열교환기의 냉각수 유량 제어용 제어밸브
- 저장 탱크 내 물질의 응고를 방지하기 위해 설치된 열교환기의 온수 유량 제어용 제어밸브
- 반응기에 발열을 일으키는 반응 원료의 유량 제어용 제어밸브
- 부반응 방지를 위하여 고온 공정 유체를 신속히 냉각시켜야 하는 열교환기의 냉각수 유량 제어용 제어밸브
54. 다음 전달함수를 역변환한 것은?
55. 함수 f(t)의 Laplace 변환이 다음과 같이 주어졌을 때, f(0)의 값을 구하면?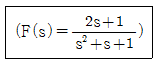
- 0.5
- 1
- 2
- 3
56. 공정이득(gain)이 2인 공정을 설정치(set point)가 1이고 비례이득(Proportional gain)이 1/2인 비례(Proportional) 제어기로 제어한다. 이 때 오프셋은 얼마인가?
- 0
- 1/2
- 3/4
- 1
57. 다음 중 Gain margin(이득마진)과 관계되는 수식은? (w는 frequency이며 w∞는 Phase lag가 -180° 일 때의 w이다. GOL은 안정도 판정에 사용되는 개루프 전달함수이고, G는 공정전달함수이다.)
58. 이상적인 PID 제어기 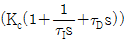 이 실용적인 PID 제어기가 되기 위해서는 여러 변형이 가해진다. 이중 옳지 않은 것은?
이 실용적인 PID 제어기가 되기 위해서는 여러 변형이 가해진다. 이중 옳지 않은 것은?
- 설정치의 일부만을 비례동작에 반영 : KcE(s)=Kc(R(s)-Y(s))→Kc(αR(s)-Y(s)), 0≤α≤1
- 설정치의 일부만을 적분동작에 반영 :
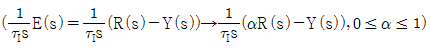
- 설정치를 미분하지 않음 : τDsE(s)=τDs(R(s)-Y(s))→-τDsY(s)
- 미분동작의 잡음에 대한 민감성을 완화시키기 위한 filltered 미분동작 :

59. 전형적인 제어루프에 관한 설명 중 틀린 것은?
- 가스크로마토그래피로 측정되는 농도제어 루프의 경우 긴 시간지연을 보이게 된다.
- 동적응답이 느린 온도제어루프는 미분동작을 추가하여 성능향상을 얻을 수 있다.
- 적분공정 형태이 액위 제어루프에는 비례동작보다는 적분동작을 위주로 설계 되어야 한다.
- 매우 빠른 동특성과 측정 노이즈가 심한 유량제어 루프에는 비례-적분 제어기가 추천된다.
60. 전달함수에 관한 설명으로 틀린 것은?
- 보통 공정(Usual Process)의 경우 분모의 차수가 분자의 차수보다 크다.
- 공정출력의 Laplace 변환을 공정입력의 Laplace 변환으로 나눈 것이다.
- 공정입력과 공정출력사이의 동특성(Dynamics)을 Laplace 영역에서 표시한 것이다.
- 비선형공정과 선형공정 모두 전달함수로 완벽하게 표현될 수 있다.
4과목: 공업화학
61. 인광석을 산분해하여 인산을 제조하는 방식 중 습식법에 해당하지 않는 것은?
- 황산 분해법
- 염산 분해법
- 질산 분해법
- 아세트산 분해법
62. 다음 중 아세틸렌에 작용시키면 아세틸렌법으로 염화비닐이 생성되는 것은?
- HCl
- NaCl
- H2SO4
- HOCl
63. 소금을 전기분해하여 하루에 1ton의 염소가스를 생산하는 전해 수산화나트륨 공장이 있다. 이 공장에서 생산되는 NaOH는 하루에 약 몇 ton 인가?
- 1.13
- 2.13
- 3.13
- 4.13
64. 순도가 70%인 아염소산나트륨의 유효염소는 몇 %인가?
- 100
- 110
- 120
- 130
65. 접착속도가 매우 빨라서 순간접착제로 흔히 사용되는 성분은?
- 시아노아크릴레이트
- 아크릴에멀젼
- 벤조퀴논
- 폴리이소부틸렌
66. 염산제조에 있어서 단위 시간당 흡수되는 HCl 가스량(G)을 나타낸 식으로 옳은 것은? (단, K:HCl 가스 흡수계수, A:기상-액상의 접촉면적, △P:기상-액상과의 HCl 분압차이다.)
- G=K2A
- G=K△P
- G=K/A△P
- G=KA△P
67. 연료전지에 쓰이는 전해질이 아닌 것은?
- 인산
- 자르코늄 다이옥사이드
- 용융탄산염
- 테프론 고분자막
68. 다음 중 기하이성질체를 나타내는 고분자가 아닌 것은?
- 폴리부타디엔
- 폴리클로로프렌
- 폴리이소프렌
- 폴리비닐알콜
69. 질소비료는 주로 어떤 형태로 식물에 흡수되는가?
- NO2-
- N2
- NO3-
- NH4OH
70. 아닐린(aniline)을 출발물질로 하여 염화벤젠디아조늄을 생성하는 디아조화 반응과 관계가 없는 것은?
- 염화수소
- 에틸렌
- 아질산나트륨
- 방향족 1차 이민
71. 니트로벤젠을 환원시켜 아닐린을 얻을 때 다음 중 가장 적합한 환원제는?
- Zn+Water
- Zn+Acid
- Alkaline Sulfide
- Zn+Alkali
72. 황산을 mSO3nH2O로 표시할 때 발연황산을 나타낸 것은?
- m >n
- m = n
- m< n
- m + n = 3
73. pH가 2인 공장 폐수 내에 Cu+2, Zn+2 등의 중금속이온이 다량 함유되어 있다. 이들을 중화처리할 때 중금속이온은 수산화물 형태로 대부분 침전되어 제거되지만, 입자의 크기가 작은 경우에는 콜로이드상태로 존재하게 되므로 응집제를 사용하여야 한다. 이와 같은 폐수처리과정에서 필요한 물질들을 옳게 나열한 것은?
- NaOH, H2SO4
- H2SO4, FeCl3
- H2SO4, Al2(SO4)3·18H2O
- CaO, Al2(SO4)3·18H2O
74. 다음 중 p형 반도체를 제조하기 위해 실리콘에 소량 첨가하는 물질은?
- 비소
- 안티몬
- 인듐
- 비스무스
75. 다음 중 2차 전지에 해당하는 것은?
- 망간전지
- 산화은전지
- 납축전지
- 수은전지
76. 산화하여 아세톤이 되는 것은?
- CH3CH2CH2OH
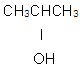
- CH3CH2CHO
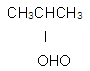
77. 암모니아 합성공정에 있어서 촉매 1m2 당 1시간에 통과하는 원료가스(0℃, 760mmHg 환산)의 m2 수를 무엇이라고 하는가?
- 순간속도
- 공시득량
- 공간속도
- 원단위
78. 접촉식 황산제조 공정에서 전화기에 대한 설명 중 옳은 것은?
- 전화기 조작에서 온도조절이 좋이 않아서 온도가 지나치게 상승하면 전화율이 감소하므로 이에 대한 조절이 중요하다.
- 전화기는 SO3 생성열을 제거시키며 동시에 미반응 가스를 냉각시킨다.
- 촉매의 온도는 200℃ 이하로 운전하는 것이 좋기 때문에 열교환기의 용량을 증대시킬 필요가 있다.
- 전화기의 열교환방식은 최근에는 거의 내부 열교환방식을 채택하고 있다.
79. 유지 성분의 공업적 분리 방법으로 다음 중 가장 거리가 먼 것은?
- 분별결정법
- 원심분리법
- 감압증류법
- 분자증류법
80. R-COOH와 SOCl2 또는 PCl5를 반응시킬 때 주성생물은?
- R-Cl
- R-CH2Cl
- R-COCl
- R-CHCl2
5과목: 반응공학
81. 자기 촉매 반응에서 목표 전환율이 반응속도가 최대가 되는 반응 전환율보다 낮을 때 사용하기에 유리한 반응기는? (단, 반응생성물의 순환이 없는 경우이다.)
- 혼합 반응기
- 플러그 반응기
- 직렬 연결한 혼합 반응기와 플러그 반응기
- 병렬 연결한 혼합 반응기와 플러그 반응기
82. 1/2차 반응을 수행하였더니 액체 반응 물질이 10분간에 75%가 분해되었다. 같은 조건하에서 이 반응을 완결하는데 시간은 몇 분이나 걸리겠는가?
- 20
- 25
- 30
- 35
83. A→R인 반응기 부피가 0.1L인 플러그 흐름 반응기에서 -rA=50CA2 mol/L·min 로 일어난다. A의 초기농도 CAO 는 0.1mol/L 이고 공급속도가 0.05L/min 일 때 전화율은 얼마인가?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
- 0.509
- 0.609
- 0.809
- 0.909
84. 촉매의 기능에 관한 설명으로 옳지 않은 것은?
- 촉매는 화학평형에 영향을 미치지 않는다.
- 촉매는 반응속도에 영향을 미친다.
- 촉매는 화학반응의 활성화에너지를 변화시킨다.
- 촉매는 화학반응의 양론식을 변화시킨다.
85. 다음과 같은 단분자형의 1차 연속 반응이 회분식 반응기에서 일어난다. 공급물에서의 생성물 R과 S의 농도가 모두 0 일 때 k1=0.05s-1, k2=0.05s-1이고, 이 때 R은 목적하는 생성물, S는 목적하지 않는 생성물이다. 반응이 30초가 경과했을 때의 초기농도에 대한 A의 농도비 CA/CAO는 얼마인가?
- 0.012
- 0.022
- 0.223
- 0.243
86. 다음 중 고체촉매반응의 반응 7단계의 순서로 올바른 것은?
- 외부확산→내부확산→흡착→표면반응→탈착→내부확산→외부확산
- 내부확산→외부확산→흡착→표면반응→탈착→내부확산→외부확산
- 내부확산→외부확산→탈착→표면반응→흡착→외부확산→내부확산
- 외부확산→흡착→내부확산→표면반응→내부확산→탈착→외부확산
87. 반감기가 20h인 어떤 방사성 유체를 200L/h의 속도로 각각 용적이 40000L인 2개의 직렬교반조를 통과하여 처리하였다. 이 반응기를 통과함으로써 방사능은 몇 % 감소되는가? (단, 방사선 붕괴를 1차반응으로 간주한다.)
- 95.8%
- 96.8%
- 97.8%
- 98.4%
88. 다음은 n차(n>0) 단일 반응에 대한 한 개의 혼합 및 플러그 흐름 반응기 성능을 비교 설명한 내용이다. 옳지 않은 것은? (단, Vm은 혼합흐름반응기 부피, Vp는 플러그흐름반응기 부피를 나타낸다.)
- Vm은 Vp 보다 크다.
- Vm/Vp는 전환율의 증가에 따라 감소한다.
- Vm/Vp는 반응차수에 따라 증가한다.
- 부피변화 분율이 증가하면 Vm/Vp가 증가한다.
89. 다음과 같은 경쟁반응에서 원하는 반응을 가장 좋게 하는 접촉방식은? (단, n>P, m<Q)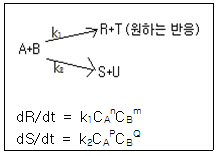
90. 반응기에 유입되는 물질량의 체류시간에 대한 설명으로 옳지 않은 것은?
- 반응물의 부피가 변하면 체류시간이 변한다.
- 반응물이 실제의 부피 유량으로 흘러 들어가면 체류시간이 달라진다.
- 액상반응이면 공간시간과 체류시간이 같다.
- 기상반응이면 공간시간과 체류시간이 같다.
91. 다음 그림은 이상적 반응기의 설계 방정식의 반응시간을 결정하는 그림이다. 회분 반응기의 반응시간 t=(면적)인데 이에 해당하는 면적을 옳게 나타낸 것은?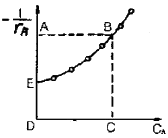
92. 다음 그림은 균일계 비가역 병렬 반응이 플러그 흐름반응기에서 진행될 때 순간수율 ø(R/A)와 반응물의 농도 (CA)간의 관계를 나타낸 것이다. 빗금친 부분의 넓이가 뜻하는 것은?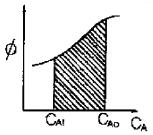
- 총괄 수율ø
- 반응하여 없어진 반응물의 몰수
- 반응으로 생긴 R의 몰수
- 반응기를 나오는 R의 농도
93. 다음 그림은 어느 반응의 농도변화를 나타낸 그림인가?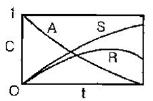
94. 기상 촉매반응의 유효인자(effectiveness factor)에 영향을 미치는 인자로 다음 중 가장 거리가 먼 것은?
- 촉매 입자의 크기
- 촉매 반응기의 크기
- 반응기 내의 전체 압력
- 반응기 내의 온도
95. 다음과 같은 A의 분해반응에서 원하는 생성물은 T이다. 등온 플러그 흐름 반응기에서 얻을 수 있는 T의 최대 농도는 얼마인가? (단, CAO=1 이다.)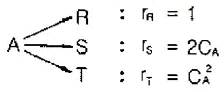
- 0.051
- 0.114
- 0.235
- 0.391
96. 어떤 반응의 속도상수가 25℃에서 3.46×10-5s-f이며 62℃에서는 4.91×10-3s-1이었다. 이때 활성화 에너지는 몇 kcal 인가?
- 44.75
- 34.75
- 24.79
- 14.75
97. 부피유량 u가 일정한 관형반응기 내에서 1차 반응 A→B 이 일어난다. 부피유량이 10L/min, 반응속도상수 k가 0.23/min일 때 유출농도를 유입농도의 10% 로 줄이는데 필요한 반응기의 부피는? (단, 반응기의 입구조건 V=0 일 떄 CA=CAO 이다.)
- 100L
- 200L
- 300L
- 400L
98. 현재의 혼합흐름 반응기를 부피가 2배인 것으로 교체하고자 한다. 같은 공급물을 동일한 공급 속도로 공급한다면 교체 후의 새로운 전화율은 얼마인가? (단, 반응속도 A→R, -rA=kCA 로 나타내며 현재의 전화율은 50% 이다.)
- 0.33
- 0.56
- 0.67
- 0.78
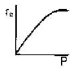
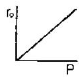
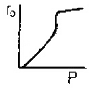
99. 고채 촉매 기상반응 A+B→C에서 초기속도 대전압(total pressure)의 plot는 보기의 그림과 같은 경우들이 있다. 반응물 A 및 B 모두가 촉매에 흡착된 후에 반응을 하며 표면반응이 율속단계일 경우 (surface reaction control)인 것은?
100. C5H5CH3+H2→C5H5+CH4의 틀루엔과 수소의 반응은 매우 빠른 반응이며 생성물은 평형 상태로 존재한다. 틀루엔의 초기 농도가 2mol/L, 수소의 초기 농도가 4mol/L이고 반응을 900K에서 진행 시켰을 때 반응 후 수소의 농도는 약 몇 mol/L인가? (단, 900K에서 평형상수 Kp=227 이다.)
- 1.89
- 1.95
- 2.01
- 4.04







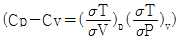
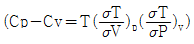

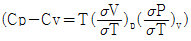
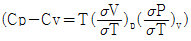 가 정답입니다.
가 정답입니다. }$에서 임계점(곡선과 점선의 교점)의 오른쪽 상단에 위치한 D 영역이 초임계영역에 해당합니다.
}$에서 임계점(곡선과 점선의 교점)의 오른쪽 상단에 위치한 D 영역이 초임계영역에 해당합니다. }$에서 $X_A = 0.4$인 지점을 수직으로 올리면, 액상선과 만나는 지점의 온도가 끓기 시작하는 온도($92\text{ ℃}$)이고, 기상선과 만나는 지점의 온도가 모든 액체가 증발하는 온도($100\text{ ℃}$)입니다.
}$에서 $X_A = 0.4$인 지점을 수직으로 올리면, 액상선과 만나는 지점의 온도가 끓기 시작하는 온도($92\text{ ℃}$)이고, 기상선과 만나는 지점의 온도가 모든 액체가 증발하는 온도($100\text{ ℃}$)입니다. }$에서 $X_A = 0.4$인 지점에서 접선을 그어 $X_A = 1.0$ 축(순수 A 성분 축)과 만나는 절편 값을 읽으면 $\overline{H}_A$의 값을 알 수 있습니다.
}$에서 $X_A = 0.4$인 지점에서 접선을 그어 $X_A = 1.0$ 축(순수 A 성분 축)과 만나는 절편 값을 읽으면 $\overline{H}_A$의 값을 알 수 있습니다.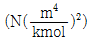
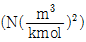
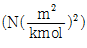
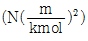
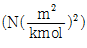 입니다.
입니다. 에서 B와 C를 잇는 밑변 쪽에 불혼화 영역(빗금친 부분)이 형성되어 있으므로, B와 C는 서로 잘 섞이지 않는 성분임을 알 수 있습니다.
에서 B와 C를 잇는 밑변 쪽에 불혼화 영역(빗금친 부분)이 형성되어 있으므로, B와 C는 서로 잘 섞이지 않는 성분임을 알 수 있습니다. 에서 $f(t-c)$는 $f(t)$가 오른쪽으로 $c$만큼 평행이동한 형태이므로, 이에 해당하는 변환은 $e^{-cs}L[f]$ 입니다.
에서 $f(t-c)$는 $f(t)$가 오른쪽으로 $c$만큼 평행이동한 형태이므로, 이에 해당하는 변환은 $e^{-cs}L[f]$ 입니다.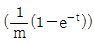
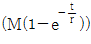
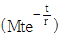
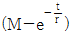
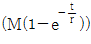 입니다.
입니다.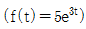
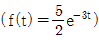
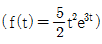

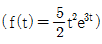 입니다.
입니다.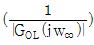
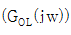
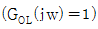
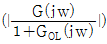
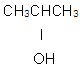 는 이소프로판올($$CH_3CH(OH)CH_3$$)로, 2차 알코올이므로 산화 시 아세톤이 생성됩니다.
는 이소프로판올($$CH_3CH(OH)CH_3$$)로, 2차 알코올이므로 산화 시 아세톤이 생성됩니다.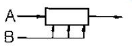
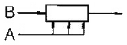

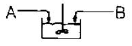
 방식이 가장 적절합니다.
방식이 가장 적절합니다.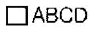

 영역이 반응 시간 $t$가 됩니다.
영역이 반응 시간 $t$가 됩니다.

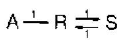

 가 정답입니다.
가 정답입니다.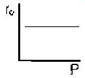
 가 정답입니다.
가 정답입니다.
$$\frac{P_1 V_1}{T_1} = \frac{P_2 V_2}{T_2}$$
$$\frac{1.4 \times 250}{294} = \frac{P_2 \times 300}{322}$$
$$P_2 \approx 1.3\text{ atm}$$