소방공무원(경력) 화학개론 2023-03-18 필기 기출문제 해설
이 페이지는 소방공무원(경력) 화학개론 2023-03-18 기출문제를 CBT 방식으로 풀이하고 정답 및 회원들의 상세 해설을 확인할 수 있는 페이지입니다.
소방공무원(경력) 화학개론
(2023-03-18 기출문제)
목록
1과목: 화학개론
2. 원소 13C의 중성자수는?
- 1
- 3
- 6
- 7
- 원자 번호는 양성자 수와 같으며, 질량수는 양성자 수와 중성자 수의 합입니다. 탄소($\text{C}$)의 원자 번호는 $6$이므로 양성자 수는 $6$개입니다.
$$\text{중성자 수} = \text{질량수} - \text{양성자 수}$$
$$\text{중성자 수} = 13 - 6$$
$$\text{중성자 수} = 7$$
3. 수산화 나트륨(NaOH) 용액 300mL에 NaOH 120g이 녹아 있을 때, 이 용액의 몰농도[M]는? (단, NaOH의 화학식량은 40 이다.)
- 10
- 40
- 160
- 300
- 용질의 몰수를 구한 뒤, 이를 용액의 부피(L)로 나누어 몰농도를 계산합니다.
① $M = \frac{w \div Mw}{V}$
② $M = \frac{120 \div 40}{0.3}$
③ $M = 10$
4. 원자가 껍질 전자쌍 반발(valence shell electron pair repulsion) 이론에 기초하여 예측한 포름알데히드(HCHO)의 분자 모양은?
- 선형
- 정사면체형
- 삼각쌍뿔형
- 평면삼각형
- 포름알데히드($\text{HCHO}$)의 중심 원자인 $\text{C}$는 2개의 $\text{H}$와 1개의 $\text{O}$와 결합하여 총 3개의 전자 영역을 가집니다. VSEPR 이론에 따라 전자 영역이 3개일 때 가장 안정한 구조는 평면삼각형입니다.
5. 밑줄 친 원소 중 가장 큰 산화수를 갖는 것은?
- 화합물 내 각 원소의 산화수를 계산하여 비교합니다. $\text{F}$는 항상 $-1$이며, $\text{S}$는 $\text{F}$ 6개와 결합하여 전체 전하가 $0$이 되어야 하므로 가장 큰 산화수를 갖습니다.
산화수 계산
$\text{SF}_6$에서 $\text{S}$의 산화수: $x + 6(-1) = 0 \rightarrow x = +6$
6. 음이온의 화학식과 이름이 옳지 않은 것은?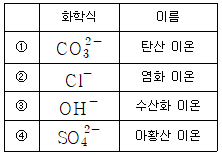
- ①
- ②
- ③
- ④
- $\text{SO}_4^{2-}$의 올바른 이름은 황산 이온입니다. 마황산 이온은 잘못된 명칭입니다.
오답 노트
$\text{CO}_3^{2-}$: 탄산 이온 (옳음)
$\text{Cl}^-$: 염화 이온 (옳음)
$\text{OH}^-$: 수산화 이온 (옳음)
7. 분자 오비탈에 대한 설명으로 옳지 않은 것은?
- 결합 차수가 커지면 결합 길이도 길어진다.
- 분자 오비탈 이론으로 산소 분자의 상자기성을 설명할 수 있다.
- 개의 원자 오비탈이 겹쳐지면 개의 분자 오비탈이 생긴다.
- 반결합성 분자 오비탈의 에너지는 분자를 형성하는 원자 오비탈의 에너지보다 높다.
- 결합 차수가 커질수록 원자 사이의 결합력이 강해져 결합 길이는 오히려 짧아집니다.
오답 노트
산소 분자의 상자기성: 홀전자가 존재하여 설명 가능
오비탈 수 보존: $n$개의 원자 오비탈이 겹치면 $n$개의 분자 오비탈 생성
반결합성 오비탈: 원자 오비탈보다 에너지가 높음
8. 용액의 농도를 나타내는 방법 중 온도에 따라 변할 수 있는 것은? (단, 용액은 증발하지 않는다고 가정한다.)
- 몰농도
- 몰분율
- 몰랄 농도
- 질량 백분율
- 몰농도는 용액의 부피를 기준으로 정의되는데, 액체의 부피는 온도 변화에 따라 팽창하거나 수축하므로 온도에 따라 농도 값이 변하게 됩니다.
오답 노트
몰분율, 몰랄 농도, 질량 백분율: 질량이나 몰수 기반으로 정의되어 온도 변화에 영향을 받지 않음
9. 990g의 미지 시료를 분석했을 때 558g의 인(P)과 432g의 산소(O)가 들어 있고, 다른 원소는 검출되지 않았다. 이 시료의 실험식은? (단, P와 O의 원자량은 각각 31과 16이다.)
- PO3
- P2O3
- P2O5
- P3O5
- 각 원소의 질량을 원자량으로 나누어 몰수 비를 구하면 가장 간단한 정수비인 실험식을 얻을 수 있습니다.
① [기본 공식] $\text{몰수} = \frac{\text{질량}}{\text{원자량}}$
② [숫자 대입] $\text{P} : \text{O} = \frac{558}{31} : \frac{432}{16} = 18 : 27$
③ [최종 결과] $\text{P} : \text{O} = 2 : 3 \rightarrow \text{P}_2\text{O}_3$
10. 염색공장에서 발생한 6M의 황산(H2SO4) 용액 2m3를 4M의 수산화 나트륨(NaOH) 용액으로 중화하는 데 필요한 NaOH 용액의 양[m3]은?
- 2
- 3
- 6
- 12
- 중화 반응의 원리에 따라 산의 당량수(노르말 농도 $\times$ 부피)와 염기의 당량수가 같아야 합니다. 황산은 2가 산, 수산화 나트륨은 1가 염기임을 이용합니다.
① [기본 공식] $M_{\text{NaOH}} \times V_{\text{NaOH}} = 2 \times M_{\text{H}_2\text{SO}_4} \times V_{\text{H}_2\text{SO}_4}$
② [숫자 대입] $4 \times V_{\text{NaOH}} = 2 \times 6 \times 2$
③ [최종 결과] $V_{\text{NaOH}} = 6$
11. 다음은 0℃, 1atm 에서 프로페인(C3H8)의 연소 반응식이다. 프로페인 2L가 완전 연소할 때 생성되는 이산화 탄소(CO2)의 부피[L]는? (단, 기체는 이상 기체이다.)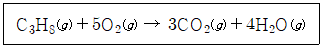
- 2
- 3
- 5
- 6
- 아보가드로 법칙에 따라 온도와 압력이 일정할 때 기체의 부피비는 화학 반응식의 계수비와 같습니다.
① [기본 공식] $\text{CO}_2 \text{ 부피} = \text{C}_3\text{H}_8 \text{ 부피} \times \frac{3}{1}$
② [숫자 대입] $\text{CO}_2 \text{ 부피} = 2 \times 3$
③ [최종 결과] $\text{CO}_2 \text{ 부피} = 6$
12. 4V의 배터리로 30분 동안 2A의 일정한 전류를 보낼 때, 배터리가 행한 전기적 일[kg]은?
- 3.6
- 14.4
- 3,600
- 14,400
- 전기적 일은 전압, 전류, 시간의 곱으로 계산하며, 단위는 줄(J)입니다. $1\text{kJ} = 1000\text{J}$ 임을 이용하여 단위를 변환합니다.
① [기본 공식] $W = V \times I \times t$
② [숫자 대입] $W = 4 \times 2 \times (30 \times 60)$
③ [최종 결과] $W = 14400\text{J} = 14.4\text{kJ}$
13. 300K에서 다음 반응의 △G°[kJ/mol]는? 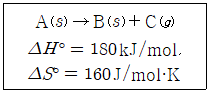
(단, G°는 표준 깁스 자유 에너지(standard Gibbs free energy), H°는 표준 엔탈피(standard enthalpy), S°는 표준 엔트로피(standard entropy)이다.)
- -180
- -48
- 132
- 180
- 표준 깁스 자유 에너지 변화량은 엔탈피 변화량에서 온도와 엔트로피 변화량의 곱을 빼서 계산합니다.
① [기본 공식] $\Delta G = \Delta H - T\Delta S$
② [숫자 대입] $\Delta G = 180 - 300 \times (160 \times 10^{-3})$
③ [최종 결과] $\Delta G = 132$
14. 주양자수(n)가 4일 때, 오비탈과 양자수에 대한 설명으로 옳지 않은 것은?
- 각운동량 양자수(l)는 0, 1, 2, 3 이다.
- 껍질 내의 전체 오비탈 수는 16개이다.
- 부껍질에는 4s, 4p, 4d, 4f가 포함된다.
- 자기 양자수(ml)는 0을 포함한 -4에서 4까지의 정숫값을 갖는다.
- 주양자수 $n=4$일 때 각 양자수의 범위와 성질을 분석합니다.
각운동량 양자수 $l$은 $0$부터 $n-1$까지 가능하므로 $0, 1, 2, 3$이 맞으며, 이에 따라 $4s, 4p, 4d, 4f$ 부껍질이 존재합니다. 전체 오비탈 수는 $n^{2} = 4^{2} = 16$개입니다.
오답 노트
자기 양자수 $m_{l}$은 $-l$부터 $+l$까지의 정수 값을 가집니다. $n=4$에서 $l$의 최댓값은 $3$이므로, $m_{l}$은 $-3$에서 $3$까지의 정수 값을 가져야 합니다.
15. 다음은 T℃에서 A(g)와 B(g)가 반응하여 C(g)가 생성되는 반응이다. 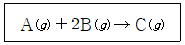
표가 A와 B의 초기 몰농도에 따른 반응 속도를 나타낼 때, 반응 속도 법칙은? (단, k는 속도 상수이고, [A]와 [B]는 각각 A와 B의 몰농도이다.)
- 속도 = k[A]2
- 속도 = k[A][B]2
- 속도 = k[A]3
- 속도 = k[A]3[B]
- 초기 농도 변화에 따른 반응 속도의 변화를 통해 반응 차수를 결정합니다.
B의 농도가 $0.15$에서 $0.45$로 3배 증가했을 때 속도가 $0.3$으로 일정하므로 B에 대한 반응 차수는 0차입니다.
A의 농도가 $0.15$에서 $0.3$으로 2배 증가했을 때 속도가 $0.3$에서 $2.4$로 8배($2^{3}$) 증가했으므로 A에 대한 반응 차수는 3차입니다.
따라서 반응 속도 법칙은 $\text{속도} = k[A]^{3}$ 입니다.
16. (가)와 (나)는 두 완충 용액의 해리 평형식이다. 완충 용액의 pH가 각각 6.4일 때, 각 완충 용액의 산과 염기의 상대적인 농도를 비교한 것으로 옳은 것은? (단, Ka는 산 해리 상수이다.)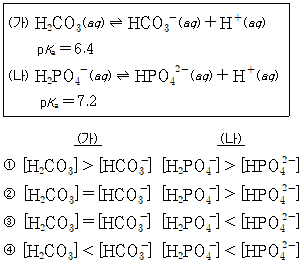
- ①
- ②
- ③
- ④
- 헨더슨-하셀바흐 식에 따르면 $pH = pK_{a} + \log \frac{[\text{염}]}{[\text{산}]}$ 입니다.
(가)는 $pH = 6.4$이고 $pK_{a} = 6.4$이므로 $\log \frac{[\text{HCO}_{3}^{-}]}{[\text{H}_{2}\text{CO}_{3}]} = 0$이 되어 $[\text{H}_{2}\text{CO}_{3}] = [\text{HCO}_{3}^{-}]$ 입니다.
(나)는 $pH = 6.4$이고 $pK_{a} = 7.2$이므로 $6.4 = 7.2 + \log \frac{[\text{HPO}_{4}^{2-}]}{[\text{H}_{2}\text{PO}_{4}^{-}]}$가 되어 $\log \frac{[\text{HPO}_{4}^{2-}]}{[\text{H}_{2}\text{PO}_{4}^{-}]} = -0.8$ 입니다. 따라서 $[\text{H}_{2}\text{PO}_{4}^{-}] > [\text{HPO}_{4}^{2-}]$가 됩니다.
17. 국제 단위계(SI unit) 기본 단위의 물리량과 단위 기호로 옳은 것은?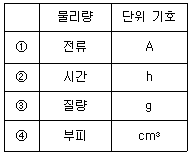
- ①
- ②
- ③
- ④
- 국제 단위계(SI)의 7가지 기본 단위와 그 기호를 정확히 암기해야 하는 문제입니다.
전류의 SI 기본 단위는 암페어(A)가 맞습니다.
오답 노트
시간: 기본 단위는 초(s)입니다.
질량: 기본 단위는 킬로그램(kg)입니다.
부피: 기본 단위가 아니며, 유도 단위인 세제곱미터($\text{m}^3$)를 사용합니다.
18. 다음 화학 반응식의 계수를 바르게 나열한 것은?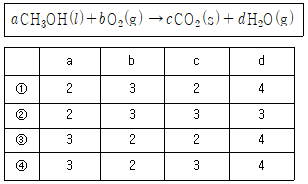
- ①
- ②
- ③
- ④
- 화학 반응식의 양변에서 각 원소의 원자 수가 동일하도록 계수를 맞춥니다.
반응식: $aCH_{3}OH(l) + bO_{2}(g) \rightarrow cCO_{2}(s) + dH_{2}O(g)$
C 원자 수: $a = c$
H 원자 수: $4a = 2d \rightarrow 2a = d$
O 원자 수: $a + 2b = 2c + d$
$a=2$일 때, $c=2, d=4$가 되며, $2 + 2b = 4 + 4$에서 $2b = 6$이므로 $b=3$입니다.
따라서 계수는 $a=2, b=3, c=2, d=4$인 조합이 정답입니다.
19. ZN2+ + 2e- → Zn의 환원 반응을 통해 금속 물체에 아연을 도금한다. 이때 충분한 양의 아연 이온이 수용액 속에 녹아 있다면, 0.0005mol 의 아연을 금속 물체에 도금하기 위해서 0.1A의 전류를 몇 초간 흘려줘야 하는가? (단, 패러데이 상수는 96,000 C/mol이고, 모든 전류는 아연 이온의 환원 반응에만 사용된다.)
- 960초
- 1,920초
- 9,600초
- 19,200초
- 전하량과 물질량의 관계를 이용하여 도금에 필요한 시간을 계산합니다.
① [기본 공식] $t = \frac{n \times z \times F}{I}$ (시간 = (물질량 $\times$이동 전자 수 $\times$ 패러데이 상수) / 전류)
② [숫자 대입] $t = \frac{0.0005 \times 2 \times 96000}{0.1}$
③ [최종 결과] $t = 960$
20. HClO3에서 염소(Cl)의 산화수는?
- 3
- 4
- 5
- 7
- 화합물 $\text{HClO}_3$에서 수소($\text{H}$)의 산화수는 $+1$, 산소($\text{O}$)의 산화수는 $-2$입니다. 전체 전하량이 $0$이 되어야 하므로 염소($\text{Cl}$)의 산화수를 $x$라 하면 다음과 같습니다.
$$+1 + x + (-2 \times 3) = 0$$
$$x - 5 = 0$$
따라서 염소($\text{Cl}$)의 산화수는 $5$입니다.
21. 염화 소듐(NaCl)의 단위 세포를 그림과 같이 나타낼 때, 이에 대한 설명으로 옳지 않은 것은? (단, r+와 r-는 각각 양이온과 음이온의 이온 반지름이다.)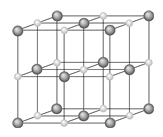
- r+/r-는 CsCl보다 크다.
- MgO보다 녹는점이 낮다.
- Cl-이온은 면심 입방 구조를 이룬다.
- 양이온과 음이온의 배위수는 각각 6 이다.
- NaCl은 면심 입방 구조(Rock salt 구조)로, 양이온과 음이온의 반지름 비가 CsCl(체심 입방 구조)보다 작습니다. 따라서 $r_{+}/r_{-}$ 값은 CsCl보다 작아야 합니다.
오답 노트
MgO보다 녹는점이 낮다: MgO는 결합력이 더 강한 $2+$ $2-$이온 결합이므로 NaCl의 녹는점이 더 낮음
Cl$^{-}$이온은 면심 입방 구조를 이룬다: 음이온이 FCC 구조를 형성하고 그 사이 공간에 양이온이 위치함
양이온과 음이온의 배위수는 각각 6 이다: 각 이온은 6개의 반대 전하 이온에 둘러싸여 있음
22. 바닥 상태의 전자 배치로 옳은 것은?
- Al : 1s22s22p63s23p2
- P : 1s22s22p63s23p3
- S2- : 1s22s22p63s23p5
- Ca2+ : 1s22s22p63s23p64s1
- 쌓음 원리에 따라 에너지가 낮은 오비탈부터 차례대로 전자가 채워져야 합니다. P(인)은 원자 번호 15번으로 $1s^{2}2s^{2}2p^{6}3s^{2}3p^{3}$ 배치가 정확합니다.
오답 노트
Al : 원자 번호 13번으로 $3p$ 전자는 1개여야 함
S$^{2-}$ : 황화 이온은 전자를 얻어 아르곤($Ar$)과 같은 전자 배치($3p^{6}$)를 가져야 함
Ca$^{2+}$ : 칼슘 이온은 최외각 $4s$ 전자를 잃어 $3p^{6}$에서 끝나야 함
23. 질량이 200g이고, 온도가 80℃인 고체 X를 20℃의 물 500g이 담긴 스티로폼 컵에 넣었다. 이 계가 열 평형 온도 30℃에 도달했을 때, 물체 X의 비열[J/g·K]은? (단, 물의 비열은 4J/g·K이고, 컵의 비열은 무시한다.)
- 1
- 2
- 4
- 10
- 고체 X가 잃은 열량과 물이 얻은 열량이 같다는 열량 보존 법칙을 이용하여 비열을 구합니다.
① $Q = m \times c \times \Delta T$
② $200 \times c \times (80 - 30) = 500 \times 4 \times (30 - 20)$
③ $c = 2$
24. 원자가 결합 이론(valence bond theory)에 따라 원자 오비탈이 혼성 오비탈을 형성할 때, 에틸렌(C2H4)에서 탄소 원자의 혼성 오비탈은?
- sp
- sp2
- sp3
- dsp
- 에틸렌($\text{C}_2\text{H}_4$)의 탄소 원자는 인접한 탄소 1개와 수소 2개, 총 3개의 원자와 시그마 결합을 형성하며 평면 삼각형 구조를 가집니다. 따라서 탄소의 혼성 오비탈은 $\text{sp}^2$입니다.
25. 화학 반응 (가)~(다)에서 환원제로 작용하는 물질은?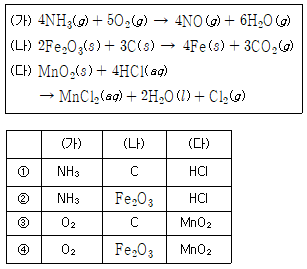
- ①
- ②
- ③
- ④
- 환원제는 자신은 산화되면서 다른 물질을 환원시키는 물질로, 산화수 증가 여부를 확인합니다.
(가) $4\text{NH}_3 + 5\text{O}_2 \rightarrow 4\text{NO} + 6\text{H}_2\text{O}$ : $\text{N}$의 산화수가 $-3$에서 $+2$로 증가하므로 $\text{NH}_3$가 환원제입니다.
(나) $2\text{Fe}_2\text{O}_3 + 3\text{C} \rightarrow 4\text{Fe} + 3\text{CO}_2$ : $\text{C}$의 산화수가 $0$에서 $+4$로 증가하므로 $\text{C}$가 환원제입니다.
(다) $\text{MnO}_2 + 4\text{HCl} \rightarrow \text{MnCl}_2 + 2\text{H}_2\text{O} + \text{Cl}_2$ : $\text{Cl}$의 산화수가 $-1$에서 $0$으로 증가하므로 $\text{HCl}$이 환원제입니다.
26. 화학 평형(chemical equilibrium)에 대한 설명으로 옳지 않은 것은?
- 평형식은 반응 메커니즘에 따라 달라진다.
- 화학 평형에서 정반응과 역반응의 속도는 같다.
- 정반응의 평형식은 역반응의 평형식의 역수이다.
- 평형에 있는 어떤 계에 변화가 가해지면, 그 변화를 감소시키려는 방향으로 평형의 위치는 이동한다.
27. (가)~(다)는 25℃에서의 열화학 반응을 나타낸 것이다. 반응 ClF(g) + F2(g) → ClF3(g)의 △H[kJ/mol]는?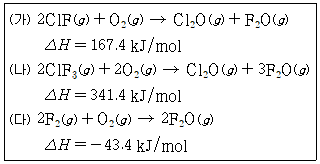
- -217.4
- -130.2
- -108.7
- 217.4
- 헤스의 법칙을 이용하여 주어진 반응식들을 조합해 목표 반응식 $\text{ClF(g)} + \text{F}_2\text{(g)} \rightarrow \text{ClF}_3\text{(g)}$의 엔탈피 변화를 구합니다.
목표 식 = $\frac{1}{2}$(가) + $\frac{1}{2}$(다) - $\frac{1}{2}$(나)
① $\Delta H = \frac{1}{2}\Delta H_{(가)} + \frac{1}{2}\Delta H_{(다)} - \frac{1}{2}\Delta H_{(나)}$
② $\Delta H = \frac{1}{2}(167.4) + \frac{1}{2}(-43.4) - \frac{1}{2}(341.4)$
③ $\Delta H = -108.7$
28. 산과 염기에 대한 설명으로 옳지 않은 것은?
- 황산(H2SO4)은 이양성자산이다.
- 루이스 염기는 전자쌍 받개이다.
- 브뢴스테드-로리 산은 양성자를 주는 물질이다.
- 아레니우스 산-염기 개념은 수용액에만 적용된다.
29. 기체 분자 운동론(kinetic molecular theory of gas)에 대한 설명으로 옳지 않은 것은?
- 입자의 크기는 무시할 수 있을 정도로 작다.
- 입자의 평균 운동 에너지는 절대 온도에 반비례한다.
- 한 입자와 다른 입자(또는 벽)의 충돌은 완전 탄성 충돌이다.
- 입자 사이의 인력과 반발력은 무시할 수 있을 정도로 작다.
30. 아세틸렌(C2H2) 을 완전 연소시킬 때 필요한 산소(O2)의 질량[g]과 이때 생성되는 물(H2O)의 질량[g]은? (단, C, H, O의 원자량은 각각 12, 1, 6이다.)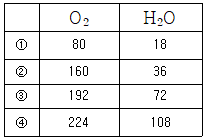
- ①
- ②
- ③
- ④
- 아세틸렌의 완전 연소 반응식 $2C_{2}H_{2} + 5O_{2} \rightarrow 4CO_{2} + 2H_{2}O$를 통해 화학 양론적 질량을 계산합니다.
이미지 의 조건에서 아세틸렌 $2\text{ mol}$($54\text{ g} \times 2 = 108\text{ g}$)이 반응한다고 가정할 때:
의 조건에서 아세틸렌 $2\text{ mol}$($54\text{ g} \times 2 = 108\text{ g}$)이 반응한다고 가정할 때:
① [산소 질량 공식]
$$\text{Mass}_{O_{2}} = \text{mol}_{O_{2}} \times M_{O_{2}}$$
② [숫자 대입]
$$\text{Mass}_{O_{2}} = 5\text{ mol} \times 32\text{ g/mol}$$
③ [최종 결과]
$$\text{Mass}_{O_{2}} = 160\text{ g}$$
생성되는 물의 질량:
① [물 질량 공식]
$$\text{Mass}_{H_{2}O} = \text{mol}_{H_{2}O} \times M_{H_{2}O}$$
② [숫자 대입]
$$\text{Mass}_{H_{2}O} = 2\text{ mol} \times 18\text{ g/mol}$$
③ [최종 결과]
$$\text{Mass}_{H_{2}O} = 36\text{ g}$$
31. 온도 T℃에서 산소(O2) 기체 분자의 분출(effusion) 속도가 500m/s일 때, 같은 온도에서 수소(H2) 기체 분자의 분출 속도[m/s]는? (단, 기체는 그레이엄의 분출 법칙(Graham's law of effusion)을 따르고, O2와 H2의 화학식량은 각각 32와 2이다.)
- 500
- 1,000
- 1,500
- 2,000
- 그레이엄의 분출 법칙에 따라 기체의 분출 속도는 분자량의 제곱근에 반비례합니다.
① [기본 공식]
$$\frac{v_{H_{2}}}{v_{O_{2}}} = \sqrt{\frac{M_{O_{2}}}{M_{H_{2}}}}$$
② [숫자 대입]
$$\frac{v_{H_{2}}}{500} = \sqrt{\frac{32}{2}}$$
③ [최종 결과]
$$v_{H_{2}} = 2000$$
32. 화학 반응 (가)와 (나)의 평형 상수 K1과 K2를 이용하여 2Cu(s) + O2(g) ⇌ 2CuO(s)의 평형 상수를 표현한 것으로 옳은 것은?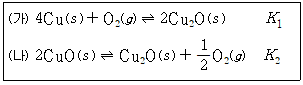
- (K1)(K2)
- (K1)(K2)0.5
- (K1)0.5/(K2)
- (K1)/(K2)2
- 목표 반응식 $2Cu(s) + O_{2}(g) \rightleftharpoons 2CuO(s)$를 만들기 위해 주어진 반응식을 조합합니다.
먼저 반응 (가) $4Cu(s) + O_{2}(g) \rightleftharpoons 2Cu_{2}O(s)$에 $0.5$를 곱하면 $2Cu(s) + 0.5O_{2}(g) \rightleftharpoons Cu_{2}O(s)$가 되며, 이때 평형 상수는 $K_{1}^{0.5}$가 됩니다.
다음으로 반응 (나) $2CuO(s) \rightleftharpoons Cu_{2}O(s) + 0.5O_{2}(g)$를 역반응으로 뒤집으면 $Cu_{2}O(s) + 0.5O_{2}(g) \rightleftharpoons 2CuO(s)$가 되며, 이때 평형 상수는 $1/K_{2}$가 됩니다.
두 식을 더하면 목표 반응식이 도출되므로, 최종 평형 상수는 두 상수의 곱인 $(K_{1})^{0.5}/(K_{2})$가 됩니다.
33. 25℃물에서 HCN의 산 해리 상수는 6.2×10-10이고, HF의 산 해리 상수는 6.6×10-4이며, HPO42-의 산 해리 상수는 2.2×10-13일 때, 이온의 염기 세기를 순서대로 옳게 나열한 것은?
- F- > PO43- > CN-
- F- > CN- > PO43-
- PO43- > CN- > F-
- CN- > F- > PO43-
- 산 해리 상수($K_a$)가 작을수록 짝염기의 세기는 강해집니다. 주어진 $K_a$ 값의 크기를 비교하면 $HPO_4^{2-} < HCN < HF$ 순으로 작으므로, 짝염기의 세기는 그 역순인 $PO_4^{3-} > CN^- > F^-$가 됩니다.
34. 일정 온도에서 5L, 600mmHg의 뷰테인(C4H10(g))이 2L로 변화했을 때의 압력[mmHg]은? (단, 기체는 이상 기체이다.)
- 600
- 900
- 1,200
- 1,500
- 온도가 일정할 때 기체의 압력과 부피는 반비례한다는 보일의 법칙을 적용합니다.
① [기본 공식] $P_1 V_1 = P_2 V_2$
② [숫자 대입] $600 \times 5 = P_2 \times 2$
③ [최종 결과] $P_2 = 1500$
35. 산소(O2) 16.0g과 메테인(CH4) 8.0g의 기체 혼합물을 0℃에서 22.4L 용기에 채웠다. 이 기체 혼합물이 들어 있는 용기의 전체 압력[atm]은? (단, 모든 기체는 이상 기체이고, 기체 상수는 0.08206 L·atm/mol·K 이다. C, H, O의 원자량은 각각 12, 1, 16이다.)
- 0.5
- 1.0
- 1.5
- 2.0
- 각 기체의 몰수를 구한 뒤, 이상 기체 상태 방정식($$PV = nRT$$)을 이용하여 혼합 기체의 전체 압력을 계산합니다.
먼저 각 기체의 몰수를 구합니다.
산소( $O_{2}$)의 몰수: $$n_{O_{2}} = \frac{16.0}{32} = 0.5 \text{ mol}$$
메테인( $CH_{4}$)의 몰수: $$n_{CH_{4}} = \frac{8.0}{16} = 0.5 \text{ mol}$$
전체 몰수: $n_{total} = 0.5 + 0.5 = 1.0 \text{ mol}$
전체 압력 계산 과정은 다음과 같습니다.
① [기본 공식] $P = \frac{nRT}{V}$
② [숫자 대입] $P = \frac{1.0 \times 0.08206 \times 273.15}{22.4}$
③ [최종 결과] $P = 1.0 \text{ atm}$
36. 다음 침전 반응에 포함된 구경꾼 이온만으로 짝 지어진 것은?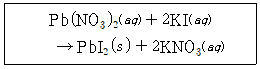
- Pb2+, I-
- Pb2+, NO3-
- K+, I-
- K+, NO3-
- 제시된 반응식
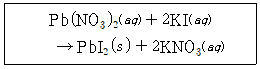 에서 $\text{PbI}_{2}$는 침전물로 생성되어 반응에 직접 참여하지만, $\text{K}^{+}$와 $\text{NO}_{3}^{-}$이온은 반응 전후에 상태 변화 없이 용액 속에 그대로 남아 있는 구경꾼 이온입니다.
에서 $\text{PbI}_{2}$는 침전물로 생성되어 반응에 직접 참여하지만, $\text{K}^{+}$와 $\text{NO}_{3}^{-}$이온은 반응 전후에 상태 변화 없이 용액 속에 그대로 남아 있는 구경꾼 이온입니다.
37. 초기 온도가 95℃인 물 0.05kg에서 1,200J의 열이 방출되었을 때, 물의 최종 온도[℃]는? (단, 물의 비열은 4J/g·K 이다.)
- 6
- 35
- 60
- 89
- 물질이 방출한 열량은 비열, 질량, 온도 변화의 곱으로 계산합니다.
① [기본 공식] $Q = c \times m \times \Delta T$
② [숫자 대입] $1200 = 4 \times 50 \times (95 - T_{final})$
③ [최종 결과] $T_{final} = 89$
38. 주양자수(n)가 3이고 각운동량 양자수(l)가 2인 오비탈에 들어갈 수 있는 최대 전자수는?
- 2
- 6
- 10
- 14
- 주양자수 $n=3$이고 각운동량 양자수 $l=2$인 오비탈은 $3d$ 오비탈을 의미합니다. $d$ 오비탈은 자기 양자수 $m_{l}$이 $-2, -1, 0, 1, 2$로 총 5개의 오비탈이 존재하며, 각 오비탈에는 스핀 방향이 다른 전자가 최대 2개씩 들어갈 수 있으므로 최대 전자수는 $5 \times 2 = 10$개입니다.
39. 격자 에너지는 고체 이온 결합 화합물 1몰의 모든 이온을 기체 상태의 이온으로 완전히 분리하는 데 필요한 에너지이다. 다음 자료를 본-하버 순환(Born-Haber cycle)에 적용하여 계산한 RbCl의 격자 에너지[kJ/ol]는? (단, I1은 1차 이온화 에너지, EA는 전자 친화도이다.)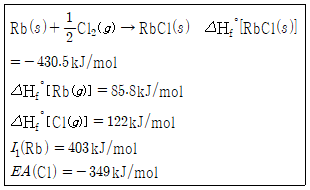
- -46.7
- -168.7
- 692.3
- 861.0
- 본-하버 순환에 따라 생성 엔탈피는 승화 엔탈피, 이온화 에너지, 결합 해리 에너지, 전자 친화도, 격자 에너지의 합과 같습니다. 격자 에너지를 구하기 위해 전체 에너지 평형 식을 세워 계산합니다.
① [기본 공식] $\Delta H_{f} = \Delta H_{sub} + I_{1} + \frac{1}{2}D + EA + U$
② [숫자 대입] $-430.5 = 85.8 + 403 + 122 + (-349) + U$
③ [최종 결과] $U = 692.3$
40. 다음은 오존(O3)의 분해 반응 2O3(g) ⇌ 3O2(g)에 대한 반응 메커니즘이다. 2단계가 속도 결정 단계이고, 1단계 평형은 2단계에 비해 훨씬 빠르다고 가정할 때, O3 분해 반응의 속도식은? (단, k는 속도 상수이다.)
- 속도 = k[O3]
- 속도 = k[O3]2
- 속도 = k[O3]2[O2]
- 속도 = k[O3]2[O2]-1
- 속도 결정 단계(2단계)의 속도식을 먼저 세우고, 1단계 평형 식을 이용해 중간체 $\text{O}$의 농도를 치환하여 구합니다.
① [기본 공식]
$$\text{rate} = k_2[\text{O}_3][\text{O}]$$
$$\text{K}_{eq} = \frac{[\text{O}_2][\text{O}]}{[\text{O}_3]} \rightarrow [\text{O}] = \frac{\text{K}_{eq}[\text{O}_3]}{[\text{O}_2]}$$
② [숫자 대입]
$$\text{rate} = k_2[\text{O}_3] \times \frac{\text{K}_{eq}[\text{O}_3]}{[\text{O}_2]}$$
③ [최종 결과]
$$\text{rate} = k[\text{O}_3]^2[\text{O}_2]^{-1}$$






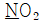
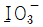
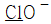
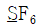
오답 노트
$1\times 10^{-12}\text{mm}$: $10^{-15}\text{m}$이므로 틀림
$1\times 10^{2}\text{pm}$: $10^{-10}\text{m}$이므로 틀림
$1\times 10^{-2}\mu\text{m}$: $10^{-8}\text{m}$이므로 틀림