1과목: 과목 구분 없음
1. 점도(viscosity)의 단위가 아닌 것은?
- Nㆍs2ㆍm-2
- kgㆍs-1ㆍm-1
- cP
- Paㆍs
2. 타일러(Tyler) 표준체(standard sieve)의 규격에서 200메시(mesh) 체의 경우 1 in2 안에 있는 체 구멍의 수는?
- 200
- 400
- 20,000
- 40,000
3. 유체가 역류하는 것을 막는 데 사용하는 밸브는?
- 게이트 밸브(gate valve)
- 체크 밸브(check valve)
- 코크 밸브(cock valve)
- 글로브 밸브(globe valve)
4. 1.0M NaOH 수용액 200 mL와 2.4M NaOH 수용액 500 mL를 혼합한 NaOH 수용액의 몰농도[M]는? (단, NaOH 수용액은 이상용액이다)
- 1.2
- 1.6
- 2.0
- 2.2
5. 화학공업 경제성 분석에서 손익분기점(break-even point)에 대한 설명으로 옳지 않은 것은?
- 총생산비와 총수입 직선의 교점으로 나타낸다.
- 생산속도와 운전시간 비용을 고려하여 구한다.
- 생산용량과 판매 수요량을 조절하는 기준으로 사용한다.
- 생산활동에 사용된 자산의 소비를 나타내어 제조원가에 반영 할 때 활용한다.
6. 화학공장의 설비를 10억 원을 들여 설치하여 매년 5천만 원의 추가이익을 올렸다. 이 설비에 대한 내구연한은 10년이었으나, 설치 후 5년간 사용한 현재, 신규 설비가 개발되어 기존 설비를 대체하고자 한다. 설비의 감가상각이 선형적이라고 할 때, 손해를 보지 않고 새로운 설비로 대체하기 위한 기존 설비의 최소 매각 가격[원]은?
- 3억
- 2억 5천만
- 2억
- 1억 5천만
7. 기체의 상태법칙에 대한 내용으로 옳지 않은 것은?
- 온도가 일정할 때, 이상기체의 부피는 절대압력에 반비례한다.
- 압력이 일정할 때, 일정량의 이상기체가 차지하는 부피는 온도가 1°C씩 상승함에 따라 25°C 때의 부피보다 1/273.15 만큼씩 증가한다.
- 일정온도에서 이상기체 혼합물의 전체압력은 각 성분의 부분압력을 합한 것과 같다.
- 대응상태 원리에 따르면, 동일한 환산온도와 환산압력에서는 모든 기체의 압축인자는 근사적으로 같다.
8. 다음 그림의 엔진 cycle에서 열이 엔진으로 들어오는 구간들로만 모은 것은? (단, P는 압력, V는 부피, 구간 1→2와 구간 4→5는 등엔트로피 과정들이다)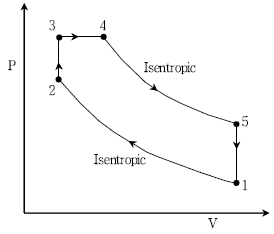
- 1→2, 4→5
- 2→3, 3→4
- 2→3, 5→1
- 3→4, 4→5
9. 30.0 kg의 탄소를 태워 이산화탄소 44.0wt%와 일산화탄소 56.0wt%로 구성된 생성물을 얻었다. 이 중 이산화탄소의 양[kg]은? (단, 탄소와 산소의 원자량은 각각 12.0 amu와 16.0 amu로 간주한다)
- 36.7
- 43.2
- 46.7
- 74.0
10. 전기로의 벽은 두께 0.33 m의 벽돌과 두께 0.13m의 석면으로 된 이중벽이다. 전기로의 내면온도가 316 °C이고 외면온도가 30 °C일 때, 벽에서 손실된 열량[kcal/hrㆍm2]은? (단, 벽돌과 석면의 열전도도는 각각 1.1 kcal/mㆍhrㆍ°C, 0.13 kcal/mㆍhrㆍ°C이다)
- 200
- 216
- 220
- 256
11. 분리조작에 대한 설명으로 옳지 않은 것은?
- 기상 중 입자가 부유하는 상태를 에어로졸(aerosol)이라 한다.
- 액상 중 입자가 부유하는 상태를 서스펜션(suspension)이라 한다.
- 기체 중에 부유하고 있는 고체나 액체의 입자를 포집하는 조작을 집진이라 한다.
- 원심력에 의해 입자를 분리하는 대표적인 장치는 스크러버(scrubber)이다.
12. 점토의 진밀도가 2.0 g/cm3이고 겉보기밀도가 1.2 g/cm3일 때, 공극률은?
- 0.8
- 0.6
- 0.4
- 0.2
13. 화학공정을 제어하기 위해서는 각종 신호를 빨리 피드백해 주는 제어기가 필수적이다. 온도 제어와 관련된 다양한 제어 방식에 대한 설명으로 옳지 않은 것은?
- 미분 제어기는 온도 편차의 변화속도에 비례하여 조작되지만 잔류편차를 제거하지는 않는다.
- 비례-적분 제어기는 온도 제어에 많은 시간이 소요될 수 있다.
- 비례-미분 제어기는 온도가 과도하게 상승하는 것을 막을 수 있다.
- 비례-적분-미분 제어기를 사용하면 과도한 온도상승 억제와 빠른 안정화를 동시에 이룰 수 있다.
14. 2A+B →3C인 기초반응(elementary reaction)에 대해 동일한 온도에서 A의 농도를 2배 증가시키고 B의 농도를 반으로 감소시킬 때, 반응속도는?
- 반으로 감소한다.
- 2배 증가한다.
- 4배 증가한다.
- 변하지 않는다.
15. 다음 그림에서 세 가지 서로 다른 고체물질 A, B, C의 평판들이 서로 밀착되어 복합체를 이루고 있다. 정상상태에서의 각 부위별 온도(T1, T2, T3, T4) 분포가 그림과 같다면, A, B, C 중에서 열전도도가 가장 큰 물질은? (단, T1 >T2 > T3이다.)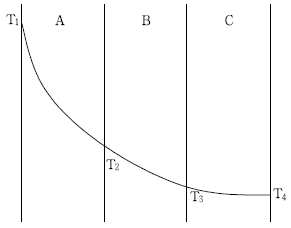
- A
- B
- C
- 판단하기 어렵다.
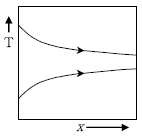
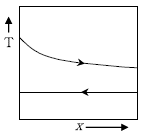
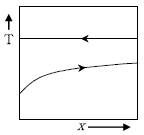
16. 평행유동(parallel flow) 열교환기 또는 대향유동(counter flow)열교환기에서 응축하는 증기를 사용하는 경우 열교환기의 온도 분포로 옳은 것은? (단, T는 온도, x는 열교환기에서의 위치이며, 화살표 →와 ←는 흐름의 방향을 의미한다)
17. 같은 무게의 A와 B를 혼합한 이상용액의 경우, 70 °C에서 기체상의 전체 압력[mmHg]은? (단, A와 B의 분자량은 각각 60 g/mol과 90 g/mol이고, 70 °C에서 순수한 A와 B의 증기압은 각각 500 mmHg와 300 mmHg이다)
- 120
- 420
- 540
- 800
18. 밀도가 0.5 g/cm3이고 유량이 157 g/s인 유체가 지름이 1 cm인 배관을 통하여 흐르다가 지름이 2 cm인 배관으로 흐르게 된다. 지름이 2 cm인 배관에서 유체의 유속[cm/s]은?
- 50
- 75
- 100
- 125
19. 이상적인 유동층(fluidized bed) 반응기의 조작에 있어서 유속(v)과 반응기 내부 압력강하(△P)와의 관계를 옳게 나타낸 그림은?
20. A→B 반응이 2차 반응일 때, 속도상수를 결정하는 과정에 대한 설명으로 옳은 것은? (단, CA는 A의 농도이며, A의 초기 농도는 CA0이다)
- 반응시간 경과에 따른
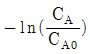 의 변화를 그래프로 나타내면 원점을 지나는 직선으로 표시된다.
의 변화를 그래프로 나타내면 원점을 지나는 직선으로 표시된다. - 반응시간 경과에 따른
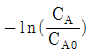 의 변화를 그래프로 나타낼 때, 직선으로 표시되며 직선의 기울기는 속도상수에 해당된다.
의 변화를 그래프로 나타낼 때, 직선으로 표시되며 직선의 기울기는 속도상수에 해당된다. - 반응시간 경과에 따른 1/CA의 변화를 그래프로 나타내면 원점을 지나는 직선으로 표시된다.
- 반응시간 경과에 따른 1/CA의 변화를 그래프로 나타낼 때, 직선으로 표시되며 직선의 기울기는 속도상수에 해당된다.







 그래프를 보면 물질 C의 온도 변화 기울기가 가장 완만하므로 열전도도가 가장 큽니다.
그래프를 보면 물질 C의 온도 변화 기울기가 가장 완만하므로 열전도도가 가장 큽니다.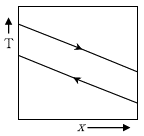
 가 옳은 설명입니다.
가 옳은 설명입니다.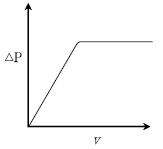
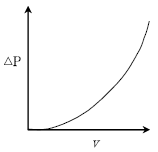
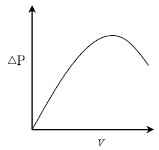
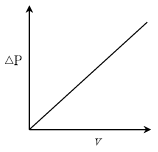
 그래프가 정답입니다.
그래프가 정답입니다.
오답 노트
$N \cdot s^2 \cdot m^{-2}$: 점도의 단위 정의와 일치하지 않는 차원임