1과목: 과목 구분 없음
1. 산-염기 이론에 대한 설명으로 옳은 것은?
- Arrhenius 이론에서 산은 물에 용해되어 H+를 공급하는 수소 함유 화학종이라 정의하며, 산-염기 화학을 수용액으로만 국한하게 된다.
- Brønsted-Lowry 이론에서 산은 전자쌍 받개(acceptor)로, 염기를 전자쌍 주개(donor)로 정의한다.
- Brønsted-Lowry 이론에서 모든 산과 염기는 짝을 갖는데, 강한 산일수록 짝염기는 강하고, 약한 산일수록 짝염기는 약하다.
- Lewis 산은 수소이온 주개(donor)로, 염기를 수소이온 받개(acceptor)로 정의한다.
2. 제올라이트에 대한 설명으로 옳은 것을 모두 고른 것은?
- ㄱ, ㄴ
- ㄱ, ㄴ, ㄷ
- ㄱ, ㄴ, ㄹ
- ㄱ, ㄴ, ㄷ, ㄹ
3. 표준상태에서 석영으로 만들어진 플라스크(flask)에 헬륨가스를 넣었더니 0.2g으로 가득 채울 수 있었다. 그런데 같은 조건에서 미지의 기체는 같은 크기의 플라스크를 채우는데 3.2g이 필요하였다. 다음 중 미지의 기체로 추정되는 물질은?
- N2
- CH4
- SO2
- NH3
4. 다음 여러 가지 인산 중에서 P의 산화수가 다른 것은?
- H3PO4
- H5P3O10
- H6P4O13
- H2PHO3
5. 금속의 화학적 반응성의 세기는 금속원자가 전자를 잃고 이온으로 되려는 이온화 경향과 일치한다. 1족과 2족에 속한 원소들의 일차 이온화 경향의 세기(이온화서열)를 순서대로 옳게 배열한 것은?
- K>Ca>Na>Mg
- K>Na>Ca>Mg
- Na>Mg>K>Ca
- Na>K>Mg>Ca
6. 고순도의 식염을 얻기 위하여 해수를 양이온교환 막과 음이온교환막을 교대로 배열하고 전압을 걸어 나트륨 이온과 염소 이온을 선택적으로 포집 농축한 후, 이를 증발시켜 식염을 제조한다. 이와 같은 방법으로 고순도의 식염을 제조하는 방법은?
- 전기분해(electrolysis)
- 전기투석(electrodialysis)
- 전기응집(electroflocculation)
- 전기영동(electrophoresis)
7. 흑연, 다이아몬드, 탄소나노튜브에 대한 설명으로 옳은 것을 모두 고른 것은?
- ㄱ, ㄴ
- ㄱ, ㄴ, ㄷ
- ㄱ, ㄴ, ㄹ
- ㄴ, ㄷ, ㄹ
8. Wacker법으로 알려진 것으로서 PdCl2 촉매와 CuCl2 조촉매를 사용하고 산화제로서 공기나 산소를 사용한 에틸렌(ethylene)의 산화 반응으로부터 제조되는 주요 생성물은?
- 에틸렌옥시드(ethylene oxide)
- 아세트알데히드(acetaldehyde)
- 에틸렌글리콜(ethylene glycol)
- 아크롤레인(acrolein)
9. 비료에 대한 설명으로 옳지 않은 것은?
- 인산비료에는 소성인비, 과린산석회, 용성인비 등이 있다.
- 중과린산석회는 P2O5를 40~50% 정도 함유한다.
- 복합비료란 N, P2O5, K2O의 세 성분 중에서 2가지 이상을 함유한 비료를 의미한다.
- 질산암모늄(NH4NO3)은 질소의 함유량이 높지만 토양을 산성화 시키는 단점이 있다.
10. 다음 암모니아와 이산화탄소를 반응시켜 요소를 만드는 반응과정에서 반응중간체의 구조를 옳게 나타낸 것은?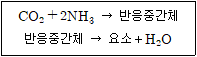
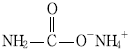
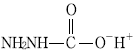
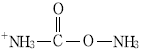
- NH2―O―CH2―O―NH2
11. 다음 중 열역학적으로 가장 안정한 화합물은?
- 사이클로부탄(cyclobutane)
- 사이클로프로판(cyclopropane)
- 사이클로헥산(cyclohexane)
- 사이클로펜탄(cyclopentane)
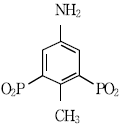
12. 다음 화합물의 명명이 옳지 않은 것은?
13. 다음 반응에서 얻어지는 생성물은?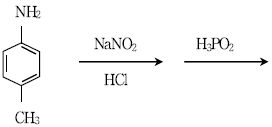
14. 산도(acidity)의 크기를 바르게 배열한 것은?
- H-NH2<H-OH<H-Br<H-F
- H-NH2<H-OH<H-F<H-Br
- H-OH<H-NH2<H-Br<H-F
- H-OH<H-NH2<H-F<H-Br
15. 다음 보기의 탄소양이온(carbocation)의 화학적 안정도가 증가하는 순으로 바르게 배열한 것은?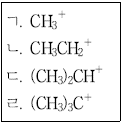
- ㄱ<ㄴ<ㄷ<ㄹ
- ㄹ<ㄷ<ㄴ<ㄱ
- ㄱ<ㄴ<ㄹ<ㄷ
- ㄷ<ㄴ<ㄱ<ㄹ
16. 다음 그림은 4종류의 탄화수소를 구조 및 반응에 따라 분류한 것이다. ㉮-㉯-㉰-㉱의 배열로 옳은 것은?
- 사이클로헥산-벤젠-헥산-헥센
- 벤젠-사이클로헥산-헥센-헥산
- 헥산-헥센-사이클로헥산-벤젠
- 헥산-헥센-벤젠-사이클로헥산
17. 다음 중 Friedel-Crafts acylation에 해당하는 반응은? (주요반응물과 생성물만 표시)
18. 벤젠과 프로필렌을 반응시켜 최종적으로 페놀이 합성되고 아세톤이 부생하는 것은?
- SOHIO법
- Cumene법
- Williamson법
- Monsanto법
19. 고분자 가공방법에 대한 설명으로 옳지 않은 것은?
- 취입성형(blow molding)은 병이나 기타 속이 빈 플라스틱 제품생산에 사용된다.
- 캘린더링(calendering)은 롤러를 이용하여 필름과 시트를 가공하고, 광택을 내기 위해 사용하는 방법이다.
- 이송성형(transfer molding)은 압축성형(compression molding)의 변형된 가공방법으로, 가열하여 용융(연화)된 재료를 사용한다.
- 압출성형(extrusion molding)은 주로 열경화성 플라스틱의 성형에 사용되는 방법이다.
20. A와 B가 서로 다른 모노머(monomer)라고 할 때, 다음 구조를 갖는 공중합체(copolymer)는?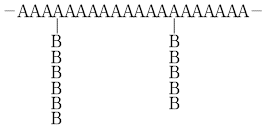
- 블록 공중합체(block copolymer)
- 그라프트 공중합체(graft copolymer)
- 랜덤 공중합체(random copolymer)
- 교대 공중합체(alternating copolymer)






 는 $CO_{2}$의 탄소에 $NH_{2}$ 그룹과 $O^{-}NH_{4}^{+}$ 그룹이 결합된 중간체 구조를 정확히 나타내고 있습니다.
는 $CO_{2}$의 탄소에 $NH_{2}$ 그룹과 $O^{-}NH_{4}^{+}$ 그룹이 결합된 중간체 구조를 정확히 나타내고 있습니다.
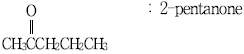
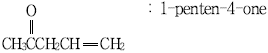
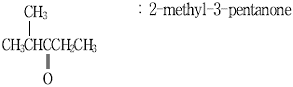
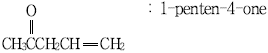 의 경우, 카보닐기($$C=O$$)가 포함된 탄소에 가장 낮은 번호를 부여해야 하므로 4-penten-2-one으로 명명하는 것이 옳습니다. 1-penten-4-one은 번호 부여 원칙에 어긋납니다.
의 경우, 카보닐기($$C=O$$)가 포함된 탄소에 가장 낮은 번호를 부여해야 하므로 4-penten-2-one으로 명명하는 것이 옳습니다. 1-penten-4-one은 번호 부여 원칙에 어긋납니다.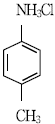
 가 정답입니다.
가 정답입니다.

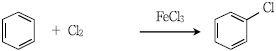
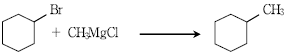
 는 벤젠과 아세틸 클로라이드($CH_{3}COCl$)가 반응하여 아세토페논을 생성하는 전형적인 아실화 반응입니다.
는 벤젠과 아세틸 클로라이드($CH_{3}COCl$)가 반응하여 아세토페논을 생성하는 전형적인 아실화 반응입니다. 를 보면, 주쇄(Main chain)가 모노머 A로 이루어져 있고, 그 가지(Branch) 부분에 모노머 B가 결합된 구조입니다.
를 보면, 주쇄(Main chain)가 모노머 A로 이루어져 있고, 그 가지(Branch) 부분에 모노머 B가 결합된 구조입니다.
오답 노트
전자쌍 받개/주개 정의: Lewis 이론에 해당함
강산의 짝염기: 강한 산일수록 짝염기는 약함
Lewis 산/염기: 산은 전자쌍 받개, 염기는 전자쌍 주개임