1과목: 과목구분없음
1. 그래프는 400K에서 H2, CO2 각 1몰에 대한 PV/RT 값을 압력에 따라 나타낸 것이다. 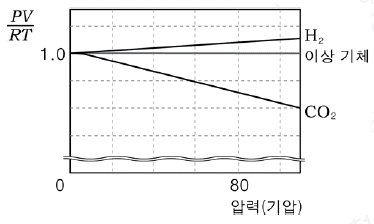
이에 대한 옳은 해석을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
2. 다음은 기체 A2, B2를 강철 용기에 각각 넣은 모습과 두 기체의 화학 반응식을 나타낸 것이다. 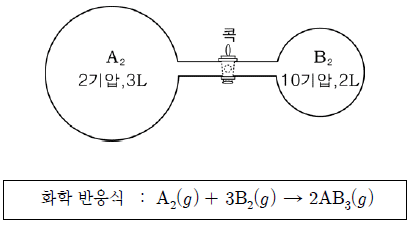
콕을 열어 A2를 모두 반응시켰을 때 B2의 부분압력은? (단, 온도는 일정하며 연결관의 부피는 무시한다.) [3점]
- 0.4기압
- 1.2기압
- 2.4기압
- 2.8기압
- 3.0기압
3. 다음은 기체의 압력에 따른 부피 변화를 알아보기 위한 실험이다. 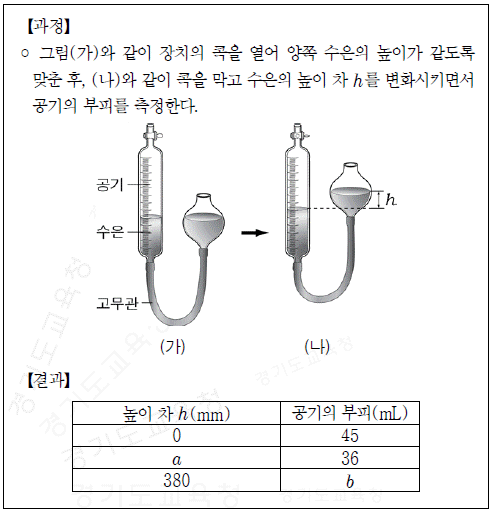
a, b로 알맞은 값을 바르게 짝지은 것은? (단, 대기압은 760mmHg이며 온도는 일정하다.) (순서대로 a, b)
- 95, 18
- 95, 22.5
- 190, 22.5
- 190, 30
- 285, 30
4. 그래프는 일정한 압력에서 같은 질량의 두 기체 A, B의 온도에 따른 부피 변화를 나타낸 것이다. 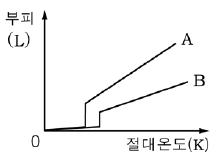
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? (단, A, B는 승화하지 않는다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
5. 다음은 기체의 확산 속도를 비교하기 위한 실험이다. 
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? (단, 온도는 일정하다.)
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
6. 다음은 기체 상수(R)를 구하기 위한 실험 과정이다. 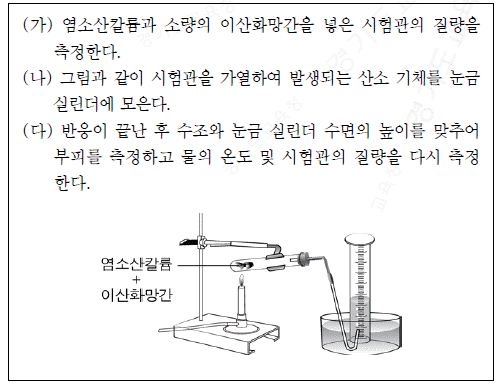
기체 상수(R)를 구하기 위해 추가로 필요한 물리량을 <보기>에서 모두 고른 것은? (단, 물의 온도는 실험실의 온도와 같고, 산소는 이상 기체라고 가정한다.)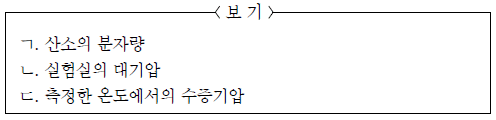
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
7. 그래프 (가)는 온도 T1, T2에서 일정량의 기체 A의 속력에 따른 분자수를, (나)는 온도 T1에서 일정량의 기체 A, B의 속력에 따른 분자수를 나타낸 것이다. 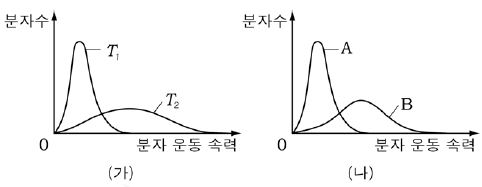
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
8. 그림은 진공인 플라스크에 액체를 넣어 수은의 높이차(h)를 측정하는 모습이다. 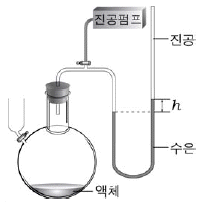
수은의 높이차(h)를 증가시키기 위한 방법으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
9. 그래프는 압력에 따라 물 100g에 녹는 질소와 산소 기체의 몰수를 각각 나타낸 것이다. 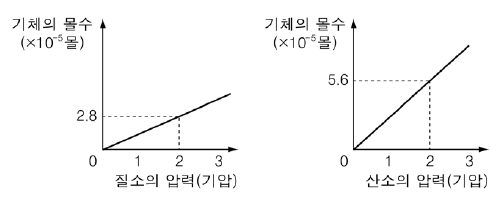
대기압은 1기압이며 공기 속 질소와 산소의 부피비가 4:1일 때, 물 100g에 녹아 있는 질소와 산소의 몰수비는? [3점]
- 1 : 1
- 1 : 2
- 1 : 4
- 2 : 1
- 4 : 1
10. 그래프는 물질 A~C의 온도에 따른 증기 압력 곡선을, 표는 각 물질의 외부 압력에 따른 끓는점을 나타낸 것이다. 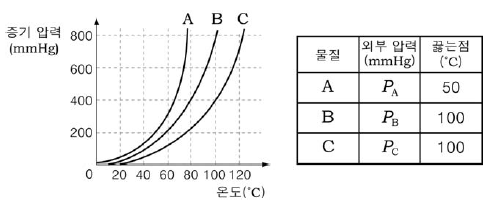
PA, PB, PC의 크기를 바르게 비교한 것은?
- PA > PB > PC
- PB > PA > PC
- PB = PC > PA
- PA > PB = PC
- PB > PC > PA
11. 그림은 잉크 (가)와 (나)를 같은 용매에 의한 종이 크로마토그래피를 이용하여 각 색소 성분으로 분리한 모습을 나타낸 것이다. 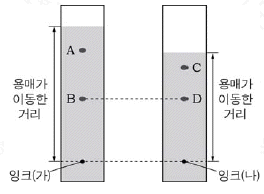
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
12. 다음은 석영을 이용하여 석영 유리를 만드는 과정과 석영 유리를 녹여 액체로 만드는 과정을 나타낸 것이다. 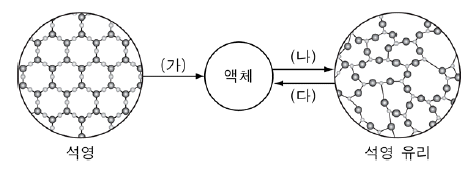
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
13. 다음은 질산나트륨의 물에 대한 용해 실험과 용해도 곡선이다. 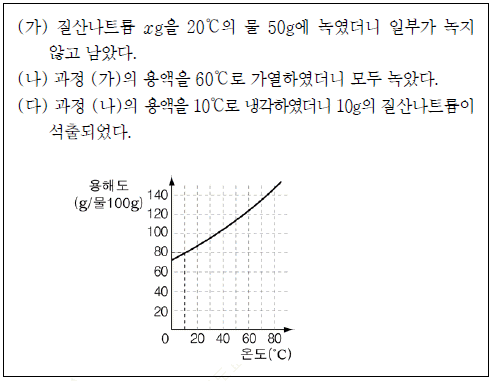
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? (단, 물은 증발하지 않는다고 가정한다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
14. 그림 (가)는 수은을 가득 채운 유리관을 수조에 거꾸로 세운 후 유리관 안에 0℃의 얼음을 넣은 모습을, (나)는 그 얼음이 녹아 20℃의 물이 되었을 때의 모습을, (다)는 물의 상평형을 나타낸 것이다. 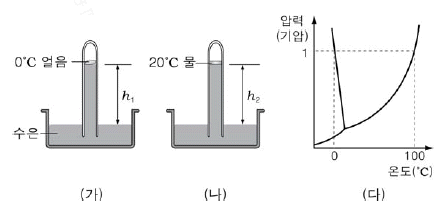
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? (단, 대기압은 760mmHg이고 물과 얼음의 질량은 무시한다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
15. 그래프는 물과 비휘발성 용질이 녹아 있는 수용액의 증기 압력을 나타낸 것이다. 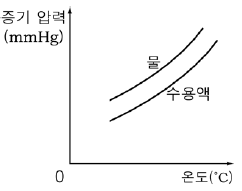
이와 관련된 현상을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
16. 크기가 같은 세 개의 플라스크에 같은 부피의 1m 소금물, 증류수, 1m 설탕물을 각각 넣었더니 그림과 같이 수은 기둥의 높이 차가 생겼다. 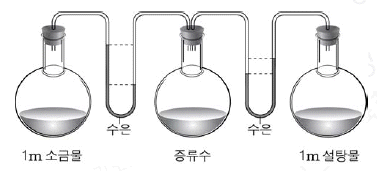
이에 대한 옳은 설명을 <보기>에서 모두 고른 것은? (단, 온도는 일정하다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
17. 표는 일정한 온도에서 10% HA 수용액과 10% BOH 수용액의 질량을 다르게 하여 중화 반응시켰을 때 생성되는 H2O의 질량을 나타낸 것이다. 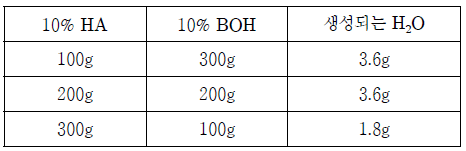
HA와 BOH의 화학식량의 비는? [3점]
- 1 : 1
- 1 : 2
- 1 : 3
- 2 : 1
- 3 : 1
18. 20% 수산화나트륨 수용액을 1몰 농도(M)로 만드는 방법으로 옳은 것은? (단, 수산화나트륨은 화학식량이 40이고 20% 수용액의 밀도는 1.2g/mL이다.)
- 20% 수용액 20g에 증류수를 가해 100g이 되게 한다.
- 20% 수용액 20g에 증류수를 가해 104g이 되게 한다.
- 20% 수용액 20g에 증류수를 가해 100mL가 되게 한다.
- 20% 수용액 20mL에 증류수를 가해 100mL가 되게 한다.
- 20% 수용액 20mL에 증류수를 가해 104mL가 되게 한다.
19. 이 실험에 대한 옳은 설명을 <보기>에서 모두 고른 것은?(19번 공통지문 문제)
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ






$H_2$는 분자 크기가 매우 작아 인력보다 반발력의 영향이 커서 $\frac{PV}{RT}$ 값이 1보다 큽니다.
$CO_2$는 분자 간 인력이 강해 $\frac{PV}{RT}$ 값이 1보다 작아집니다.
따라서 압력이 증가할수록 $\frac{PV}{RT}$ 값이 1에서 더 멀어지는 경향을 보입니다.