1과목: 과목구분없음
1. 그림은 상온에서 물이 들어 있는 비커를 용기 속에 넣고 밀폐한 후, 수증기로 포화된 상태를 나타낸 것이다. 
위의 상태보다 물의 증기압력을 높일 수 있는 방법을 옳게 말한 학생만을 <보기>에서 있는 대로 고른 것은?
- 철수
- 영희
- 철수, 민수
- 영희, 민수
- 철수, 영희, 민수
2. 그림은 수소(H2)와 요오드(I2)가 반응할 때 에너지 관계를 나타낸 것이다. 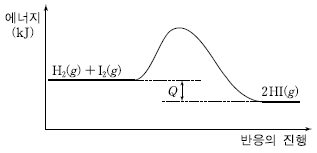
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 정반응의 활성화에너지는 83 kJ 이며, Q는 반응열이다.)
- ㄱ
- ㄷ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
3. 다음은 중심 원자가 2 주기 원소인 분자의 결합각을 세 영역 A~C로 나타낸 것과 세 가지 화합물의 분자식이다. 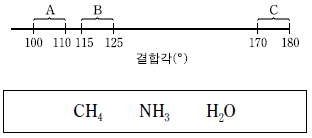
위 화합물 중에서 결합각이 A~C에 속하는 화합물의 수로 옳은 것은? (순서대로 A, B, C) [3점]
- 1, 1, 1
- 1, 2, 0
- 2, 0, 1
- 2, 1, 0
- 3, 0, 0
4. 표는 세 가지 물질의 녹는점이며, 물질 (가)~(다)는 각각 NaF, NaBr, MgO 중의 하나이다. 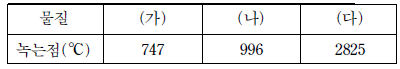
물질 (가)~(다)로 옳은 것은? (순서대로 가, 나, 다)
- NaF, NaBr, MgO
- NaF, MgO, NaBr
- NaBr, NaF, MgO
- NaBr, MgO, NaF
- MgO, NaF, NaBr
5. 다음은 프로판(C3H8)이 연소될 때의 화학반응식과 자료이다. 
발생한 열량의 비(Q1 : Q2)로 옳은 것은? (단, a~c는 화학 반응식의 계수이다.)
- 5 : 1
- 4 : 1
- 1 : 1
- 1 : 4
- 1 : 5
6. 그래프는 압력이 P1 과 P2일 때 물에 대한 질소의 용해도를 온도에 따라 나타낸 것이다. 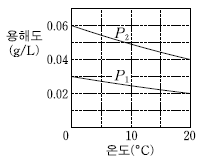
그림 (가)~(다)는 온도와 압력이 각각 다른 조건에서 물 1L에 질소가 포화되어 있는 수용액을 나타낸 것이다. 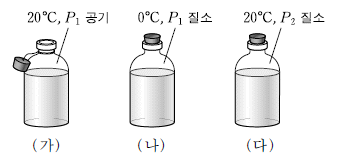
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 공기 중에서 질소의 몰분율은 0.8 이다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
7. 다음은 HBr가 생성되는 열화학반응식이다. 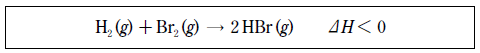
그림은 H2, Br2, HBr의 분자 내 핵간 거리에 따른 에너지를 모식적으로 나타낸 것이다. 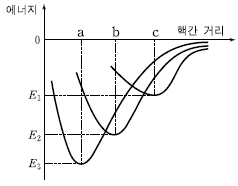
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
8. 표는 세 가지 원소의 1 차 이온화에너지이고, 원소 (가)~(다)는 각각 Li, F, Na 중의 하나이다. 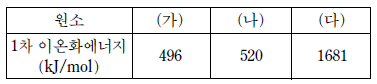
(가)~(다)를 비교하여 설명한 것으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
9. 그림은 용매 A의 냉각 곡선과 용질 x, y 가 A에 각각 녹아 있는 용액의 냉각 곡선을 나타낸 것이다. 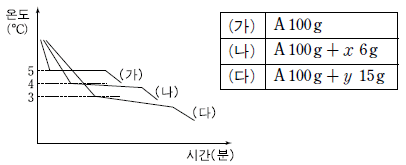
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, A, x, y 는 모두 비휘발성, 비전해질이고 서로 반응하지 않는다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
10. 그림은 할로겐 원소(X)의 전기음성도에 따라 할로겐(X2)과 할로겐화수소 화합물(HX)의 끓는점을 나타낸 것이다. 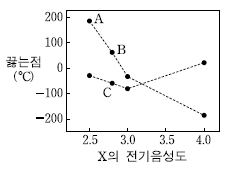
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
11. 그림 (가)는 25℃에서 눈금 실린더에 산소 기체를 포집하는 실험 장치이고, (나)는 산소가 포집된 후의 모습이다. 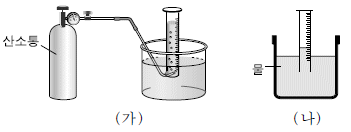
포집된 산소 기체에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
12. 농도가 48.0%, 밀도 1.5g/mL인 어떤 산 HA 수용액이 있다. 이 수용액 1.0 L 에 물을 넣어 처음 몰랄농도의 이 되도록 희석하려고 한다. 이 때 필요한 물의 양은? [3점]
- 480 g
- 520 g
- 720 g
- 780 g
- 1000 g
13. 그림 (가)는 보어의 수소 원자 모형에서 에너지 준위를, (나)는 수소 방전관에서 얻은 가시광선 영역의 선 스펙트럼을 모식적으로 나타낸 것이다. 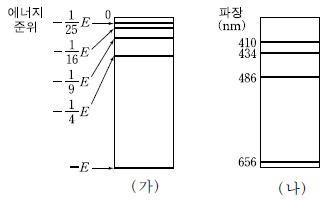
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, E=1312 kJ 이다.) [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
14. 그림은 어떤 기체 1 몰의 PV/RT 값을 압력에 따라 나타낸 것이다. 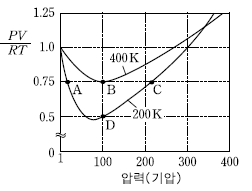
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
15. 그림은 25℃에서 어떤 산 HA 50 mL를 1.0M NaOH 수용액으로 적정한 중화 적정 곡선이다. 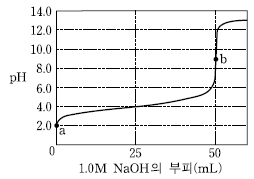
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
16. 다음은 아황산(H2SO3)과 요오드(I2)의 산화·환원반응식이다. 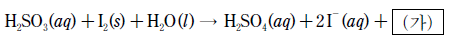
이 반응식에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
17. 그림은 산성 수용액에서 백금을 전극으로 하는 전기분해 장치이다. 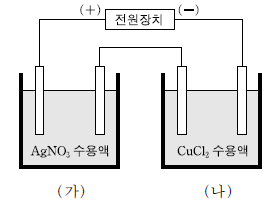
위 장치에 일정한 전기량을 통해 주었더니 (가)에서 Ag 10.8g이 석출되었다. 이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, Ag 과 Cu 의 원자량은 각각 108.0, 64.0 이다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
18. 다음은 어떤 열화학반응식이다. 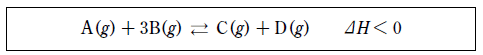
그림은 위 반응에서 부피 변화와 온도 변화에 따른 평형 이동을 모식적으로 나타낸 것이다. 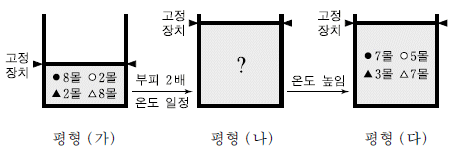
평형 (가)~(다)에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 평형 (가)에서 혼합 기체의 부피는 1L이다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
19. 다음은 25℃에서 1.0 M 산 HA와 1.0 M 염기 B 의 이온화 반응식과 이온화상수이다. 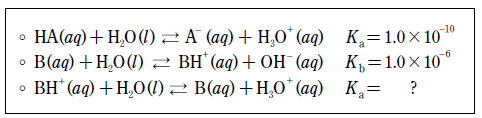
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 25 ℃에서 물의 이온곱상수 Kw=1.0 × 10-14 이다.)
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
20. 그림은 밀폐 용기에서 기체 X가 기체 Y로 되는 어떤 반응에서 시간에 따른 기체 X의 농도[X]를 역수로 나타낸 것이다. (가)와 (나)는 서로 다른 반응 조건에서 측정한 결과이다. 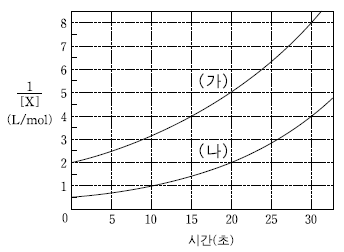
(가)와 (나)에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 촉매는 사용하지 않았다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ






온도가 상승하면 분자들의 평균 운동 에너지가 증가하여 액체 표면을 탈출하는 분자 수가 늘어나므로 증기압이 높아집니다.
오답 노트
물을 덜어내야 해: 증기압은 농도나 양에 무관함
더 큰 밀폐 용기를 사용하면 돼: 증기압은 용기의 부피와 무관함