1과목: 과목구분없음
1. 그림은 염화나트륨(NaCl) 결정을 가열하여 용융시킨 것을 나타낸 것이다. 
두 상태를 비교하였을 때 변하는 것을 <보기>에서 고른 것은?
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄴ, ㄹ
- ㄷ, ㄹ
2. 그림은 물질을 이루는 입자를 표시한 것이다. 
a~c 에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, Z 는 임의의 원소 기호이다.) [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
3. 그림은 수소 원자의 1 s, 2 s 오비탈의 모습과 각 오비탈에서 전자가 발견될 확률을 핵으로부터의 거리에 따라 나타낸 것이다. 
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
4. 그림은 산소(O2)의 물에 대한 용해도를 압력과 온도에 따라 나타낸 것이다. 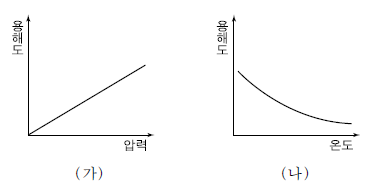
영희가 관찰한 <보기>의 여러 현상 중에서 (가)와 (나)로 가장 잘 설명할 수 있는 것은? (순서대로 가, 나)
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄱ
- ㄴ, ㄷ
- ㄷ, ㄱ
5. 고체는 5 가지 종류로 구분할 수 있다. 고체를 몇 가지 기준에 따라 다음과 같이 구분하였을 때, A~E에 대한 설명으로 옳은 것은? [3점]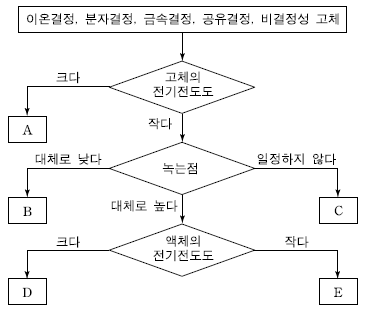
- A는 이온 사이의 정전기적 인력에 의해 결합되어 있다.
- B는 기체가 되어도 원자간 결합이 유지된다.
- C는 구성 입자 사이의 결합력이 모두 같다.
- D는 연성과 전성이 있다.
- E는 쉽게 승화한다.
6. 철수는 다음에 제시된 자료를 참고하여 주기율표를 채우려고 한다. 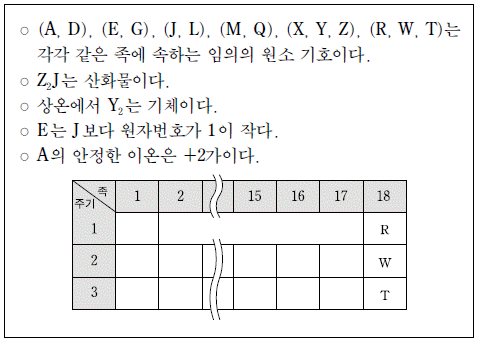
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
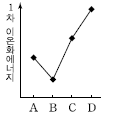
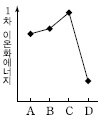
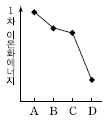
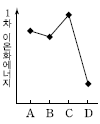
7. 그림은 2~3 주기 임의의 중성 원자 A~D의 전자 배치를 나타낸 것이다. 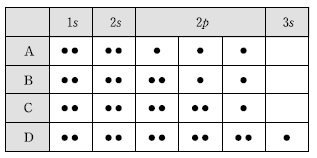
A~D의 1차 이온화에너지를 비교한 것으로 옳은 것은?
8. 다음은 세 가지 분자의 구조식이다. 이에 대한 설명으로 옳지 않은 것은? [3점]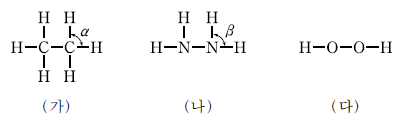
- 분자의 극성이 가장 작은 것은 (가)이다.
- (나)의 끓는점은 (가)보다 높다.
- 비공유전자쌍의 수는 (다)가 가장 많다.
- (다)의 분자 모양은 선형 구조이다.
- 분자 모양에서 결합각은 α가 β보다 크다.
9. 그림은 14족 원소 A의 수소화합물(AH4)에서 A-H 결합에너지와 끓는점을 나타낸 것이다. 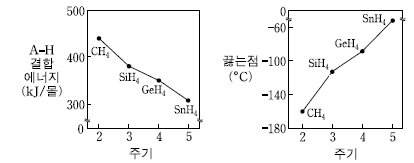
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
10. 표는 어떤 수소(H2) 시료와 산소(O2) 시료에서 동위원소의 존재 비율을 나타낸 것이다. 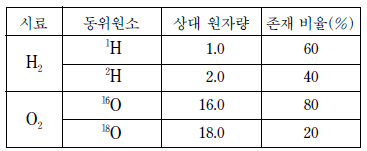
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
11. 표는 일정한 온도에서 기체 A~C가 들어 있는 용기의 질량과 압력을 나타낸 것이다. 
기체 A~C에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 세 용기는 동일하다.)
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
12. 철수는 2.5M 탄산수소칼륨(KHCO3) 수용액 200mL를 희석시켜 1M 수용액을 만들려고 하였으나 실수로 물을 더 넣어 600mL가 되었다. 이 수용액을 1M 수용액으로 만들기 위한 방법으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, KHCO3 의 화학식량은 100 이며, 온도 변화는 없다.) [3점] 
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
13. 그림 (가)는 수소(H2)와 헬륨(He)이 들어 있는 실린더가 피스톤으로 구분된 상태를, (나)는 같은 온도에서 메탄(CH4)을 더 넣었을 때 피스톤이 이동한 모습을 나타낸 것이다. 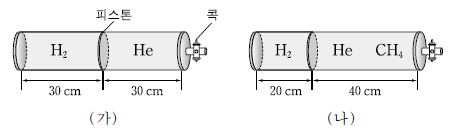
(나)에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, H, He, C의 원자량은 각각 1, 4, 12 이며, 피스톤의 마찰은 무시한다.)
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
14. 그림은 25℃에서 기체 A와 B를 여러 비율로 혼합하였을 때, 각 기체의 물에 대한 용해도(몰/L)를 부분압력에 따라 나타낸 것이다. 
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, B의 분자량은 A의 2 배이다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
15. 2 주기 원소 A~D는 25℃, 1 기압에서 기체로 존재한다. 그림은 A~D가 각각 이원자분자를 형성한다고 가정하였을 때, 원자핵간 거리에 따른 에너지를 대략적으로 나타낸 것이다. 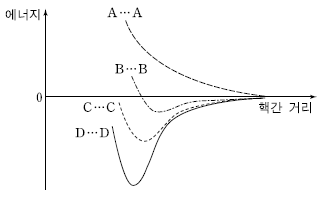
A~D에 대한 설명으로 옳지 않은 것은? (단, A~D는 임의의 원소 기호이다.) [3점]
- A는 안정한 이원자분자를 형성하지 않는다.
- 1 차 이온화에너지가 가장 큰 것은 A이다.
- 결합에너지가 가장 큰 것은 D이다.
- 결합길이가 가장 긴 것은 B이다.
- B의 원자반지름은 C보다 크다.
16. 다음에서 a~e를 모두 더한 값과 가장 가까운 것은?
- 1
- 2
- 3
- 4
- 5
17. 그림은 27℃에서 산소(O2)와 포도당 (C6H12O6)이 들어 있는 0.82 L 크기의 용기를 나타낸 것이다. 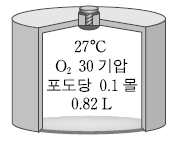
포도당을 완전연소시킨 후, 용기를 27℃로 냉각시켰을 때에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 포도당의 부피, 생성된 물의 부피와 증기압력은 무시하고, 기체상수 R=0.082 기압·L/몰·K이다.) [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
18. 그림은 –100℃, 1 기압에서 고체인 물질 A 와 B 를 단위 시간당 일정한 열량으로 가열 하여 모두 기체로 변할 때까지 시간에 따른 온도 변화를 나타낸 것이다. 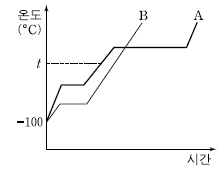
A 와 B 에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
19. 그림 (가)~(다)는 물이 담긴 3L의 용기에 기체 A를 넣은 것을, 표는 온도 T1, T2 에서 물의 증기압력을 나타낸 것이다. 
충분한 시간이 지난 후, 용기에 들어 있는 혼합 기체에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, A의 용해도와 물의 부피 변화는 무시한다.)
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
20. 그림 (가)는 양쪽 플라스크에 동일한 질량의 순수한 액체 A와 B가 각각 들어 있는 모습을, (나)는 양쪽에 동일한 질량의 물질 C를 각각 녹였을 때의 모습을 나타낸 것이다. 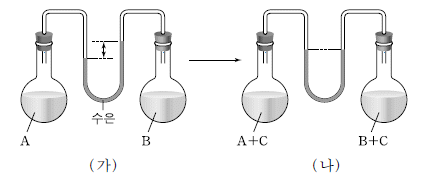
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, C는 비휘발성, 비전해질이고, 용액은 라울의 법칙을 따르며, 온도는 일정하다.) [3점]
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ







 가 정답입니다.
가 정답입니다.
몰수는 B가 A의 2배이므로 몰수는 B > A가 맞습니다.
용기 질량이 동일할 때 기체 질량은 (용기+기체) 질량에서 용기 질량을 뺀 값입니다. C는 용기 2개 분량의 질량($516 = 258 \times 2$)을 가지므로, 기체 C의 질량은 기체 A의 질량과 같습니다. 그런데 압력은 C가 A의 2배이므로 몰수 또한 C가 A의 2배입니다. 질량이 같은데 몰수가 2배라는 것은 분자량이 A의 절반이라는 뜻이므로 분자량은 A > C가 되어 분자량은 C > A는 틀린 설명입니다.
평균 운동 에너지는 오직 절대 온도에만 비례합니다. 세 기체의 온도가 일정하므로 평균 운동 에너지는 모두 같습니다.
오답 노트
분자량은 C > A: 실제로는 A > C임
평균운동에너지는 C > B: 온도가 같으므로 동일함