1과목: 과목구분없음
1. 다음은 어떤 물질 X의 물리적 성질을 알아보기 위한 실험이다. 
다음 중 X에 해당하는 것으로 가장 적절한 것은?
- 흑연
- 구리
- 염화칼슘
- 다이아몬드
- 드라이아이스
2. 그림과 같이 일정한 부피의 강철 용기에 헬륨(He)을 넣고 온도를 올렸다. 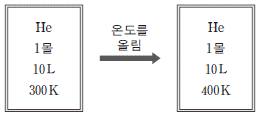
온도를 올린 후, 용기 내에서 증가한 것만을 <보기>에서 있는 대로 고른 것은?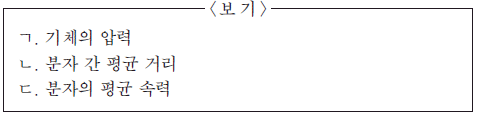
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
3. 표는 강철 용기에서 A(g) → B(g) + C(g)의 반응이 일어날 때, 반응 시간에 따른 각 기체 A~C 의 부분 압력을 일부 나타낸 것이다. 이 반응은 A에 대한 1 차 반응이다. 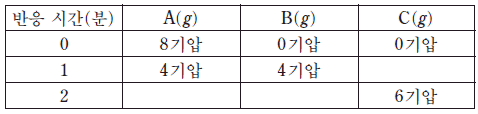
반응 시간이 2 분일 때, 강철 용기 내부에 존재하는 혼합 기체의 전체 압력은? (단, 온도는 일정하다.) [3점]
- 14 기압
- 16 기압
- 18 기압
- 20 기압
- 22 기압
4. 그래프는 온도 T1 과 T2 에서 기체 A의 부분 압력에 따른 물에 대한 용해도를 나타낸 것이다. 그림 (가), (나)는 기체 A의 부분 압력과 온도가 각각 다른 조건에서 물 1 L에 기체 A 가 포화되어 있는 수용액을 나타낸 것이다. 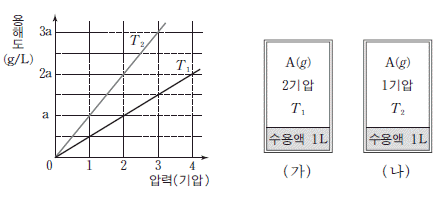
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 기체 A는 헨리의 법칙을 따르며, A의 용해에 따른 수용액의 부피 변화는 없다.)
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
5. 그림은 보어의 수소 원자 모형에서 4 가지 전자 전이 A~D를 나타낸 것이다. 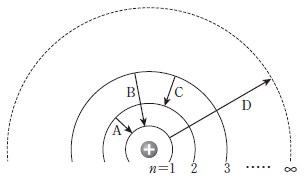
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 수소 원자의 에너지 준위  이다.) [3점]
이다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
6. 표는 25℃에서 물에 잘 녹는 4 가지 염과 그 수용액의 액성을 나타낸 것이다. (가)~(다)는 산성 또는 염기성이다. 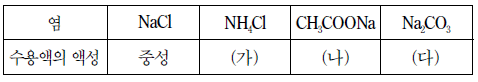
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
7. 그림은 임의의 원소 A~D의 이온 반지름을 나타낸 것이다. A~D는 각각 O, F, Na, Mg 중 하나이다. 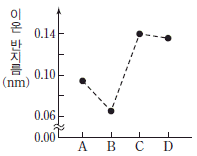
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, A~D 이온의 전자 배치는 Ne의 바닥 상태와 같다.)
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
8. 그림은 1% 포도당 수용액의 농도를 몰농도와 몰랄 농도로 환산하는 과정을 나타낸 것이다. 포도당의 분자량은 M이고, 포도당 수용액의 밀도는 d g/mL이다. 
A~C로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
9. 표는 1 기압에서 물 100g에 비휘발성이고 비전해질인 물질 A와 B를 각각 9.0 g 과 6.0 g 을 녹인 수용액의 어는점과 끓는점을 나타낸 것이다. 
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 물의 몰랄 내림 상수 Kƒ 는 1.86℃/m이고, 몰랄 오름 상수 Kb는 0.52℃/m이다.)
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
10. 그림은 임의의 중성 원자 A~C의 전자 배치를 나타낸 것이다. 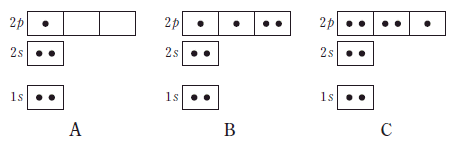
A~C에 대한 설명으로 옳은 것은? [3점]
- B는 들뜬 상태이다.
- B의 원자가 전자 수는 4 개이다.
- C2 에는 이중 결합이 있다.
- 제1 이온화 에너지는 A가 C보다 크다.
- AC3 에서 A는 옥텟 규칙을 만족하지 않는다.
11. 그림은 물과 관련된 반응의 엔탈피(H) 변화를 나타낸 것이다. 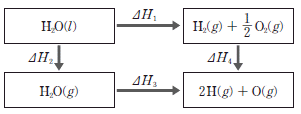
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
12. 그림 (가)는 고정 장치가 있는 진공 실린더에 어떤 물질 X(l)를 넣은 후 압력 P1, 온도 T1 에서 액체와 기체가 평형을 이루고 있는 것을, (나)는 이 물질의 상평형 그림을 나타낸 것이다. 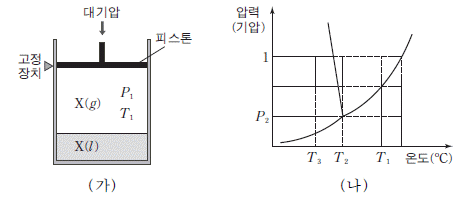
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 대기압은 1 기압이고, 피스톤의 질량과 마찰은 무시한다.)
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
13. 그림은 25℃ 에서 콕이 닫힌 진공 상태의 두 용기 A, B 에 액체 X와 Y를 각각 넣고 평형에 도달한 상태를 나타낸 것이다. 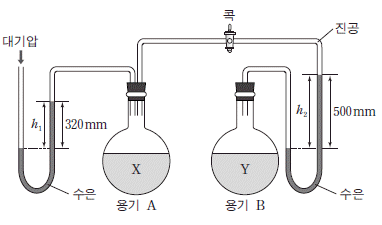
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 대기압은 760mmHg이다.) [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
14. 다음은 식초 속의 아세트산(CH3COOH)의 몰농도를 결정하기 위한 실험이다. 
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 실험에서 산으로 작용하는 물질은 CH3COOH만 있으며, 종말점은 중화점으로 간주한다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
15. 다음은 기체 A와 B가 반응하여 기체 C가 생성되는 열화학 반응식이다. 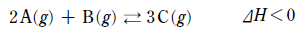
그림 (가)는 고정 장치가 있는 실린더에서 주어진 반응이 평형을 이루고 있는 것을, (나)는 (가)의 온도를 올려 새로운 평형에 도달한 것을 나타낸 것이다. 그림 (다)는 (나)의 고정 장치를 풀고 피스톤을 밀어 또 다른 평형에 있는 것을 나타낸 것이다. 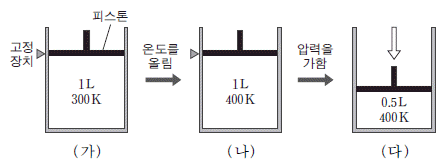
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
16. 그림은 4 가지 분자를 3 가지 분류 기준 (가)~(다)에 따라 분류한 것이다. 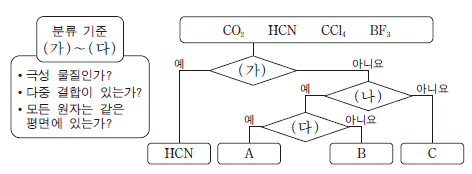
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, A~C는 서로 다른 분자이다.) [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
17. 다음은 25℃의 물에서 어떤 산 HA와 염기 B의 이온화 반응식과 이온화 상수를 나타낸 것이다. 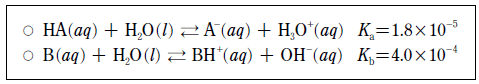
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 25℃에서 물의 이온곱 상수(Kw)는 1.0×10-14이다.)
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
18. 다음은 수용액에서 일어나는 어떤 산화∙환원 반응의 알짜 이온 반응식이며, a~e 는 이온 반응식의 계수이다. 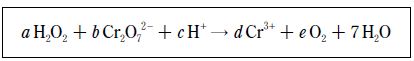
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
19. 그림은 금속 X의 염인 XSO4 수용액과 금속 Y의 염인 YCl 수용액을 전기분해하는 장치를, 표는 전기분해가 진행되는 동안 각 전극에서 관찰된 결과를 나타낸 것이다. X, Y는 임의의 금속 원소이다. 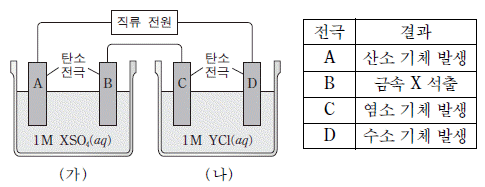
전기분해 과정에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
20. 다음은 기체 A와 B가 반응하여 기체 C가 생성되는 반응식이다. 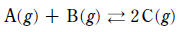
그림 (가)는 1L 강철 용기에 같은 몰수의 A와 B만을 넣은 초기 상태를, (나)는 충분한 시간 경과 후 평형에 도달한 상태를 나타낸 것이다. 이어서 온도를 올렸을 때 새로운 평형 상태인 (다)가 되었다. 평형 상수는 (다)가 (나)의 4 배이다. 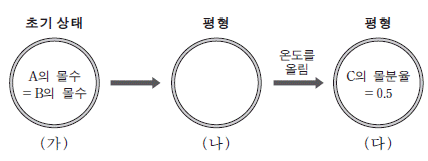
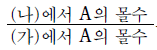 는? [3점]
는? [3점]
- 1/3
- 2/5
- 1/2
- 2/3
- 3/4






염화칼슘은 대표적인 이온 결합 물질로, 고체일 때는 이온들이 강하게 결합되어 이동할 수 없지만 액체 상태가 되면 이온들이 자유롭게 이동하여 전류를 흐르게 합니다.
오답 노트
흑연, 구리: 고체 상태에서도 전기 전도성이 있음
다이아몬드, 드라이아이스: 액체 상태에서도 전기 전도성이 없음