1과목: 화공열역학
1. 순환법칙 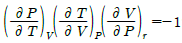 에서 얻을 수 있는 최종식은? (단, β는 부피 팽창률(Volume expansivity), k는 등온압축률(Isothermal compressibility)이다.
에서 얻을 수 있는 최종식은? (단, β는 부피 팽창률(Volume expansivity), k는 등온압축률(Isothermal compressibility)이다.
2. 그림과 같이 상태 A로부터 상태 C로 변화하는데 A → B → C의 경로로 변하였다. 경로 B → C과정에 해당하는 것은?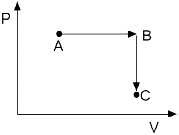
- 등온과정
- 정압과정
- 정용과정
- 단열과정
3. 온도의 함수로 순수물질의 증기압을 계산하는 다음 식의 이름은? (단, P, T는 각각 온도와 압력을 타 내며, A, B, C는 순수물질 고유상수이다.)
- 돌턴(Dalton)식
- 뉴턴(Newton)식
- 라울(Raoult)식
- 안토인(Antoine)식
4. 다음과 같은 반응이 1105K에서 일어나며, 반응 평형 상수 K는 1.0이다. 초기에 1몰의 일산화탄소와 2몰의 물로 반응이 진행된다면 최종 반응좌표(몰)은얼마인가? (단, 혼합물은 이상기체로 본다.)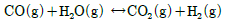
- 0.333
- 0.500
- 0.667
- 0.700
5. 10atm, 260℃의 과열증기(엔트로피 : 1.66kcal/kgㆍK)가 단열가역적으로 2atm 까지 팽창한다면 수증기의 질량 %는 얼마인가? (단, 2atm일 때 포화증기와 포화액체의 엔트로피는 각각 1.70, 0.36kcal/kgㆍK이다.)
- 97
- 94
- 89.5
- 88.7
6. 실제기체(real gas)가 이상기체와 가장 가까워질 경우의 상태는?
- 고압, 저온
- 저압, 고온
- 고압, 고온
- 저압, 저온
7. 이상기체를 등온 하에서 압력을 증가시키면 엔탈피는?
- 증가한다.
- 감소한다.
- 일정하다.
- 초기에 증가하다 점차로 감소한다.
8. 500K와 10bar의 조건에 있는 메탄가스가 1bar가 될 때까지 가역단열팽창 된다. 이 조건에서 메탄이 이상 기체라고 가정하면 마지막의 온도 T2를 초기온도 T1으로 옳게 나타낸 것은?
9. 어떤 화학반응에 대한 △S°는 △ H°=△G°인 온도에서 어떤 값을 갖겠는가? (단, △S° : 표준엔트로피 변화, △H° : 표준 엔탈피 변화, △ G° : 표준 깁스에너지 변화, T : 전대온도 이다.)
- △ S° > 0
- △ S° < 0
- △ S° = 0
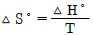
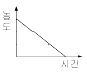
10. 액체의 증발잠열을 계산하는 식과 관계없는 식은?
- Clapeyron식
- Watson correlation식
- Riedel식
- Gibbs-Duhem식
11. 압축비 4.5인 오토 사이클(Otto cycle)에 있어서 압축비가 7.5로 되었다고 하면 열효율은 몇 배가 되겠는가? (단, 작동유체는 이상기체이며, 열용량의 비 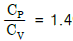 이다.)
이다.)
- 1.22
- 1.96
- 2.86
- 3.31
12. 다음 중 열역학 제2법칙의 수학적인 표현으로 올바른 것은?

- ΔStotal≥ 0
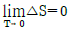
- dU=dQ-dW
13. 반응의 평형상수 K에 관한 내용 중 틀린 것은? (단, ai, ui는 각각 i성분의 활동도와 양론수이며, △G0 준 깁스(Gibbs)자유에너지 변화이다.)
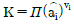
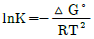
- K는 온도에 의존하는 함수이다.
- K는 무차원이다.
14. 순수한 성분이 액체에서 기체로 변화하는 상의 전이에 대한 설명 중 옳지 않은 것은?
- 1몰당 깁스(Gibbs) 자유에너지 G는 불연속이다.
- 1몰당 엔트로피 S는 불연속이다.
- 1몰당 부피 V는 불연속이다.
- 액체는 일정 온도에서의 감압 또는 일정 압력에서의 가열에 의해 기체로 상 전이가 일어난다.
15. PVn=c일경우 폴리트로픽 지수 n의 값에 따라 변화하는 과정으로 틀린 것은? (단, c는 상수이고, 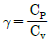 이다.)
이다.)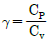
- n = 0, P = c, 등압변화
- n = 1, PV = c, 등온변화
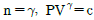 , 등압변화
, 등압변화- n = ∞, V = c, 정용변화
16. 다음 등온선 그래프에서 빗금 친 부분의 면적은 무엇을 나타내는가?(참고, 세로축이 (aV/aT)p 입니다)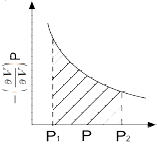
- Ω
- W
- △S
- △H
17. 100℃에서 물의 엔트로피 값은 0.3kcal/kgㆍK이다. 증발열이 539.1kcal/kg이라면 100℃에서의 수증기의 엔트로피 값은 약 몇 kcal/kgㆍK인가?
- 5.69
- 2.85
- 1.74
- 0.87
18. 상평형에서 계의 성질이 최대가 되는 것은?
- 엔탈피
- 엔트로피
- 내부 에너지
- 깁스(Gibbs) 자유 에너지
19. 단일 상계에서 열역학적 특성 값들의 관계에서 틀린것은?
20. 주어진 온도와 압력에서 화학반응의 평형조건은?
- △S = 0
- △A = 0
- △H = 0
- △G = 0
2과목: 단위조작 및 화학공업양론
21. 30℃, 750mmHg에서 percentage humidity(비교습도%H)는 20%이고, 30℃에서 포화증기압은 31.8mmHg이다. 공기 중의 실제 증기압은?
- 6.58mmHg
- 7.48mmHg
- 8.38mmHg
- 9.29mmHg
22. 다음 중 습구온도계 하단부의 구를 젖은 솜으로 싸는 이유로서 가장 거리가 먼 것은?
- 물을 공기 중으로 기화시키기 위하여
- 주위 공기의 건조 상태를 예측하기 위하여
- 잠열이 공기온도에 미치는 영향을 예측하기 위하여
- 공기건조도가 기화속도에 무관하게 됨을 예측하기 위하여
23. CO2 25vol%와 NH375vol%의 기체 혼합물 중 NH3의 일부가 산에 흡수되어 제거된다. 이 흡수탑을 떠나는 기체가 37.5vol%의 NH3을 가질 때 처음에 들어있던 NH3부피의 몇 %가 제거 되었는가? (단, CO2의 양은 변하지 않으며 산 용액은 증발하지 않는 다고 가정한다.).
- 15%
- 20%
- 62.5%
- 80%
24. 포도당(C6H12O6) 4.5g이 녹아 있는 용액 1L와 소금물을 반투막을 사이에 두고 방치해 두었더니 두 용액의 농도 변화가 일어나지 않았다. 이 농도에서 소금은 완전히 전리한다고 보고 1L 중에는 몇 g의 소금이 녹아 있는가?
- 0.0731g
- 0.146g
- 0.731g
- 1.462g
25. 10mol의 N2와 32 mol의 H2를 515℃, 300 atm에서 반응시킨 결과 평형에서 전체 가스는 38 mol이 되었다. 생성된 NH3의 몰수는?
- 1.5 mol
- 2 mol
- 4 mol
- 6.5 mol
26. 시량변수와 시강변수에 대한 설명으로 옳은 것은?
- 시량변수에는 체적, 온도, 비체적이 있다.
- 시강변수에는 온도, 질량, 밀도가 있다.
- 계의 크기에 무관한 변수가 시강변수이다.
- 시강변수는 계의 상태를 규정할 수 없다.
27. 다음 단위환산 관계 중 틀린 것은?
- 1.0g/cm3=1000kg/m3
- 0.2386 J = 0.057 cal
- 0.4536 kgf = 9.80665 N
- 1.013 bar = 101.3 kPa
28. 몰 증발잠열을 구할 수 있는 방법 중 2가지 물질의 증기압을 동일 온도에서 비교하여 대수좌표에 나타낸 것은?
- Duhring 도표
- Othmer 도표
- Cox 선도
- Watson 도표
29. 10ppm SO2을 %로 나타내면?
- 0.0001%
- 0.001%
- 0.01%
- 0.1%
30. 그림과 같은 순환조작에서 A, B, C, D, E의 각 흐름의 양을 기호로 나타내었다. 이들의 관계 중 옳은 것은? (단, 이 조작은 정상상태에서 진행되고 있다.)
- A = B
- A + C = D + B
- D = E + C
- B = A = C
31. 70℃, 1atm에서 에탄올과 메탄올의 혼합물이 액상과 기상의 평형을 이루고 있을 때 액상의 메탄올의 몰분율은? (단, 이 혼합물은 이상용액으로 가정하며, 70℃에서 순수한 에탄올과 메탄올의 증기압은 각각 543mmHg, 857mmHg이다.
- 0.12
- 0.31
- 0.69
- 0.75
32. 젖은 고체 10kg을 완전히 건조하였더니 9.2kg이 되었다. 처음 재료의 수분은 몇 %인가?
- 0.08%
- 0.8%
- 8%
- 10%
33. 기체 흡수에 관한 설명으로 옳지 않은 것은?
- 기체 속도가 일정하고 액 유속이 줄어들면 조작선의 기울기는 감소한다.
- 액/기(L/V)비가 작으면 조작선과 평형선의 거리가 줄어서 흡수탑의 길이가 길어진다.
- 일반적으로 경제적인 조업을 위해서는 조작선과 평형선이 대략 평행이 되어야 한다.
- 항류 흡수탑의 경우에는 한계 기액비가 흡수탑의 경제성에 별로 영향을 미치지 않는다.
34. 다음 중 기계적 분리조작과 가장 거리가 먼 것은?
- 여과
- 침강
- 집진
- 분쇄
35. 다음 중 순수한 물 20℃의 점도를 가장 옳게 나타낸 것은?
- 1g/cmㆍS
- 1cP
- 1Paㆍs
- 1kg/mㆍs
36. 항류 열교환기에서 온도 300K의 냉각수 30kg/s을 사용하여 더운 물 20kg/s을 370K에서 340K로 연속 냉각시키려고 한다. 총괄 전열계수를 2.5kW/m2ㆍK로 가정하였을 때 전열 면적은 약 몇 m2인가?
- 22.4
- 34.1
- 41.3
- 50.2
37. 열전달과 온도 관계를 표시한 가장 기본 되는 법칙은?
- 뉴톤의 법칙
- 푸리어의 법칙
- 픽의 법칙
- 후크의 법칙
38. Fanning 마찰계수를 f라 하고 손실수두를 Hf라 할때 Hf와 f의 관계를 나타내는 식은?

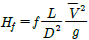
- HF=16/f
- Hf=16f/NRe
39. 다음의 확산식 중 단일 성분 확산과 관계가 있는 식은? (단, NA= 물질이동속도, Dm : 확산계수, B : 확산층 두께, A : 면적, yi, y : 상경계 및 기상의 용질몰 분률)
40. 2개의 관을 연결할 때 사용되는 관 부속품이 아닌것은?
- 유니온(union)
- 니플(nipple)
- 소켓(socket)
- 플러그(plug)
3과목: 공정제어
41. 다음 중 캐스케이드 제어를 적용하기에 가장 적합한 동특성을 가진 경우는?
- 부제어루프 공정 :
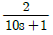 , 주제어루프 공정 :
, 주제어루프 공정 : 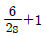
- 부제어루프 공정 :
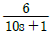 , 주제어루프 공정 :
, 주제어루프 공정 : 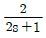
- 부제어루프 공정 :
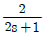 , 주제어루프 공정 :
, 주제어루프 공정 : 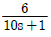
- 부제어루프 공정 :
 , 주제어루프 공정 :
, 주제어루프 공정 : 
42. 다음 공정에 비례제어기(Kc = 3)가 연결되어 있고 초기 정상상태에서 설정값이 5만큼 계단변화할 때 잔류편차는?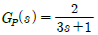
- 0.71
- 1.43
- 3.57
- 4.29
43. Amplitude ratio가 항상 1인 계의 전달함수는?
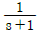
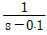
- e-0.2s
- s + 1
44. Routh의 판별법에서 수열의 최좌열(最左列)이 다음과 같을 때 이 주어진 계의 특성방정식은 양의 근 또는 양의 실수부를 갖는 근이 몇 개있는가?
- 0개
- 1개
- 2개
- 3개
45. 전달함수  로 표현되는 공정에 단위계단 입력이 들어왔을 때의 응답과 관련한 내용으로 트린 것은? (단, 시간단위는 분이다.)
로 표현되는 공정에 단위계단 입력이 들어왔을 때의 응답과 관련한 내용으로 트린 것은? (단, 시간단위는 분이다.)
- 출력응답은 최종적으로 6 만큼 변한다.
- 실제 출력변화는 4분 지난 후에 발생한다.
- 역응답(inverse response)을 보이지 않는다.
- 극점값이 실수이므로 진동 응답은 발생하지 않는다.
46. x1과 x2는 다음의 미분방정식을 만족할 때 x1과 x2에 대하여 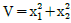 는 시간에 따라 어떻게 되는가?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
는 시간에 따라 어떻게 되는가?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)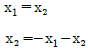
- 감소한다.
- 증가한다.
- 진동한다.
- 초기값에 따라 달라진다.
47. f(t)=1의 Laplace 변환은?
- s
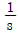
- S2
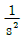
48. 공정에 대한 수학적 모델의 직접적 용도로 부적절한 것은?
- 공정에 대한 이해의 향상
- 공정 운전의 최적화
- 제어 시스템의 설계와 평가
- 제품 시장의 분석 및 평가
49. 제어계를 조작하는 방법으로 몇 가지 방법이 있다. 부하(load)에 변화가 들어오고 설정치(set point)를 일정하게 유지하며 화학공장에서 흔히 나타나는 문제는?
- 서어보 문제
- 레귤레이터 문제
- 혼합 문제
- 브라시우스 문제
50. 정상상태에서의 x와 y의 값을 각각 0, 2라 할 때 함수 f(x, y)=ex+y2-5 을 주어진 정상상태에서 선형화하면?
- x + 4y - 8
- x + 4y - 5
- x + 2y - 8
- x + 2y - 5
51. 피드포워드제어기에 대한 설명으로 옳은 것은?
- 설정점과 제어변수간의 오차를 측정하여 제어기의 입력 정보로 사용한다.
- 주로 PID 알고리즘을 사용한다.
- 보상하고자 하는 외란을 측정할 수 있어야 한다.
- 피드백제어기와 함께 사용하면 성능저하를 가져온다.
52. 어떤 이차계의 특성방정식의 두 근이 다음과 같다고 할 때 단위계단입력에 대하여 감쇠하는 진동 응답을 보이는 공정은?
- 1+3 i, 1-3 i
- -1, -2
- 2, 4
- -1+2 i, -1-2 i
53. 선형제어계의 안전성을 판별하기 위한 특성방정식을 옳게 나타낸 것은?
- 1 + 닫힌 루프 전달함수 = 0
- 1 - 닫힌 루프 전달함수 = 0
- 1 + 열린 루프 전달함수 = 0
- 1 - 열린 루프 전달함수 = 0
54. 다음 블록선도에서 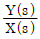 를 구하면?
를 구하면?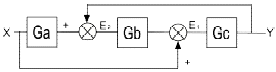
55. 전달함수가 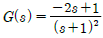 인 공정의 단위계단 응답의 모양으로 옳은 것은?
인 공정의 단위계단 응답의 모양으로 옳은 것은?
56. 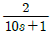 로 표현되는 공정 와 A와
로 표현되는 공정 와 A와 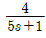 로 표현되는 공정 B가 있을 때 같은 크기의 계단입력이 가해졌을 경우 옳은 것은?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
로 표현되는 공정 B가 있을 때 같은 크기의 계단입력이 가해졌을 경우 옳은 것은?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
- 공정 A가 더 빠르게 정상상태에 도달한다.
- 공정 B가 더 진동이 심한 응답을 보인다.
- 공정 A가 더 진동이 심한 응답을 보인다.
- 공정 B가 더 큰 최종 응답 변화값을 가진다.
57. 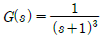 인 공정에
인 공정에 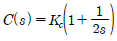 인 PI 제어기가 연결되었을 때, 폐루프가 안정하기 위한 Kc의 최대치와 임계주파수(critical frequency 또는 phase crossover frequency) 값은?
인 PI 제어기가 연결되었을 때, 폐루프가 안정하기 위한 Kc의 최대치와 임계주파수(critical frequency 또는 phase crossover frequency) 값은?
- (4.34, 1.33 (radian/time))
- (0.23, 1.33 (radian/time))
- (4.34, 2.68 (radian/time))
- (0.23, 2.68 (radian/time))
58. 앞먹임 제어에서 사용되는 측정 변수는?
- 공정 상태 변수
- 출력 변수
- 입력 조작 변수
- 측정 가능한 외란
59. 어떤 계의 단위계단 응답이 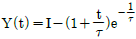 일 경우 이 계의 단위충격 응답(impulse response)은?
일 경우 이 계의 단위충격 응답(impulse response)은?
60. 공정제어(Process Control)의 범주에 들지 않는 것은?
- 전력량을 조절하여 가열로의 온도를 원하는 온도로 유지시킨다.
- 폐수처리장의 미생물의 량을 조절함으로써 유출수의 독성을 격감시킨다.
- 증류탑(Distillation Column)의 탑상농도(Top Concentration)를 원하는 값으로 유지시키기 위하여 무엇을 조절할 것인가를 결정한다.
- 열효율을 극대화시키기 위해 열교환기의 배치를 다시 한다.)
4과목: 공업화학
61. 인산 제조법 중 건식법에 대한 설명으로 틀린 것은?
- 전기로법과 용광로법이 있다.
- 철과 알루미늄 함량이 많은 저품위의 광석도 사용할 수 있다.
- 인의 기화와 산화를 별도로 진행시킬 수 있다.
- 철, 알루미늄, 칼슘의 일부가 인산 중에 함유되어 있어 순도가 낮다.
62. 폴리탄산에스테르 결합을 갖는 열가소성 수지로 비스페놀 A로부터 얻어지며 투명하고 자기소화성을 가지고 있으며, 뛰어난 내충격성, 내한성, 전기적 성질을 균형 있게 갖추고 있는 엔지니어링 플라스틱은?
- 폴리프로필렌
- 폴리아미드
- 폴리이소프렌
- 폴리카보네이트
63. 페놀의 공업적 제조 방법 중에서 페놀과 부산물로 아세톤이 생성되는 합성법은?
- Raschig법
- Cumene법
- Dow법
- Toluene법
64. 다음 중 석유의 접촉 분해시 일어나는 반응으로 가장 거리가 먼 것은?
- 축합
- 탈수소
- 고리화
- 이성질화
65. 반도체의 일반적인 성질에 대한 설명 중 틀린 것은?
- 4족 원소가운데 에너지 갭의 크기순서는 탄소 > 실리콘 > 게르마늄 이다.
- 에너지 갭의 크기가 클수록 전기전도도는 감소한다.
- 진성 반도체의 전기전도도는 온도가 증가함에 따라 감소한다.
- 절대온도 0K에서 전자가 존재하는 최상위 에너지 준위를 페르미 준위라고 한다.
66. 격막법에서 사용하는 식염수의 농도는 30g/100mL이다. 분해율은 50% 일 때 전체 공정을 통한 염의 손실률이 5%이면 몇 m3의 식염수를 사용하여 NaOH 1ton을 생산할 수 있는가? (단, NaCl의 분자량은 58.5이고, NaOH 분자량은 40이다.)
- 10.26
- 20.26
- 30.26
- 40.26
67. 가성소오다를 제조할 때 격막식 전해조에서 양극재료로 주로 사용되는 것은?
- 수은
- 철
- 흑연
- 구리
68. 칼륨 광물 실비아니트(Sylvinite) 중 KCl의 함량은? (단, 원자량은 K : 39.1, Na : 23, Cl : 35.5이다.)
- 36.05%
- 46.05%
- 56.05%
- 66.05%
69. 황산제조방법 중 연실법에 있어서 장치의 능률을 높이고 경제적으로 조업하기 위하여 개량된 방법(또는 설비)인 것은?
- 소량응축법
- Pertersen Tower법
- Reynold법
- Monsanto법
70. 다음 중 무수 염산의 제조법이 아닌 것은?
- 직접 합성법
- 액중 연소법
- 농염산의 증류법
- 건조 흡탈착법
71. 염안소오다법에 의한 Na2CO3제조시 생성되는 부산물은?
- NH4CI
- NaCl
- CaO
- CaCI2
72. 다음 중 슬폰산화가 되기 가장 쉬운 것은?
73. 다음 중 유리기(free radical) 연쇄반응으로 일어나는 반응은?
- CH2=CH2+H2→CH3CH3
- CH4+CI2→CH3CI+CHI
- CH2=CH2+Br2→CH2Br-CH2Br
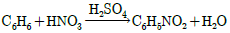
74. 수평균 분자량이 100000인 어떤 고분자 시료 1g과 수평균 분자량이 200000인 같은 고분자 시료 2g을 서로 섞으면 혼합시료의 수평균 분자량은?
- 0.5×105
- 0.667×5
- 1.5×5
- 1.667×5
75. 다음 중 직접적으로 전지의 성능을 나타내는 것이 아닌 것은?
- 에너지 밀도
- 충방전 횟수
- 자기방전율
- 전해질
76. 같은 몰수의 두 종류의 단량체 사이에서 이루어지는 선형 축합중합체의 경우 전환율과 수평규중합도 사이에는 Carothers식에 의한 관계를 가정할 수 있다. 전 환율이 99%인 경우, 얻어지는 축합고분자의 수평균 중합도는?
- 10
- 100
- 1000
- 10000
77. 암모니아 산화에 의한 질산제조 공정에서 사용되는 촉매에 대한 설명으로 틀린 것은?
- 촉매로 백금(Pt)에 Rh이나 Pd를 첨가하여 만든 백금계 촉매가 일반적으로 사용된다.
- 촉매는 단위 중량에 대한 표면적이 큰 것이 유리하다.
- 촉매형상은 직경 0.2cm 이상의 선으로 망을 떠서 사용한다.
- Rh은 가격이 비싸지만 강도, 촉매활성, 촉매손실을 개선하는데 효과가 있다.
78. 다음 중 syndiotactic-폴리스타이렌의 합성에 관여하는 촉매로 가장 적합한 것은?
- 메탈로센 촉매
- 메탈올사이드 촉매
- 린들러 촉매
- 벤조일퍼록사이드
79. 아세틸렌과 작용하여 염화비닐을 생성하는 물질은?
- CI2
- NaCl
- NaClO
- HCl
80. 유지의 분석시험 값으로 성분 지방산의 평균분자량을 알 수 있는 것은?
- Acid value(산값)
- Rhodan value(로단값)
- Acetyl value(아세틸값)
- Saponification value(비누화값)
5과목: 반응공학
81. 체적 0.212m3의 로켓엔진에서 수소가 6kmol/s의 속도로 연소된다. 이 때 수소의 반응속도는 약 몇kmol/m3ㆍs인가?
- 18.0
- 28.3
- 38.7
- 49.0
82. 그림은 단열 조작에서 에너지수지식의 도식적 표현이다. 발열반응의 경우 불활성 물질을 증가시켰을 때 단열 조작선은 어느 방향으로 이동하겠는가? (단, 실선은 불활성 물질이 없는 경우를 나타낸다.)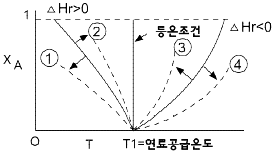
- ①
- ②
- ③
- ④
83. 플러그 흐름반응기(plug flow reactor)에서 반응이 진행된다. 그림의 빗금 친 부분은 무엇을 의미하는가? (단, 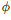 는 반응 A → R에 대해 이 반응기에서 R의 순간수율(instantaneous fractional yield)이다.)
는 반응 A → R에 대해 이 반응기에서 R의 순간수율(instantaneous fractional yield)이다.)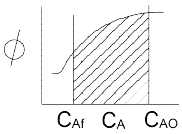
- 총괄수율
- 반응해서 없어진 반응물의 몰수
- 생성되는 R의 최종농도
- 그 순간의 반응물의 농도
84. 액상 비가역 2차 반응 A → B를 [그림]과 같이 순환비 R의 환류식 플러그 흐름 반응기에서 연속적으로 진행 시키고자 한다. 이때 반응기 입구에서의 A의 농도를 옳게 표현한 식은?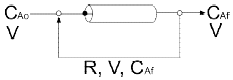
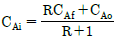
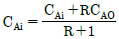
- CAiRCAf+CAo
- CAf=CAf+RCA0
85. 가열적 소반응(기초반응) A+B 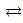 R+S 에서 rR=k1C1CB이고 -rR=k2CRCS 때 다음 중 이 반응의 평형상수 Kc에 해당하는 것은?
R+S 에서 rR=k1C1CB이고 -rR=k2CRCS 때 다음 중 이 반응의 평형상수 Kc에 해당하는 것은?
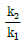
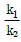
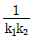
- k1k2
86. 반감기가 50시간인 방사능액체를 10L/h의 속도를 유지하며 직렬로 연결된 두 개의 혼합탱크(각각 V = 4000L)에 통과시켜 처리한다. 이와 같이 처리시킬 때 방사능이 얼마나 감소하겠는가?
- 93.67%
- 95.67%
- 97.67%
- 99.67%
87. 연속흐름 반응기에서 물질수지식으로 옳은 것은?
- 입류량 = 출류량 - 소멸량 + 축적량
- 입류량 = 출류량 - 소멸량 - 축적량
- 입류량 = 출류량 + 소멸량 + 축적량
- 입류량 = 출류량 + 소멸량 - 축적량
88. 그림 A, B, C는 mixed flow reactor와 plug flow reactor을 각각 다르게 연결한 것이다. 1차 이상의 반응에서 (A)의 생성물의 양을 X1로 하고 (B)의 생성물의 양을 X2로 하며, (C)의 생성물의 양을 X3로 하였을 때 옳은 것은?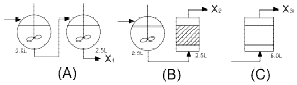
- X1 < X3 < X2
- X2 < X1 < X3
- X1 < X2 < X3
- X3 < X1 < X2
89. 반응전화율을 온도에 대하여 나타낸 직교좌표에서 반응기에 열을 가하면 기울기는 단열과정에서보다 어떻게 되는가?
- 증가한다.
- 감소한다.
- 일정하다.
- 반응열의 크기에 따라 증가 또는 감소한다.
90. 0차 반응의 반응물 농도와 시간과의 관계를 옳게 나타낸 것은?
91. 불균질(heterogeneous) 반응속도에 대한 설명으로 가장 거리가 먼 것은?
- 불균질 반응에서 일반적으로 반응속도식은 화학반응항에 물질 이동항이 포함된다.
- 어떤 단계가 비선형성을 띠며 이를 회피하지 말고 총괄속도식에 적용하여 문제를 해결해야 한다.
- 여러 과정의 속도를 나타내는 단위가 서로 같으면 총괄 속도식을 유도하기 편리하다.
- 총괄 속도식에는 중간체의 농도항이 제거되어야 한다.
92. 이상적 반응기 중 완전교반흐름 반응기에 대한 설명으로 틀린 것은?
- 반응기 입구와 출구의 몰 속도가 같다.
- 정상상태 흐름반응기이다.
- 축방향의 농도 구배가 없다.
- 반응기 내의 온도 구배가 없다.
93. 크기가 다른 2개의 혼합흐름반응기를 사용하여 1차 반응에 의해서 제품을 생산하려 한다. 다음 중 옳은 것은?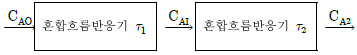
- 혼합흐름반응기의 순서는 전환율에 아무런 영향도 주지 않는다.
- 혼합속도가 느린 반응기를 먼저 설치해야 전환율이 크다.
- 작은 혼합흐름반응기를 먼저 설치해야 전환율이 크다.
- 큰 혼합흐름반응기를 먼저 설치해야 전환율이 크다.
94. 부피가 일정한 회분식반응기에서 반응혼합물 A기체의 최초 압력을 478mmHg로 할 경우에 반감기가 80s 이었다고 한다. 만일 이 A기체의 반응 혼합물에 최초 압력을 315mmHg로 하였을 때 반감기가 120s로 되었다면 반응의 차수는 몇 차 반응으로 예상할 수 있는가? (단, 반응물은 초기 조성이 같고, 비가역 반응이 일어난다.)
- 1차 반응
- 2차 반응
- 3차 반응
- 4차 반응
95. 체적이 일정한 회분식 반응기에서 다음과 같은 기체 반응이 일어난다. 초기의 전압과 분압을 각각 P0, PA0, 나중의 전압을 P라 할 때 분압 PA을 표시하는 식은? (단, 초기에 A, B는 양론비대로 존재하고 R은 없다.)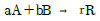
- PA=PA0-[a/(r+a+b)](P-P0)
- PA=PA0-[a/(r-a-b)](P-P0)
- PA=PA0+[a/(r-a-b)](P-P0)
- PA=PA0+[a/(r++)](P-P0)
96. 촉매 반응에서 기공확산 저항에 대한 설명 중 옳은 것은?
- 유효인자(effectiveness factor)가 작을수록 실제 반응속도가 작아진다.
- 고체촉매 반응에서 기공확산 저항만이 율속단계가 될 수 있다.
- 기공확산 저항이 클수록 실제 반응속도는 증가된다.
- 기공확산 저항은 항상 고체입자의 형태에는 무관하다.
97. 양론식 A + 3B → 2R + S가 2차 반응 -rA=K1CAC13일 때 rA, rB와 rR의 관계식으로 옳은 것은?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
- rA=rB=rR
- -rA=-rB=rR
- -rA=(1/3)rB=(1/2)rR
- -rA=-3rB=2rR
98. 부피가 일정한 회분식(batch) 반응기에서 다음의 기초반응(elementary reaction)이 일어난다. 반응속도 상수 k=1.0mol/m3/(sㆍmol), 반응 초기 A의 농도는1.0mol/m3이라면 A의 전화율이 75%일 때까지 걸리는 반응 시간은 얼마인가?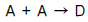
- 1.4s
- 3.0s
- 4.2s
- 6.0s
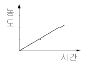
99. 다음은 Arrhenius 법칙에 의해 그린 활성화 에너지(Activation energy)에 대한 그래프이다. 이 그래프에 대한 설명으로 옳은 것은?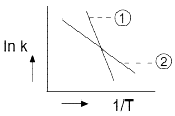
- 직선 ②보다 ①이 활성화 에너지가 크다.
- 직선 ①보다 ②가 활성화 에너지가 크다.
- 초기에는 직선 ①이 활성화 에너지가 크나 후기에는 ②가 크다.
- 초기에는 직선 ②가 활성화 에너지가 크나 후기에는 ①이 크다.
100. 다음의 액상 병렬반응을 연속 흐름 반응기에서 진행 시키고자 한다. 이때 같은 입류조건에 A의 전환율이 모두 0.9가 되도록 반응기를 설계한다면 어느 반응기를 사용하는 것이 R로의 전환율을 가장 크게 해주겠는가? (단 rR=20CA이고 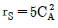 이다.)
이다.)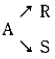
- 플러그 흐름 반응기
- 혼합 흐름 반응기
- 환류식 플러그 흐름 반응기
- 다단식 혼합 흐름 반응기





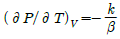
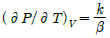
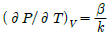
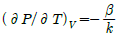

 그래프에서 경로 B $\rightarrow$ C는 부피($V$) 축의 값이 변하지 않고 압력($P$)만 감소하는 수직 직선 형태입니다. 이처럼 부피가 일정하게 유지되는 과정을 정용과정이라고 합니다.
그래프에서 경로 B $\rightarrow$ C는 부피($V$) 축의 값이 변하지 않고 압력($P$)만 감소하는 수직 직선 형태입니다. 이처럼 부피가 일정하게 유지되는 과정을 정용과정이라고 합니다.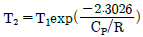

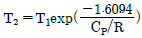
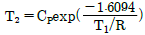
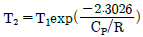 형태의 식이 도출됩니다.
형태의 식이 도출됩니다.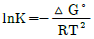 식은 분모에 $T^{2}$가 포함되어 있어 잘못된 표현입니다.
식은 분모에 $T^{2}$가 포함되어 있어 잘못된 표현입니다.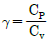
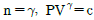

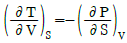
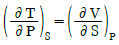
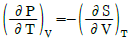
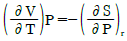
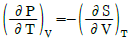 식은 우변에 마이너스($-$) 부호가 붙어 있어 틀린 관계식입니다.
식은 우변에 마이너스($-$) 부호가 붙어 있어 틀린 관계식입니다.
 이며, 수식으로 변환하면 다음과 같습니다.
이며, 수식으로 변환하면 다음과 같습니다.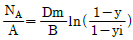
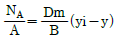
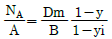
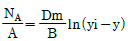
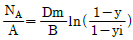 입니다. 이를 수식으로 변환하면 다음과 같습니다.
입니다. 이를 수식으로 변환하면 다음과 같습니다.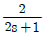 의 시상수는 2분이고,
의 시상수는 2분이고, 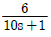 의 시상수는 10분이므로, 부제어루프가 주제어루프보다 5배 빠르게 응답하여 캐스케이드 제어에 가장 적합합니다.
의 시상수는 10분이므로, 부제어루프가 주제어루프보다 5배 빠르게 응답하여 캐스케이드 제어에 가장 적합합니다. 의 최좌열 부호를 살펴보면:
의 최좌열 부호를 살펴보면:
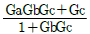


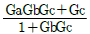 가 정답입니다.
가 정답입니다.

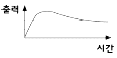

 가 정답입니다.
가 정답입니다.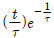
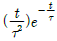
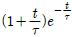
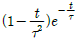
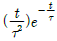 입니다.
입니다.
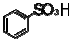
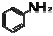
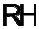
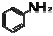 가 가장 반응성이 큽니다.
가 가장 반응성이 큽니다. 에서 이 방향에 해당하는 것은 ③번 화살표 방향입니다.
에서 이 방향에 해당하는 것은 ③번 화살표 방향입니다. 의 빗금 친 부분은 생성되는 R의 최종농도를 나타냅니다.
의 빗금 친 부분은 생성되는 R의 최종농도를 나타냅니다.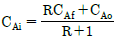 입니다.
입니다.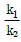 입니다.
입니다. 에서 (A)는 MFR 2개 연결, (B)는 MFR과 PFR 연결, (C)는 단일 PFR 구성이므로, PFR의 비중이 가장 높은 (C)의 생성물 양이 가장 많고 MFR만으로 구성된 (A)가 가장 적습니다. 따라서 $X_1 < X_2 < X_3$ 순으로 나타납니다.
에서 (A)는 MFR 2개 연결, (B)는 MFR과 PFR 연결, (C)는 단일 PFR 구성이므로, PFR의 비중이 가장 높은 (C)의 생성물 양이 가장 많고 MFR만으로 구성된 (A)가 가장 적습니다. 따라서 $X_1 < X_2 < X_3$ 순으로 나타납니다.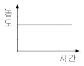

 가 정답입니다.
가 정답입니다.
 그래프에서 직선 ①의 기울기가 직선 ②보다 더 가파르므로(절댓값이 크므로), 직선 ②보다 ①의 활성화 에너지가 더 큽니다.
그래프에서 직선 ①의 기울기가 직선 ②보다 더 가파르므로(절댓값이 크므로), 직선 ②보다 ①의 활성화 에너지가 더 큽니다.
부피 팽창률 $\beta = \frac{1}{V}(\frac{\partial V}{\partial T})_P$와 등온압축률 $k = -\frac{1}{V}(\frac{\partial V}{\partial P})_T$의 정의를 대입하면 다음과 같습니다.
$$(\frac{\partial P}{\partial T})_V = -\frac{1}{(\frac{\partial T}{\partial V})_P (\frac{\partial V}{\partial P})_T} = -\frac{1}{\frac{1}{V\beta} \cdot (-Vk)} = \frac{\beta}{k}$$
따라서 최종식은