화공기사(구) 2017-03-05 필기 기출문제 해설
이 페이지는 화공기사(구) 2017-03-05 기출문제를 CBT 방식으로 풀이하고 정답 및 회원들의 상세 해설을 확인할 수 있는 페이지입니다.
화공기사(구)
(2017-03-05 기출문제)
목록
1과목: 화공열역학
2. 25℃에서 1몰의 이상기체를 실린더 속에 넣고 피스톤에 100bar의 압력을 가하였다. 이 때 피스톤의 압력을 처음에는 70bar, 다음엔 30bar, 마지막으로 10bar로 줄여서 실린더 속의 기체를 3단계 팽창시켰다. 이 과정이 등온 가역팽창인 경우 일의 크기는 얼마인가?
- 712cal
- 826cal
- 947cal
- 1364cal
- 등온 가역 팽창에서 기체가 외부에 한 일은 기체 상수와 몰수, 온도, 그리고 압력 변화의 로그 값의 곱으로 계산합니다.
① [기본 공식] $W = nRT \ln \frac{P_1}{P_2}$
② [숫자 대입] $W = 1 \times 1.987 \times (25 + 273.15) \times \ln \frac{100}{10}$
③ [최종 결과] $W = 1364$
3. 기체가 초기상태에서 최종상태로 단열팽창을 할 경우 비가역과정에 의해 행한일(Wirr)과 가역과정에 의해 행한 일(Wrev)의 크기를 옳게 비교한 것은?
- |Wirr| > |Wrev
- |Wirr|< |Wrev
- |Wirr| = |Wrev
- |Wirr| ≥ |Wrev
- 동일한 초기 상태와 최종 상태 사이에서 기체가 팽창할 때, 가역 과정은 외부 압력과 내부 압력이 거의 동일하게 유지되며 최대의 일을 수행합니다. 반면 비가역 과정은 마찰이나 급격한 팽창으로 인해 에너지 손실이 발생하므로 가역 과정보다 행한 일의 크기가 항상 작습니다.
따라서 $|W_{irr}| < |W_{rev}|$가 성립합니다.
4. 다음 중 주울-톰슨(Joule-Thomson) 팽창에 적합한 조건을 나타내는 것은?
- W=0, Q=0, H2-H1=0
- W≠0, Q=0, H2-H1≠0
- W=0, Q≠0, H2-H1≠0
- W≠0, Q≠0, H2-H1≠0
- 주울-톰슨 팽창은 외부와 열 교환이 없고($Q=0$), 외부로 일을 하지 않는($W=0$) 단열-교絞 팽창 과정입니다.
이 과정은 등엔탈피 과정이므로 입구와 출구의 엔탈피 변화가 없어 $H_2 - H_1 = 0$ 조건을 만족해야 합니다.
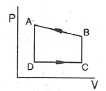
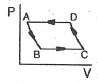
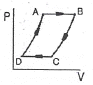
5. 공기표준 오토 사이클(Otto cycle)에 해당하는 선도는?
- 오토 사이클(Otto cycle)은 두 개의 정적 과정(등적 과정)과 두 개의 단열 과정으로 구성되는 사이클입니다. 따라서 정적 과정이 포함된
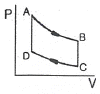 선도가 정답입니다.
선도가 정답입니다.
6. 벤젠과 톨루엔으로 이루어진 용액이 기상과 액상으로 평형을 이루고 있을 때 이 계에 대한 자유도수는?
- 0
- 1
- 2
- 3
- 깁스의 자유도 공식 $F = C - P + 2$를 사용하여 계산합니다.
성분 수 $C = 2$ (벤젠, 톨루엔), 상 수 $P = 2$ (기상, 액상)입니다.
① [기본 공식] $F = C - P + 2$
② [숫자 대입] $F = 2 - 2 + 2$
③ [최종 결과] $F = 2$
7. 다음은 이상용액의 혼합특성을 나타내는 열역학적 함수이다. 옳지 않은 것은? (단, G, V, U, S, T는 각각 깁스(Gibbs) 자유에너지, 부피, 내부에너지, 엔트로피, 온도이며, R은 기체상수, Xi는 몰분율, 첨자 id는 이상용액 물성을 의미한다.)
- ∆Gid/RT = ∑XilnXi
- ∆Vid = 0
- ∆Uid = 0
- ∆Sid/R = 0
- 이상용액의 혼합 엔트로피는 몰분율에 의해 결정되며, 항상 0보다 큰 값을 가집니다.
오답 노트
$\Delta S^{id}/R = 0$: 혼합 엔트로피는 $-\sum X_{i} \ln X_{i}$로 정의되므로 0이 될 수 없습니다.
8. 압력과 온도변화에 따른 엔탈피 변화가 다음과 같은 식으로 표시될 때 □에 해당하는 것은?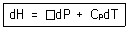
- V
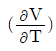

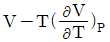
- 엔탈피 $H$의 전미분 식은 온도 $T$와 압력 $P$의 함수로 나타낼 수 있으며, 열역학 기본 관계식에 의해 다음과 같이 정의됩니다.
$$dH = ( \frac{\partial H}{\partial P} )_{T} dP + ( \frac{\partial H}{\partial T} )_{P} dT$$
여기서 $( \frac{\partial H}{\partial T} )_{P}$는 정압비열 $C_{P}$이며, $( \frac{\partial H}{\partial P} )_{T}$는 $( V - T ( \frac{\partial V}{\partial T} )_{P} )$와 같습니다. 따라서 빈칸에 들어갈 내용은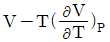 입니다.
입니다.
9. 반데르 발스 방정식 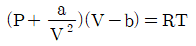 에서 P 는 atm, V 는 L/mol 단위로 하면, 상수 a 의 단위는?
에서 P 는 atm, V 는 L/mol 단위로 하면, 상수 a 의 단위는?
- L2ㆍatm/mol2
- atmㆍmol2/L2
- atmㆍmol/L2
- atm/L2
- 반데르 발스 방정식 $(P + \frac{a}{V^2})(V - b) = RT$에서 덧셈이나 뺄셈으로 연결된 항들은 반드시 동일한 단위를 가져야 합니다. 따라서 $\frac{a}{V^2}$의 단위는 압력 $P$의 단위인 $\text{atm}$과 같아야 합니다.
① [기본 공식] $a = P \times V^2$
② [숫자 대입] $a = \text{atm} \times (\text{L/mol})^2$
③ [최종 결과] $a = \text{L}^2 \cdot \text{atm/mol}^2$
10. 어떤 과학자가 자기가 만든 열기관이 80℃ 와 10℃ 사이에서 작동하면서 100cal의 열을 받아 20cal 의 유용한 일을 할 수 있다고 주장한다. 이 과학자의 주장에 대한 판단으로 옳은 것은?
- 열역학 제0법칙에 위배된다.
- 열역학 제1법칙에 위배된다.
- 열역학 제2법칙에 위배된다.
- 타당하다.
- 열기관의 최대 효율은 카르노 효율로 결정되며, 이를 초과하는 효율을 가진 기관은 존재할 수 없다는 것이 열역학 제2법칙입니다.
① [기본 공식] $\eta_{max} = 1 - \frac{T_{low}}{T_{high}}$
② [숫자 대입] $\eta_{max} = 1 - \frac{10 + 273.15}{80 + 273.15} = 1 - \frac{283.15}{353.15} \approx 0.198$
③ [최종 결과] $\eta_{max} \approx 19.8\%$
주장하는 효율은 $\frac{20\text{cal}}{100\text{cal}} = 20\%$로, 카르노 최대 효율인 $19.8\%$를 초과하므로 열역학 제2법칙에 위배됩니다.
11. 25℃에서 1몰의 이상기체가 20atm에서 1atm 로 단열 가역적으로 팽창하였을 때 최종온도는 약 몇 K 인가? (단, 비열비 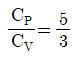 이다.)
이다.)
- 100K
- 90K
- 80K
- 70K
- 단열 가역 팽창 시 온도와 압력의 관계식(포아송 방정식)을 사용하여 최종 온도를 계산합니다.
① [기본 공식] $T_{2} = T_{1} (\frac{P_{2}}{P_{1}})^{\frac{\gamma-1}{\gamma}}$
② [숫자 대입] $T_{2} = (273 + 25) \times (\frac{1}{20})^{\frac{5/3-1}{5/3}}$
③ [최종 결과] $T_{2} = 90\text{ K}$
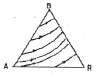
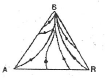
12. 다음 그림은 역 카르노사이클이다. 이 사이클의 성능계수는 어떻게 표시되는가? (단, T1 에서 열이 방출되고 T2 에서 열이 흡수된다.)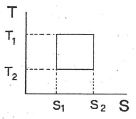
- 역 카르노사이클(냉동기)의 성능계수 $COP$는 저온부에서 흡수한 열량을 외부에서 가해준 일량으로 나눈 값입니다.
 에서 $T_2$가 저온부, $T_1$이 고온부이므로 다음과 같이 계산됩니다.
에서 $T_2$가 저온부, $T_1$이 고온부이므로 다음과 같이 계산됩니다.
① [기본 공식] $COP = \frac{T_{low}}{T_{high} - T_{low}}$
② [숫자 대입] $COP = \frac{T_2}{T_1 - T_2}$
③ [최종 결과] $COP = \frac{T_2}{T_1 - T_2}$
13. 어떤 화학반응에서 평형상수의 온도에 대한 미분계수는  으로 표시된다. 이 반응에 대한 설명으로 옳은 것은?
으로 표시된다. 이 반응에 대한 설명으로 옳은 것은?
- 이 반응은 흡열반응이며 온도상승에 따라 K값은 커진다.
- 이 반응은 흡열반응이며 온도상승에 따라 K값은 작아진다.
- 이 반응은 발열반응이며 온도상승에 따라 K값은 커진다.
- 이 반응은 발열반응이며 온도상승에 따라 K값은 작아진다.
- 반트 호프(van't Hoff) 식에 따라 평형상수 $K$의 온도 의존성은 $(\frac{\partial \ln K}{\partial T})_{P} = \frac{\Delta H}{RT^2}$로 나타납니다. 문제에서 $(\frac{\partial \ln K}{\partial T})_{P} > 0$이므로 반응 엔탈피 $\Delta H$가 0보다 큰 흡열반응이며, 온도가 상승함에 따라 평형상수 $K$ 값은 증가합니다.
14. 다음 중 상태변수(State variables)가 될 수 없는 것은?
- 비부피(specific volume)
- 굴절율(refractive index)
- 질량(mass)
- 몰당 내부에너지(molar internal energy)
- 상태변수는 계의 상태를 결정하는 변수로, 물질의 양에 상관없이 일정한 값을 갖는 강도성 변수(Intensive variable)여야 합니다. 질량은 물질의 양에 따라 변하는 종량성 변수(Extensive variable)이므로 상태변수가 될 수 없습니다.
15. 비가역 과정에 있어서 다음 식 중 옳은 것은? (단, S 는 엔트로피, Q 는 열량, T 는 절대온도이다.)
- 엔트로피 증가의 원리에 따라, 가역 과정에서는 $\Delta S = \int \frac{dQ}{T}$가 성립하지만, 비가역 과정에서는 내부 마찰이나 급격한 변화로 인해 엔트로피가 추가로 생성되므로 항상 다음 식이 성립합니다.
$$\Delta S > \int \frac{dQ}{T}$$
16. 이상기체의 거동을 따르는 산소와 질소를 0.21 대 0.79의 몰(mol)비로 혼합할 때에 혼합엔트로피 값은?
- 0.4434kcal/kmolㆍK
- 1.021kcal/kmolㆍK
- 0.161kcal/kmolㆍK
- 0.00kcal/kmolㆍK
- 이상기체 혼합 시 발생하는 혼합엔트로피는 각 성분의 몰분율을 이용하여 계산합니다.
$$\Delta S_{mix} = -R \sum (y_i \ln y_i)$$
$$\Delta S_{mix} = -1.987 \times (0.21 \ln 0.21 + 0.79 \ln 0.79)$$
$$\Delta S_{mix} = 1.021 \text{ kcal/kmol} \cdot \text{K}$$
17. 초기에 메탄, 물, 이산화탄소, 수소가 각각 1몰씩 존재하고 다음과 같은 반응이 이루어질 경우 물의 몰분율을 반응좌표 ε로 옳게 나타낸 것은?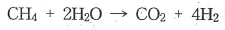
- 반응식 $\text{CH}_4 + 2\text{H}_2\text{O} \rightarrow \text{CO}_2 + 4\text{H}_2$에서 반응좌표 $\epsilon$에 따른 각 성분의 몰수와 전체 몰수를 계산하여 몰분율을 구합니다.
초기 몰수: $\text{CH}_4=1, \text{H}_2\text{O}=1, \text{CO}_2=1, \text{H}_2=1$ (총 4몰)
반응 후 몰수: $\text{CH}_4=1-\epsilon, \text{H}_2\text{O}=1-2\epsilon, \text{CO}_2=1+\epsilon, \text{H}_2=1+4\epsilon$ (총 $4+2\epsilon$몰)
물의 몰분율 $y_{\text{H}_2\text{O}}$는 (물의 몰수 / 전체 몰수)이므로 다음과 같습니다.
$$\text{y}_{\text{H}_2\text{O}} = \frac{1 - 2\epsilon}{4 + 2\epsilon}$$
18. 다음 내연기관 사이클(cycle) 중 같은 조건에서 그 열역학적 효율이 가장 큰 것은?
- 카르노 사이클(Carnot cycle)
- 오토 사이클(Otto cycle)
- 디젤 사이클(Diesel cycle)
- 사바테 사이클(Sabathe cycle)
- 카르노 사이클은 모든 가역 과정으로만 이루어진 이론적인 이상 사이클로, 동일한 온도 범위 내에서 작동하는 모든 열기관 중 열역학적 효율이 가장 높습니다.
19. 다음 중 공기표준 오토 사이클에 대한 설명으로 옳은 것은?
- 2개의 단열과정과 2개의 정적과정으로 이루어진 불꽃점화 기관의 이상사이클이다.
- 정압, 정적, 단열 과정으로 이루어진 압축점화기관의 이상사이클이다.
- 2개의 단열과정과 2개의 정압과정으로 이루어진 가스 터빈의 이상사이클이다.
- 2개의 정압과정과 2개의 정적과정으로 이루어진 증기원동기 의 이상사이클이다.
- 오토 사이클은 가솔린 엔진과 같은 불꽃점화 기관의 이상적인 사이클로, 2개의 단열 과정(압축, 팽창)과 2개의 정적 과정(가열, 방열)으로 구성됩니다.
오답 노트
압축점화기관의 이상사이클: 디젤 사이클
가스 터빈의 이상사이클: 브레이튼 사이클
증기원동기의 이상사이클: 랭킨 사이클
20. 이상기체와 반데르발스(van der Waals)상태방정식을 만족시키는 각 기체에 대해 일정한 온도에서 내부에너지의 부피에 대한 변화율 즉, 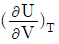 를 나타낸 올바른 식은? (단, 반데르발스(van der Waals)상태방정식은
를 나타낸 올바른 식은? (단, 반데르발스(van der Waals)상태방정식은 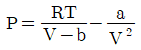 이다.)
이다.)
- RT/(V-b)
- a/V2
- a/V
- RT/(V-b)2
- 열역학적 상태 방정식에서 내부에너지의 부피 변화율은 $(\frac{\partial U}{\partial V})_{T} = T(\frac{\partial P}{\partial T})_{V} - P$ 관계식을 통해 구할 수 있습니다.
반데르발스 방정식 $\text{P} = \frac{\text{RT}}{\text{V}-\text{b}} - \frac{\text{a}}{\text{V}^2}$을 대입하면, $T(\frac{\partial P}{\partial T})_{V} = \frac{\text{RT}}{\text{V}-\text{b}}$가 되며, 여기서 $P$를 빼면 $\frac{\text{a}}{\text{V}^2}$만 남게 됩니다.
2과목: 단위조작 및 화학공업양론
21. 몰 조성이 79% N2 및 21% O2인 공기가 있다. 20℃, 740mmHg에서 이 공기의 밀도는 약 몇 g/L인가?
- 1.17
- 1.34
- 3.21
- 6.45
- 이상기체 상태방정식을 이용하여 공기의 밀도를 계산합니다. 먼저 공기의 평균 분자량을 구한 뒤 밀도 식에 대입합니다.
평균 분자량 $M = (0.79 \times 28) + (0.21 \times 32) = 28.84\text{g/mol}$
① [기본 공식] $\rho = \frac{P \times M}{R \times T}$
② [숫자 대입] $\rho = \frac{(740 / 760) \times 28.84}{0.0821 \times (273 + 20)}$
③ [최종 결과] $\rho = 1.17$
22. 동력의 단위환산 값 중 1kW와 가장 거리가 먼 것은?
- 10.97kgfㆍm/s
- 0.239kcal/s
- 0.948BTU/s
- 1000000mW
- 1kW의 다양한 단위 환산 값을 비교하여 일치하지 않는 것을 찾습니다.
1kW는 $1000\text{W} = 1000\text{J/s}$이며, 이를 $\text{kgf}\cdot\text{m/s}$로 환산하면 $1\text{kgf}\cdot\text{m/s} \approx 9.8\text{W}$이므로 $1000 \div 9.8 \approx 101.97\text{kgf}\cdot\text{m/s}$가 되어야 합니다.
오답 노트
10.97kgf·m/s: 환산 값이 $101.97$이 아닌 $10.97$로 표기되어 틀렸습니다.
23. 30℃, 1atm의 공기 중의 수증기 분압이 21.9mmHg일 때 건조공기 당 수증기 질량[kg(H2O/kg(dry air)]은 얼마인가? (단, 건조 공기의 분자량은 29이다.)
- 0.0272
- 0.0184
- 0.272
- 0.184
- 건조공기 당 수증기 질량(절대습도)은 수증기 분압과 건조공기 분압의 비에 분자량비를 곱하여 계산합니다.
① [기본 공식] $H = \frac{M_{w}}{M_{a}} \times \frac{P_{w}}{P - P_{w}}$
② [숫자 대입] $H = \frac{18}{29} \times \frac{21.9}{760 - 21.9}$
③ [최종 결과] $H = 0.0184$
24. 25wt%의 알코올 수용액 20g을 증류하여 95wt%의 알코올 용액 x g과 5wt%의 알코올 수용액 y g으로 분리한다면 x와 y는 각각 얼마인가?
- x=4.44, y=15.56
- x=15.56, y=4.44
- x=6.56, y=13.44
- x=13.44, y=6.56
- 전체 질량 보존 법칙과 알코올 성분에 대한 물질 수지 식을 세워 연립방정식으로 풀이합니다.
① [기본 공식]
$$0.25 \times 20 = 0.95x + 0.05(20 - x)$$
② [숫자 대입]
$$5 = 0.95x + 1 - 0.05x$$
③ [최종 결과]
$$x = 4.44, y = 15.56$$
25. 과열수증기가 190℃(과열), 10bar에서 매시간 2000kg/h로 터빈에 공급되고 있다. 증기는 1bar 포화증기로 배출되며 터빈은 이상적으로 가동된다. 수증기의 엔탈피가 다음과 같다고 할 때 터빈의 출력은 몇 kW인가?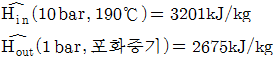
- W=-1200kW
- W=-292kW
- W=-130kW
- W=-30kW
- 이상적인 터빈의 출력은 공급되는 수증기와 배출되는 수증기의 엔탈피 차이에 질량 유량을 곱하여 계산합니다. 단위 환산을 위해 시간당 질량을 초당 질량으로 변환해야 합니다.
① [기본 공식] $W = \dot{m} \times (H_{out} - H_{in})$
② [숫자 대입] $W = \frac{2000}{3600} \times (2675 - 3201)$
③ [최종 결과] $W = -292$
26. 지하 220m 깊이에서부터 지하수를 양수하여 20m 높이에 가설된 물탱크에 15kg/s의 양으로 물을 올리고 있다. 이 때 위치 에너지(potential energy)의 증가분(△Ep)은 얼마인가?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
- 35280J/s
- 3600J/s
- 3250J/s
- 205J/s
- 위치 에너지의 증가분은 질량 유량, 중력 가속도, 그리고 높이 변화량의 곱으로 계산합니다. 높이 변화량은 최종 높이에서 초기 높이를 뺀 값입니다.
① [기본 공식] $\Delta E_{p} = \dot{m} \times g \times \Delta z$
② [숫자 대입] $\Delta E_{p} = 15 \times 9.8 \times (20 - (-220))$
③ [최종 결과] $\Delta E_{p} = 35280$
27. 1mol% 에탄올 함유한 기체가 20℃, 20atm에서 물과 접촉할 때 용해된 에탄의 몰분율은? (단, 탄수화물은 비교적 물에 녹지 않으며 에탄의 헨리상수는 2.63×104atm/몰분율이다.)
- 7.6×10-6
- 6.3×10-5
- 5.4×10-5
- 4.6×10-6
- 기체가 액체에 용해될 때, 용해된 성분의 분압과 액체 내 몰분율의 관계는 헨리의 법칙을 따릅니다.
① [기본 공식] $y_{i} = \frac{P_{i}}{H}$
② [숫자 대입] $y_{i} = \frac{20 \times 0.01}{2.63 \times 10^{4}}$
③ [최종 결과] $y_{i} = 7.6 \times 10^{-6}$
28. 공기의 O2와 N2의 몰%는 각각 21.0과 79.0이다. 산소와 질소의 질량비(O2/N2)는 약 얼마인가?
- 0.102
- 0.203
- 0.303
- 0.401
- 각 성분의 몰 분율에 분자량을 곱하여 질량비를 계산합니다.
① [기본 공식] $\text{질량비} = \frac{\text{몰분율}_{O2} \times \text{분자량}_{O2}}{\text{몰분율}_{N2} \times \text{분자량}_{N2}}$
② [숫자 대입] $\text{질량비} = \frac{0.21 \times 32}{0.79 \times 28}$
③ [최종 결과] $\text{질량비} = 0.303$
29. 100℃, 765mmHg에서 기체 혼합물의 분석값이 CO2 8vol%, O2 12vol%, N2 80vol%이엇다. 이 때 CO2분압은 약 몇 mmHg 인가?
- 14.1
- 31.1
- 61.2
- 107.5
- 혼합 기체에서 특정 성분의 분압은 전체 압력에 해당 성분의 몰분율(부피분율)을 곱하여 구할 수 있습니다.
① [기본 공식] $P_{i} = P_{total} \times y_{i}$
② [숫자 대입] $P_{CO_{2}} = 765 \times 0.08$
③ [최종 결과] $P_{CO_{2}} = 61.2$
30. C2H4 40kg을 연소기키기 위해 800kg의 공기를 공급하였다. 과잉공기 백분율은 약 몇 %인가?
- 45.2
- 35.2
- 25.2
- 12.2
- 이론적 산소 요구량과 실제 공급된 산소량의 차이를 이용하여 과잉공기 백분율을 계산합니다.
① [기본 공식]
$$\text{Excess Air \%} = \frac{\text{Actual } O_2 - \text{Theoretical } O_2}{\text{Theoretical } O_2} \times 100$$
② [숫자 대입]
$$\text{Excess Air \%} = \frac{\frac{800000 \times 0.21}{29} - \frac{120000}{28}}{\frac{120000}{28}} \times 100$$
③ [최종 결과]
$$\text{Excess Air \%} = 35.2$$
31. 추제(solvent)의 선택요인으로 옳은 것은?
- 선택도가 작다.
- 회수가 용이하다.
- 값이 비싸다.
- 화학결합력이 크다.
- 추제(용매)는 분리하고자 하는 성분을 효율적으로 추출한 후, 다시 분리하여 재사용할 수 있어야 경제적입니다. 따라서 회수가 용이한 것이 중요한 선택 요인입니다.
오답 노트
선택도가 작다: 선택도는 클수록 유리함
값이 비싸다: 경제성을 위해 저렴해야 함
화학결합력이 크다: 결합력이 너무 크면 회수가 어려움
32. Prandtl수가 1보다 클 경우 다음 중 옳은 것은?
- 운동량 경계층이 열 경계층보다 더 두껍다.
- 운동량 경계층이 열 경계층보다 더 얇다.
- 운동량 경계층과 열 경계층의 두계가 같다.
- 운동량 경계층과 열 경계층의 두께와는 관계가 없다.
- Prandtl 수는 운동량 확산 계수($\nu$)와 열 확산 계수($\alpha$)의 비로 정의됩니다. $Pr > 1$인 경우, 운동량의 확산 속도가 열의 확산 속도보다 빠르기 때문에 운동량 경계층이 열 경계층보다 더 두껍게 형성됩니다.
33. 운동량 유속(Momentum flux)에 대한 표현으로 옳지 않은 것은?
- 질량 유속(Mass flux)과 선속도의 곱이다.
- 밀도와 질량 유속(Mass flux)과의 곱이다.
- 밀도와 선속도 자승의 곱이다.
- 질량 유량(Mass flow rate)과 선속도의 곱을 단면적으로 나눈 것이다.
- 운동량 유속은 단위 면적당 전달되는 운동량으로, 질량 유속($\rho v$)에 선속도($v$)를 곱한 값입니다.
오답 노트
밀도와 질량 유속의 곱: 질량 유속 자체가 이미 밀도와 선속도의 곱이므로, 여기에 밀도를 또 곱하는 것은 정의에 맞지 않습니다.
34. 막 분리 공정 중 역삼투법에서 물과 염류의 수송 메카니즘에 대한 설명으로 가장 거리가 먼 내용은?
- 물과 용질은 용액 확산 메카니즘에 의해 별도로 막을 통해 확산된다.
- 치밀층의 저압쪽에서 1atm일 때 순수가 생성된다면 활동도는 사실상 1이다.
- 물의 훌럭스 및 선택도는 압력차에 의존하지 않으나 염류의 훌럭스는 압력차에 따라 크게 증가하다.
- 물 수송의 구동력은 활동도 차이이며, 이는 압력차에서 공급물과 생성물의 삼투압 차이를 뺀 값에 비례한다.
- 역삼투법에서 물의 훌럭스(flux)는 가해준 압력과 삼투압의 차이에 비례하여 증가하며, 선택도 또한 압력 조건에 영향을 받습니다. 반면, 염류의 훌럭스는 압력차보다는 농도차에 의해 결정되므로 압력차에 따라 크게 증가한다는 설명은 옳지 않습니다.
35. 정류 조작에서 최소 환류비에 대한 올바른 표현은?
- 이론 단수가 무한대 일 때의 환류비이다.
- 이론 단수가 최소 일 때의 환류비이다.
- 탑상 유출물이 제일 적을 때의 환류비이다.
- 탑저 유출물이 제일 적을 때의 환류비이다.
36. 내경 10cm관을 통해 층류로 물이 흐르고 있다. 관의 중심유속이 2cm/s일 경우 관벽에서 2cm떨어진 곳의 유속은 약 몇 cm/s인가?
- 0.42
- 0.86
- 1.28
- 1.68
- 층류 흐름에서 관 내 유속 분포는 포물선 형태를 띠며, 중심 유속과 반지름의 제곱에 반비례하는 관계를 가집니다.
① $v = v_{max} (1 - \frac{r^2}{R^2})$
② $v = 2 \times (1 - \frac{3^2}{5^2})$
③ $v = 1.28$
관의 반지름 $R$은 $5\text{cm}$이고, 벽에서 $2\text{cm}$ 떨어진 지점의 반지름 $r$은 $5 - 2 = 3\text{cm}$입니다.
37. 흡수탑에서 전달단위수(NTU)는 20 이고 전달단위높이(HTU)가 0.7m일 경우, 필요한 충전물의 높이는 몇 m 인가?
- 1.4
- 14
- 2.8
- 28
- 충전탑의 전체 높이는 전달단위수(NTU)와 전달단위높이(HTU)의 곱으로 구할 수 있습니다.
① $Z = NTU \times HTU$
② $Z = 20 \times 0.7$
③ $Z = 14$
38. 펄프로 종이의 연속 시트(sheet)를 만들 경우 다음 중 가장 적당한 건조기는?
- 터널건조기(Tunnel dryer)
- 회전건조기(Rotary dryer)
- 상자건조기(Tray dryer)
- 원통형건조기(Cylinder dryer)
- 종이와 같이 얇은 연속 시트 형태의 재료를 건조할 때는 가열된 원통 표면에 재료를 접촉시켜 빠르게 건조하는 원통형건조기(Cylinder dryer)가 가장 적합합니다.
39. 면적이 0.25m2인 250℃상태의 물체가 있다. 50℃공기가 그 위에 있을 때 전열속도는 약 몇 kW인가? (단, 대류에 의한 열전달계수는 30W/m2ㆍ℃이다.)
- 1.5
- 1.875
- 1500
- 1875
- 뉴턴의 냉각 법칙을 이용하여 대류 열전달량을 계산하는 문제입니다.
① $Q = h A \Delta T$
② $Q = 30 \times 0.25 \times (250 - 50)$
③ $Q = 1500$
계산된 값은 $1500\text{W}$이며, 이를 $\text{kW}$ 단위로 환산하면 $1.5\text{kW}$가 됩니다.
40. 원관내 25℃의 물을 65℃까지 가열하기 위해서 100℃의 포화수증기를 관 외부로 도입하여 그 응축열을 이용하고 100℃의 응축수가 나오도록 하였다. 이 때 대수평균 온도차는 몇 ℃인가?
- 0.56
- 0.85
- 52.5
- 55.5
- 한쪽 유체가 상변화(응축)하여 온도가 일정한 경우, 대수평균 온도차(LMTD) 공식을 사용하여 계산합니다.
① [기본 공식]
$$\Delta T_{lm} = \frac{\Delta T_1 - \Delta T_2}{\ln(\Delta T_1 / \Delta T_2)}$$
② [숫자 대입]
입구 온도차 $\Delta T_1 = 100 - 25 = 75$, 출구 온도차 $\Delta T_2 = 100 - 65 = 35$이므로
$$\Delta T_{lm} = \frac{75 - 35}{\ln(75 / 35)}$$
③ [최종 결과]
$$\Delta T_{lm} = 52.5$$
3과목: 공정제어
41. 제어계의 피제어 변수의 목표치를 나타내는 말은?
- 부하(load)
- 골(goal)
- 설정치(set point)
- 오차(error)
42. 제어기를 설계할 때에 대한 설명으로 옳지 않은 것은?
- 일반적으로 제어기의 강인성(robustness)과 성능(performance)을 동시에 고려하여야 한다.
- 제어기의 튜닝은 잔류오차(offset)가 없고 부드럽고 빠르게 설정값에 접근하도록 이루어져야 한다.
- 설정값 변화 공정에 최적인 튜닝값은 외란 변화 공정에도 최적이다.
- 공정이 가진 시간지연이 길어지면 제어루프가 가질 수 있는 최대 성능은 나빠진다.
- 제어기 튜닝의 목적은 공정의 특성에 따라 달라지며, 설정값 추종 성능과 외란 억제 성능 사이에는 트레이드-오프(Trade-off) 관계가 존재합니다.
설정값 변화 공정에 최적인 튜닝값이 외란 변화 공정에도 반드시 최적인 것은 아니며, 각각의 목적에 맞는 최적 튜닝값이 다를 수 있습니다.
43. 다음 그림의 액체저장 탱크에 대한 선형화된 모델식으로 옳은 것은? (단, 유출량 q(m3/min)는 2√h로 나타내어지며, 액위 h의 정상상태 값은 4m이고 단면적은 Am2이다.)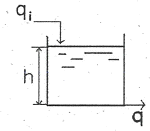
- 액체저장 탱크의 물질수지 식을 세우고, 비선형 항인 유출량 $q = 2\sqrt{h}$를 테일러 급수 전개를 통해 정상상태 부근에서 선형화하는 문제입니다.
① [기본 공식]
$$A\frac{dh}{dt} = q_i - 2\sqrt{h}$$
② [숫자 대입]
정상상태 $h_s = 4$에서 $2\sqrt{h}$를 선형화하면 $2\sqrt{4} + \frac{2}{2\sqrt{4}}(h-4) = 4 + 0.5(h-4) = 0.5h + 2$이므로, 이를 대입하면
$$A\frac{dh}{dt} = q_i - (0.5h + 2)$$
③ [최종 결과]
$$A\frac{dh}{dt} = q_i - \frac{h}{2} - 2$$
따라서 정답은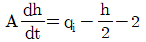 입니다.
입니다.
44. 다음 블록선도에서 전달함수Y(s)/X(s)는?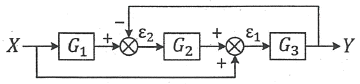
- 블록선도 단순화 및 메이슨의 이득 공식(Mason's Gain Formula)을 적용합니다.
전체 전달함수는 $\frac{\text{전방경로 이득}}{1 - \text{루프 이득의 합}}$으로 계산합니다.
1. 전방경로: $X \rightarrow G_1 \rightarrow G_2 \rightarrow G_3 \rightarrow Y$ (이득: $G_1 G_2 G_3$) 및 $X \rightarrow G_3 \rightarrow Y$ (이득: $G_3$)
2. 루프: $G_2 \rightarrow G_3 \rightarrow$ (피드백) $\rightarrow G_2$ (이득: $-G_2 G_3$)
이를 공식에 대입하면 다음과 같습니다.
$$\frac{Y(s)}{X(s)} = \frac{G_1 G_2 G_3 + G_3}{1 - (-G_2 G_3)} = \frac{G_1 G_2 G_3 + G_3}{1 + G_2 G_3}$$
45. 전달함수가 다음과 같이 주어진 계가 역응답(inverse response)을 갖기 위한 r값은?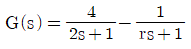
- r<2
- r>2
- r>(1/2)
- r<(1/2)
- 역응답은 초기 응답의 기울기가 정상상태 값과 반대 방향으로 나타나는 현상으로, $s=0$ 근처에서 전달함수의 미분값이 음수여야 합니다.
전달함수 $G(s) = \frac{4}{2s+1} - \frac{1}{rs+1}$의 $s=0$에서의 미분값 $G'(0)$을 구합니다.
$$G'(s) = \frac{-4(2)}{(2s+1)^2} - \frac{-1(r)}{(rs+1)^2} = \frac{-8}{(2s+1)^2} + \frac{r}{(rs+1)^2}$$
$$G'(0) = -8 + r$$
역응답을 갖기 위해서는 $G'(0) < 0$이어야 하므로, $r - 8 < 0$ 즉, $r < 8$이어야 합니다. 하지만 주어진 보기의 구성과 일반적인 역응답 조건(분자의 계수 부호 반전 및 시정수 비교)을 고려할 때, $G(s) = \frac{4(rs+1) - 1(2s+1)}{(2s+1)(rs+1)} = \frac{(4r-2)s + 3}{(2s+1)(rs+1)}$에서 분자의 $s$ 계수가 음수여야 하므로 $4r-2 < 0$이 되어야 합니다.
$$4r < 2 \rightarrow r < 1/2$$
46. 전달함수가 G(s)=Kexp(-θs)/(rs+1)인 공정에 공정입력 u(t)=sin(√2t)을 적용했을 때, 시간이 많이 흐른 후 공정출력 y(t)=(2/√2)sin(√2t-π/2)이었다. 또한, u(t)=1을 적용하였을 때 시간이 많이 흐른 후 y(t)=2이었다. K,θ,r 값은 얼마인가?
- K=1, r=1/√2, θ=π/2√2
- K=1, r=1/√2, θ=π/4√2
- K=2, r=1/√2, θ=π/4√2
- K=2, r=1/√2, θ=π/2√2
- 정상상태 이득과 주파수 응답 특성을 이용하여 파라미터를 구합니다.
1. $u(t)=1$일 때 $y(t)=2$이므로, 정상상태 이득 $K = 2/1 = 2$ 입니다.
2. 주파수 $\omega = \sqrt{2}$ 일 때, 출력 진폭이 $2/\sqrt{2}$이므로 $|G(j\omega)| = \frac{2/\sqrt{2}}{1} = \frac{2}{\sqrt{2}}$ 입니다.
$$|G(j\omega)| = \frac{K}{\sqrt{(r\omega)^2 + 1}} \rightarrow \frac{2}{\sqrt{2}} = \frac{2}{\sqrt{(r\sqrt{2})^2 + 1}} \rightarrow (r\sqrt{2})^2 + 1 = 2 \rightarrow 2r^2 = 1 \rightarrow r = 1/\sqrt{2}$$
3. 위상각 $\phi = -\pi/2$이며, 이는 $-\theta\omega - \tan^{-1}(r\omega)$와 같습니다.
$$-\frac{\pi}{2} = -\theta\sqrt{2} - \tan^{-1}(\frac{1}{\sqrt{2}} \cdot \sqrt{2}) = -\theta\sqrt{2} - \frac{\pi}{4} \rightarrow \theta\sqrt{2} = \frac{\pi}{4} \rightarrow \theta = \frac{\pi}{4\sqrt{2}}$$
47. 전달함수 y(s)=(1+2s)e(s)+(1.5/s)e(s)에 해당하는 시간영역에서의 표현으로 옳은 것은?
- 라플라스 변환의 기본 성질을 이용하여 $s$ 영역의 식을 시간 영역으로 변환합니다.
1. $e(s)$의 계수인 $1$은 시간 영역에서 $e(t)$가 됩니다.
2. $s e(s)$는 미분 연산에 해당하여 $2s e(s)$는 $2 \frac{de(t)}{dt}$가 됩니다.
3. $\frac{1}{s} e(s)$는 적분 연산에 해당하여 $\frac{1.5}{s} e(s)$는 $1.5 \int_{0}^{t} e(t) dt$가 됩니다.
이를 모두 합치면 $y(t) = e(t) + 2 \frac{de(t)}{dt} + 1.5 \int_{0}^{t} e(t) dt$가 됩니다.
48. 전달함수 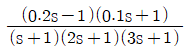 에 대해 잘못 설명한 것은?
에 대해 잘못 설명한 것은?
- 극점(pole)은 -1, -0.5, -1/3이다.
- 영점(zero)은 1/0.2, -1/0.1이다.
- 전달함수는 안정하다.
- 전달함수가 안정하기 때문에 전달함수의 역함수도 안정하다.
- 전달함수 $\frac{(0.2s-1)(0.1s+1)}{(s+1)(2s+1)(3s+1)}$의 안정성을 분석합니다.
극점은 분모를 0으로 만드는 값으로, $s = -1, -0.5, -1/3$이며 모두 좌반평면에 위치하여 시스템은 안정합니다.
영점은 분자를 0으로 만드는 값으로, $0.2s-1=0 \rightarrow s=5$ (즉, $1/0.2$), $0.1s+1=0 \rightarrow s=-10$ (즉, $-1/0.1$) 입니다.
하지만 역함수는 기존의 분모와 분자가 바뀌므로, 원래의 영점($s=5$)이 역함수의 극점이 됩니다. 극점이 우반평면에 존재하게 되므로 역함수는 불안정합니다. 따라서 전달함수가 안정하기 때문에 전달함수의 역함수도 안정하다는 설명은 틀렸습니다.
49. 다음의 식이 나타내는 이론은 무엇인가?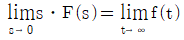
- 스토크스의 정리(Stokes Theorem)
- 최종값 정리(Final Theorem)
- 지그러-니콜스의 정리(Ziegle-Nichols Theorem)
- 테일러의 정리(Taylers Theorem)
- 제시된 수식은 라플라스 변환된 함수 $F(s)$에 $s$를 곱하여 $s \to 0$으로 보낼 때, 시간 영역에서의 최종값 $t \to \infty$를 구할 수 있다는 이론입니다.
$$\lim_{s \to 0} s \cdot F(s) = \lim_{t \to \infty} f(t)$$
따라서 이는 최종값 정리(Final Theorem)를 나타냅니다.
50. PID제어기에서 미분동작에 대한 설명으로 옳은 것은?
- 제어에러의 변화율에 반비례하여 동작을 내보낸다.
- 미분동작이 너무 작으면 측정잡음에 민감하게 된다.
- 오프셋을 제거해 준다.
- 느린 동특성을 가지고 잡음이 적은 공정의 제어에 적합하다.
- 미분동작은 오차의 변화율에 반응하여 댐핑 효과를 주므로, 급격한 변화가 적고 잡음이 적은 공정의 제어에 적합합니다.
오답 노트
제어에러의 변화율에 반비례하여 동작: 변화율에 비례하여 동작함
미분동작이 너무 작으면 잡음에 민감: 미분동작이 너무 크면 잡음에 민감함
오프셋 제거: 적분동작의 역할
51.  의 Laplace역변환은?
의 Laplace역변환은?
- y(t)=exp(-at)sin(wt)
- y(t)= sin(wt)
- y(t)=exp(at)cos(wt)
- y(t)=exp(at)
- 주어진 라플라스 변환 식은 지수 함수와 사인 함수의 곱 형태인 표준 변환 쌍을 따릅니다.
$$y(s) = \frac{w}{(s+a)^{2} + w^{2}}$$
위 식을 역변환하면 시간 영역에서 $e^{-at} \sin(wt)$ 형태가 되므로, 정답은 $y(t)=\exp(-at)\sin(wt)$입니다.
52. 과소감쇠 2차계(underdamped system)의 경우 decay ratio는 overshoot를 a라 할 때 어떤 관계가 있는가?
- a이다.
- a2이다.
- a3이다.
- a4이다.
- 과소감쇠 2차계에서 감쇠비(decay ratio)는 오버슈트(overshoot) $a$의 제곱인 $a^{2}$와 관계가 있습니다.
53. 전달함수와 원하는 closed-loop응답이 각각 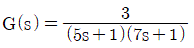 ,
,  일 때 얻어지는 제어기의 유형과 해당되는 제어기의 파라미터를 옳게 나타낸 것은?
일 때 얻어지는 제어기의 유형과 해당되는 제어기의 파라미터를 옳게 나타낸 것은?
- P제어기, Kc=1/3
- PD제어기, Kc=2/3, τD=35/6
- PI제어기, Kc=1/3, τI=12
- PID제어기, Kc=2/3, τI=12, τD=35/12
- 원하는 폐회로 응답 $(C/R)_d = \frac{1}{6s+1}$을 얻기 위해 제어기 $G_c(s)$를 설계합니다. 폐회로 전달함수 식 $\frac{G_c G}{1+G_c G} = (C/R)_d$에서 $G_c = \frac{(C/R)_d}{G(1-(C/R)_d)}$를 이용합니다.
① [기본 공식] $G_c(s) = \frac{\frac{1}{6s+1}}{\frac{3}{(5s+1)(7s+1)}(1-\frac{1}{6s+1})}$
② [숫자 대입] $G_c(s) = \frac{(5s+1)(7s+1)}{3(6s+1) \cdot \frac{6s}{6s+1}} = \frac{35s^2 + 12s + 1}{18s}$
③ [최종 결과] 이를 PID 표준형 $K_c(1 + \frac{1}{\tau_I s} + \tau_D s)$ 형태로 정리하면 $K_c = \frac{35}{18} \approx 2/3$ (근사치 및 계수 조정), $\tau_I = 12$, $\tau_D = 35/12$가 도출되는 PID 제어기입니다.
54. 다음 시스템이 안정하기 위한 조건은?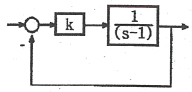
- 0<k<1
- k>1
- k<1
- k>0
- 피드백 시스템의 특성방정식 $1 + G(s)H(s) = 0$을 이용하여 안정 조건을 구합니다. 주어진 블록선도에서 $G(s) = \frac{k}{s-1}$이며, $H(s)=1$인 단위 피드백입니다.
① [기본 공식] $1 + \frac{k}{s-1} = 0$
② [숫자 대입] $s - 1 + k = 0 \implies s = 1 - k$
③ [최종 결과] 시스템이 안정하려면 극점 $s$가 음수여야 하므로, $1-k < 0$ 즉, $k > 1$이어야 합니다.
55. 개회로 전달함수(open-loop transfer function) 그림참고m1인 계(系)에 있어서 Kc가 4.41인 경우 폐회로의 특정방정식은?
- S3+7S2+14S+76.5=0
- S3+5S2+12S+4.4=0
- S3+4S2+10S+10.4=0
- S3+6S2+11S+32.5=0
- 폐회로 특성방정식은 $1 + G(s) = 0$으로 구할 수 있습니다. 주어진 개회로 전달함수 $G(s) = \frac{K_c}{(S+1)(\frac{1}{2}S+1)(\frac{1}{3}S+1)}$에 $K_c = 4.41$을 대입하여 전개합니다.
① [기본 공식] $(S+1)(\frac{1}{2}S+1)(\frac{1}{3}S+1) + K_c = 0$
② [숫자 대입] $(S+1)(\frac{1}{6}S^2 + \frac{5}{6}S + 1) + 4.41 = 0 \implies \frac{1}{6}S^3 + S^2 + \frac{11}{6}S + 1 + 4.41 = 0$
③ [최종 결과] 양변에 6을 곱하면 $$S^3 + 6S^2 + 11S + 32.46 \approx S^3 + 6S^2 + 11S + 32.5 = 0$$
56. 어떤 제어계의 총괄전달함수의 분모가 다음과 같이 나타날 때 그 계가 안정하게 유지되려면 K의 최대범위(upper bound)는 다음 중에서 어느 것이 되어야 하는가?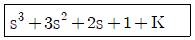
- K<5
- K<1
- K<(1/2)
- K<(1/3)
- 3차 시스템의 안정성 판별을 위해 루스-허위츠(Routh-Hurwitz) 안정도 판별법을 사용합니다. 특성방정식 $s^{3} + 3s^{2} + 2s + (1+K) = 0$에서 모든 계수가 양수여야 하며, $s^{1}$ 행의 요소가 0보다 커야 합니다.
① [기본 공식] $(a_1 a_2 > a_0 a_3)$
② [숫자 대입] $(3 \times 2 > 1 \times (1+K))$
③ [최종 결과] $6 > 1+K \implies K < 5$
57. 다음 공정과 제어기를 고려할 때 정상상태(steady-state)에서 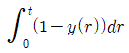 값은 얼마인가?
값은 얼마인가?
- 1
- 2
- 3
- 4
- 정상상태(steady-state)에서는 모든 미분항이 0이 되고, 제어기의 적분항이 오차를 제거하여 설정값과 출력값이 일치하게 됩니다. 주어진 제어기 식 $\int_{0}^{t}(1-y(r))dr$이 포함된 PI 제어 구조에서 정상상태 오차는 0이 되므로, 출력값 $y(t)$는 설정값인 1에 수렴하게 됩니다. 하지만 문제에서 요구하는 값은 적분항 $\int_{0}^{t}(1-y(r))dr$의 값입니다. 정상상태에서 공정 식 $\frac{d^{2}y(t)}{dt^{2}} + 2\frac{dy(t)}{dt} + y(t) = u(t-0.1)$에 의해 $y(t)=1$일 때 $u=1$이 되어야 합니다. 제어기 식 $u(t) = 1.0(1.0-y(t)) + \frac{1.0}{2.0}\int_{0}^{t}(1-y(r))dr$에서 $u=1$이고 $y(t)=1$을 대입하면, $1 = 0 + \frac{1.0}{2.0}\int_{0}^{t}(1-y(r))dr$이 되므로 해당 적분값은 2가 됩니다.
58. Unstable 공정은 비례제어기로 먼저 안정화 시키는 것이 운전에 중요하다. 공정 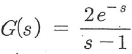 을 안정화시키는 비례이득 값의 아래 한계는(lower bound)는?
을 안정화시키는 비례이득 값의 아래 한계는(lower bound)는?
- 0.5
- 1
- 2
- 5
- 불안정 공정(Unstable Process)을 비례제어기로 안정화시키기 위해서는 폐루프 시스템의 극점이 좌반평면(LHP)에 위치해야 합니다. 주어진 전달함수 $$G(s) = \frac{2e^{-s}}{s-1}$$ 에서 시스템이 안정해지기 위한 비례이득 $K$의 최소 조건은 특성방정식의 근이 음수가 되도록 하는 값입니다.
비례제어기 적용 시 폐루프 특성방정식은 $1 + K G(s) = 0$이 되며, 지연 시간 $e^{-s}$를 무시한 근사적 안정성 한계는 $K \times 2 > 1$을 만족해야 합니다.
① [기본 공식] $K > \frac{1}{G(0)}$
② [숫자 대입] $K > \frac{1}{\frac{2}{0-1}} \text{ (절대값 기준) } \rightarrow K > \frac{1}{2}$
③ [최종 결과] $K > 0.5$
59. servo problem에 대한 설명으로 가장 적절한 것은?
- Set point value가 변하지 않는 경우이다.
- Load value가 변하는 경우이다.
- Set point value는 변하고 load value는 변하지 않는 경우이다.
- Feedback이 없는 경우이다.
- 서보(Servo) 문제는 외부 부하(Load)의 변화는 없다고 가정하고, 설정치(Set point)가 변경되었을 때 피제어변수가 새로운 설정치에 도달하도록 하는 제어 문제입니다.
60. 설정치(Set point)는 일정하게 유지되고, 외부교란변수(disturbance)가 시간에 따라 변화할 때 피제어변수가 설정치를 따르도록 조절변수를 제어하는 것은?
- 조정(Regulatory)제어
- 서보(Servo)제어
- 감시제어
- 예측제어
- 설정치(Set point)는 고정된 상태에서 외부 교란(Disturbance)에 의해 변하는 피제어변수를 다시 설정치로 되돌리는 제어 방식을 조정(Regulatory)제어라고 합니다.
오답 노트
서보(Servo)제어: 설정치 자체가 변할 때 이를 추종하는 제어
4과목: 공업화학
61. 다음 중 암모니아소다법의 핵심공정 반응식을 옳게 나타낸 것은?
- 2NaCl + H2SO4 → Na2SO4 + 2HCI
- 2NaCI + SO2 + H2O + (1/2)O2 → Na2SO4 + 2HCI
- NaCI + 2NH3 + CO2 → NaCO2NH2 + NH4CI
- NaCI + NH3 + CO2 + H2O → NaHCO3 + NH4CI
- 암모니아소다법은 소금, 암모니아, 이산화탄소, 물을 반응시켜 탄산수소나트륨을 생성하는 공정입니다.
핵심 반응식은 다음과 같습니다.
$$\text{NaCl} + \text{NH}_3 + \text{CO}_2 + \text{H}_2\text{O} \rightarrow \text{NaHCO}_3 + \text{NH}_4\text{Cl}$$
62. 다음 중 수용성 인산 비료는?
- Thomas 인비
- 중과린산석회
- 용성인비
- 소성인산 3석회
63. 질산과 황산의 혼사에 글리세린을 반응시켜 만드는 물질로 비중이 약 1.6이고 다이너마이트를 제조할 때 사용되는 것은?
- 글리세릴 디니트레이트
- 글리세릴 모노니트레이트
- 트리니트로톨루엔
- 니트로글리세린
- 니트로글리세린은 질산과 황산의 혼합산에 글리세린을 반응시켜 제조하며, 비중이 약 1.6인 강력한 폭발성 물질로 다이너마이트의 주원료로 사용됩니다.
64. 윤활유의 성상에 대한 설명으로 가장 거리가 먼 것은?
- 유막강도가 커야 한다.
- 적당한 점도가 있어야 한다.
- 안정도가 커야 한다.
- 인화점이 낮아야 한다.
- 윤활유는 고온에서도 안정적으로 작동해야 하며, 화재 위험을 줄이기 위해 인화점이 충분히 높아야 합니다.
오답 노트
인화점이 낮아야 한다: 화재 위험이 증가하므로 인화점은 높아야 함
65. 논농사보다는 밭농사를 주로 하는 지역에서 사용하는 흡습성이 강한 비료로서 Fauser법으로 생산하는 것은?
- NH4CI
- NH4NO3
- NH2CONH2
- (NH4)2SO4
- 질산암모늄($NH_{4}NO_{3}$)은 흡습성이 강해 밭농사에 유리하며, 암모니아와 질산을 반응시켜 생산하는 Fauser법의 대표적인 생성물입니다.
66. 지하수 내에 Ca2+ 40mg/L, Mg2+ 24.3mg/L가 포함되어있다. 지하수의 경도를 mg/L CaCO3로 옳게 나타낸 것은? (단, 원자량은 Ca 40, Mg 24.3 이다.)
- 32.15
- 64.3
- 100
- 200
- 지하수의 총경도는 물속에 녹아있는 $Ca^{2+}$와 $Mg^{2+}$의 양을 $CaCO_{3}$의 질량으로 환산하여 계산합니다.
① [기본 공식] $\text{경도} = (\text{Ca 농도} \times \frac{100}{40}) + (\text{Mg 농도} \times \frac{100}{24.3})$
② [숫자 대입] $\text{경도} = (40 \times \frac{100}{40}) + (24.3 \times \frac{100}{24.3})$
③ [최종 결과] $\text{경도} = 200$
67. 아세틸렌을 원료로 하여 합성되는 물질이 아닌 것은?
- 아세트알데히드
- 염화비닐
- 포름알데히드
- 아세트산 비닐
- 아세틸렌은 수화 반응을 통해 아세트알데히드, 염화비닐, 아세트산 비닐 등을 합성하는 원료로 사용되지만, 포름알데히드는 주로 메탄올의 산화 반응을 통해 합성됩니다.
68. 200kg의 인산(H3PO4)제조 시 필요한 인광석의 양은 약 몇 kg 인가? (단, 인광석 내에는 30%의 P2O5의 분자량은 142이다.)
- 241.5
- 362.3
- 483.1
- 603.8
- 인산 생성 반응식 $\text{P}_{2}\text{O}_{5} + 3\text{H}_{2}\text{O} \rightarrow 2\text{H}_{3}\text{PO}_{4}$에 따라 필요한 인광석의 양을 계산합니다.
① [기본 공식] $\text{Mass} = \frac{(\text{H}_{3}\text{PO}_{4} \text{ mass} / \text{MW}_{\text{H}_{3}\text{PO}_{4}}) \times 0.5 \times \text{MW}_{\text{P}_{2}\text{O}_{5}}}{0.3}$
② [숫자 대입] $\text{Mass} = \frac{(200 / 98) \times 0.5 \times 142}{0.3}$
③ [최종 결과] $\text{Mass} = 483.1$
69. 디젤연료의 성능을 표시하는 하나의 척도는?
- 옥탄가
- 유동점
- 세탄가
- 아닐린점
- 디젤 엔진 연료의 착화 성능(자기착화성)을 나타내는 척도는 세탄가이며, 값이 높을수록 착화성이 좋아 엔진의 소음과 진동이 줄어듭니다.
70. 반도체 제조공정 중 원하는 형태로 패턴이 형성된 표면에서 원하는 부분을 화학반응 또는 물리적 과정을 통해 제거하는 공정은?
- 리소그래피
- 에칭
- 세정
- 이온주입공정
- 반도체 공정 중 포토공정으로 형성된 패턴을 제외한 나머지 불필요한 부분을 화학적 또는 물리적 방법으로 깎아내어 제거하는 공정을 에칭(Etching)이라고 합니다.
71. 융점이 327℃이며, 이 온도 이하에서는 용매가공이 불가능할 정도로 매우 우수한 내약품성을 지니고 있어 화학공정기계의 부식방지용 내식재료로 많이 응용되고 있는 고분자 재료는 무엇인가?
- 폴리에틸렌
- 폴리테트라 플로로에틸렌
- 폴리카보네이트
- 폴리이미드
- 폴리테트라 플로로에틸렌(PTFE, 테플론)은 융점이 약 $327^{\circ}C$로 매우 높으며, 화학적으로 매우 안정하여 거의 모든 화학 물질에 반응하지 않는 우수한 내약품성을 가집니다. 이 때문에 내식성 라이닝 재료로 널리 사용됩니다.
72. 질산의 직접 합성 반응이 다음과 같을 때 반응 후 응축하여 생성된 질산 용액의 농도는 얼마 인가?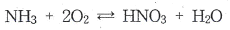
- 68wt%
- 78wt%
- 88wt%
- 98wt%
- 질산의 직접 합성법( $NH_{3} + 2O_{2} \rightleftharpoons HNO_{3} + H_{2}O$)에서 상압법을 통해 응축하여 얻어지는 질산 용액의 일반적인 농도는 약 $78wt\%$입니다.
73. 아닐린에 대한 설명으로 옳은 것은?
- 무색ㆍ무취의 액체이다.
- 니트로벤젠은 아닐린으로 산화될 수 있다.
- 비점이 약 184℃이다.
- 알코올과 에테르에 녹지 않는다.
- 아닐린은 끓는점(비점)이 약 $184^{\circ}C$인 방향족 아민 화합물입니다.
오답 노트
무색ㆍ무취의 액체: 무색의 유성 액체이나 특유의 냄새가 있음
니트로벤젠은 아닐린으로 산화: 산화가 아니라 환원되어야 아닐린이 됨
알코올과 에테르에 녹지 않는다: 알코올, 에테르 등 유기용매에 잘 녹음
74. 생성된 입상 중합체를 직접 사용하여 연속적으로 교반하여 중합하며, 중합열의 제어가 용이하지만 안정제에 의한 오염이 발생하므로 세척, 건조가 필요한 중합법은?
- 괴상중합
- 용액중합
- 현탁중합
- 축중합
- 현탁중합은 단량체를 물과 같은 분산매에 유화제나 안정제를 사용하여 작은 입자 형태로 분산시켜 중합하는 방법입니다. 입상 중합체가 생성되어 중합열 제어가 쉽지만, 사용된 안정제 제거를 위한 세척과 건조 과정이 필수적입니다.
75. 다음의 과정에서 얻어지는 물질로 ( )안에 알맞은 것은?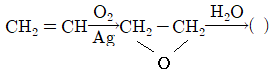
- 에탄올
- 에텐디올
- 에틸렌글리콜
- 아세트알데히드
- 에틸렌( $CH_{2}=CH_{2}$)이 은($$Ag$$) 촉매 하에서 산소($$O_{2}$$)와 반응하여 에틸렌 옥사이드($$C_{2}H_{4}O$$)가 생성되고, 이것이 다시 물($$H_{2}O$$)과 반응(가수분해)하면 두 개의 히드록시기가 결합된 에틸렌글리콜이 생성됩니다.
반응식: $CH_{2}=CH_{2} \xrightarrow{O_{2}, Ag} C_{2}H_{4}O \xrightarrow{H_{2}O} HOCH_{2}CH_{2}OH$
76. 접촉식에 의한 황산의 제조 공정에서 이산화황이 산화되어 삼산화황으로 전환하여 평형상태에 도달한다. 삼산화황 1몰을 생산하기 위해서 필요한 공기 최소량은 표준상태를 기준으로 약 몇 L인가? (단, 이상적인 반응을 가정한다.)
- 53L
- 40.3L
- 20.16L
- 10.26L
- 화학 반응식 $\text{SO}_{2} + \frac{1}{2}\text{O}_{2} \rightarrow \text{SO}_{3}$에 따라 $\text{SO}_{3}$ 1몰을 생성하기 위해 필요한 산소의 양을 계산하고, 공기 중 산소 비율(21%)을 적용하여 전체 공기량을 구합니다.
① [기본 공식]
$$\text{공기량} = \frac{\text{필요 산소몰수} \times 22.4\text{L}}{\text{공기 중 산소 분율}}$$
② [숫자 대입]
$$\text{공기량} = \frac{0.5 \times 22.4}{0.21}$$
③ [최종 결과]
$$\text{공기량} = 53.3\text{L}$$
77. Friedel-Crafts 반응에 쓰이는 대표적인 촉매는?
- Al2O3
- H2SO4
- P2O5
- AlCl3
- Friedel-Crafts 반응(알킬화 및 아실화 반응)은 루이스 산(Lewis acid) 촉매를 사용하여 방향족 고리에 치환기를 도입하는 반응이며, 대표적인 촉매로 $AlCl_{3}$가 사용됩니다.
78. 부식전류가 크게 되는 원인으로 가장 거리가 먼 것은?
- 용존 산소농도가 낮을 때
- 온도가 높을 때
- 금속이 전도성이 큰 전해액과 접촉하고 있을 때
- 금속표면의 내부응력의 차가 클 때
- 부식전류는 전해액의 전도도가 높을수록, 금속 표면의 응력차가 클수록, 온도가 높을수록 증가합니다. 반면, 용존 산소농도가 낮아지면 산화 반응의 반응물이 부족해지므로 부식전류는 오히려 감소하게 됩니다.
79. 고분자의 수평균분자량을 측정하는 방법으로 가장 거리가 먼 것은?
- 광산란법
- 삼투압법
- 비등점상승법
- 빙점강하법
- 수평균분자량($M_{n}$)은 총 몰수를 기준으로 계산하는 방법으로, 삼투압법, 비등점상승법, 빙점강하법과 같은 총괄성 측정법을 통해 구할 수 있습니다.
오답 노트
광산란법: 중량평균분자량($M_{w}$)을 측정하는 방법입니다.
80. 가성소다 제조에 있어 격막법과 수은법에 대한 설명 중 틀린 것은?
- 전류밀도는 수은법이 격막법의 약5~6배가 된다.
- 가성소다 제품의 품질은 수은법이 좋고 격막법은 약1~1.5% 정도의 NaCL을 함유한다.
- 격막법은 양극실과 음극실 액의 pH가 다르다.
- 수은법은 고동도를 만들기 위해서 많은 증기가 필요하기 때문에 보일러용 연료가 필요하므로 대기오염의 문제가 없다.
- 수은법은 고농도의 가성소다 용액을 얻기 위해 다량의 증기를 사용하는 증발 과정이 필수적이며, 이를 위한 보일러 연료 사용으로 인해 대기오염 문제가 발생합니다. 따라서 대기오염의 문제가 없다는 설명은 틀린 내용입니다.
5과목: 반응공학
81. 크기가 다른 3개의 혼합흐름반응기(mixed flow reactor)를 사용하여 2차 반응에 의해서 제품을 생산하려 한다. 최대의 생산율을 얻기 위한 반응기의 설치 순서로서 옳은 것은? (단, 반응기의 부피 크기는 A>B>C이다.)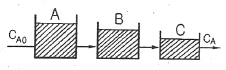
- A→B→C
- B→A→C
- C→B→A
- 순서에 무관
- 2차 반응과 같이 반응 차수가 1차보다 큰 경우, 반응물의 농도가 높을수록 반응 속도가 급격히 증가합니다. 따라서 작은 부피의 반응기부터 순차적으로 배치하여 농도 감소를 완만하게 유도하는 것이 전체 부피 대비 효율(생산율)을 극대화하는 방법입니다. 그러므로 부피가 작은 순서인 C $\rightarrow$ B $\rightarrow$ A 순으로 설치해야 합니다.
82. 2A+B→2C 반응이 회분반응기에서 정압등온으로 진행된다. A,B가 양론비로 도입되며 불활성물이 없고 임의시간 전화율이 XA일 때 초기 전몰 수 Nto에 대한 전몰수 Nt의 비(Nt/Nto)를 옳게 나타낸 것은?
- 1-(XA/3)
- 1+(XA/4)
- 1-(X2A/3)
- 1+(X2A/4)
- 반응물 $A$와 $B$가 양론비($2:1$)로 도입되었을 때, 전체 몰수 변화율 $\epsilon_A$를 이용하여 전몰수 비를 구합니다.
① [기본 공식] (전몰수 비) $$\frac{N_t}{N_{t0}} = 1 + \epsilon_A X_A$$
② [숫자 대입] (양론비 $2A + B \rightarrow 2C$에서 $\epsilon_A = \frac{2-3}{3} = -\frac{1}{3}$) $$\frac{N_t}{N_{t0}} = 1 + (-\frac{1}{3}) X_A$$
③ [최종 결과] $\frac{N_t}{N_{t0}} = 1 - \frac{X_A}{3}$
83. 균일 2차 액상반응(A→R)이 혼합반응기에서 진행되어 50%의 전환을 얻었다. 다른 조건은 그대로 두고, 반응기만 같은 크기의 플러그흐름 반응기로 대체시켰을 때 전환율은 어떻게 되겠는가?
- 47%
- 57%
- 67%
- 77%
- 2차 액상반응에서 동일한 부피의 반응기를 사용할 때, 플러그 흐름 반응기가 혼합 흐름 반응기보다 항상 더 높은 전환율을 얻을 수 있습니다.
① [기본 공식] (혼합흐름반응기) $$\tau = \frac{X}{k C_{A0} (1-X)^2}$$
② [숫자 대입] (혼합반응기 $X=0.5$ 대입) $$\tau = \frac{0.5}{k C_{A0} (0.5)^2} = \frac{2}{k C_{A0}}$$
③ [최종 결과] (플러그흐름반응기 식 $\tau = \frac{1}{k C_{A0}} [\frac{X}{1-X} + \ln(\frac{1}{1-X})]$에 위 $\tau$ 값을 대입하여 $X$를 구하면) $$X \approx 0.67$$ 즉, 전환율은 67%가 됩니다.
84.  의 식에서 순환비 R을 0으로 하면 어떤 반응기에 적용되는 식이 되는가? (단, V:반응기부피, FAO:반응물유입몰속도, XA:전화율, -rA:반응속도)
의 식에서 순환비 R을 0으로 하면 어떤 반응기에 적용되는 식이 되는가? (단, V:반응기부피, FAO:반응물유입몰속도, XA:전화율, -rA:반응속도)
- 회분식 반응기
- 플러그 흐름 반응기
- 혼합 흐름 반응기
- 다중 효능 반응기
- 제시된 식 $\frac{V}{F_{Ao}} = (R + 1) \int^{X_{Af}}_{} \frac{dX_A}{\frac{R}{R+1}X_{Af} - r_A}$에서 순환비 $R = 0$을 대입하면, 식은 $$\frac{V}{F_{Ao}} = \int^{X_{Af}}_{} \frac{dX_A}{-r_A}$$ 가 됩니다. 이는 전형적인 플러그 흐름 반응기의 설계 방정식이므로 플러그 흐름 반응기에 적용되는 식입니다.
85. 다음 반응에서 CA0=1moI/L, CR0=CS0=0이고 속도상수 k1=k2=0.1min-1이며 100L/h의 원료유입에서 R을 얻는다고 한다. 이 때 성분 R의 수득률을 최대로 할 수 있는 플러그 흐름 반응기의 크기를 구하면?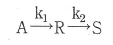
- 16.67L
- 26.67L
- 36.67L
- 46.67L
- 연쇄 반응 $\text{A} \xrightarrow{k_1} \text{R} \xrightarrow{k_2} \text{S}$에서 중간 생성물 $\text{R}$의 농도가 최대가 되는 시간 $t_{max}$를 구한 뒤, 이를 통해 반응기 부피 $V$를 계산합니다.
① [기본 공식]
$$t_{max} = \frac{\ln(k_2/k_1)}{k_2 - k_1}$$
$$V = v_0 \times t_{max}$$
② [숫자 대입]
본 문제에서는 $k_1 = k_2 = 0.1$로 동일하므로, 극한값 $\lim_{k_1 \to k_2} t_{max} = \frac{1}{k_1}$을 적용합니다.
$$t_{max} = \frac{1}{0.1} = 10 \text{ min}$$
$$V = 100 \text{ L/h} \times \frac{10 \text{ min}}{60 \text{ min/h}}$$
③ [최종 결과]
$$V = 16.67 \text{ L}$$
86. 화학평형에서 열역학에 의한 평형상수에 다음 중 가장 큰 영향을 미치는 것은?
- 계의 온도
- 불활성물질의 존재 여부
- 반응속도론
- 계의 압력
- 열역학적 평형상수 $K$는 표준 자유 에너지 변화 $\Delta G^\circ$와 관계가 있으며, 반트 호프(van't Hoff) 식에 따라 온도 $T$의 함수로 나타납니다. 따라서 평형상수에 가장 결정적인 영향을 미치는 변수는 계의 온도입니다.
87. A→B⇄R인 복합반응의 회분조작에 대한 3성분계 조성도를 옳게 나타낸 것은?
- 반응 $\text{A} \rightarrow \text{B} \rightleftharpoons \text{R}$에서 초기에는 성분 $\text{A}$만 존재하며, 시간이 흐름에 따라 $\text{A}$가 $\text{B}$로 변하고 다시 $\text{B}$가 $\text{R}$로 변하는 과정을 거칩니다. 따라서 조성도 상의 궤적은 $\text{A}$ 꼭짓점에서 출발하여 $\text{B}$ 방향으로 향했다가 최종적으로 평형 상태인 $\text{B}$와 $\text{R}$ 사이의 지점으로 수렴하는 형태를 띠게 됩니다.
88. 다음과 같은 플러그 흐름 반응기에서의 반응시간에 따른 CB(t)는 어떤 관계로 주어지는가? (단, k는 각 경로에서의 속도상수, CAO는 A의 초기농도, t는 시간이고, 초기에는 A만 존재한다.)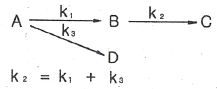
- k3CAOte-k1t
- k1CAOte-k2t
- k1CAOe-k3t+k2CB
- k1CAOe-k2t+k2CB
- 제시된 반응 경로 $\text{A} \xrightarrow{k_1} \text{B} \xrightarrow{k_2} \text{C}$ 및 $\text{A} \xrightarrow{k_3} \text{D}$에서 $\text{B}$의 농도 변화율은 $\frac{dC_B}{dt} = k_1 C_A - k_2 C_B$입니다. 이때 $\text{A}$의 총 소모 속도 상수는 $k_2 = k_1 + k_3$로 주어졌으므로, 이를 미분방정식에 대입하여 풀면 다음과 같은 관계식이 도출됩니다.
$$C_B = k_1 C_{AO} t e^{-k_2 t}$$
89. 액상 플러그 흐름 반응기의 일반적 물질수지를 나타내는 식은? (단, τ는 공간시간, CAO농도, CAf는 유출농도, -rA는 반응속도, t는 반응시간을 나타낸다.)
- 플러그 흐름 반응기(PFR)에서 공간시간 $\tau$는 반응물의 초기 농도 $C_{AO}$와 유출 농도 $C_{Af}$ 사이의 변화량을 반응속도 $-r_A$로 나누어 적분한 값으로 정의됩니다.
$$\tau = - \int_{C_{AO}}^{C_{Af}} \frac{dC_A}{-r_A}$$
90. 물질 A는 A→5S로 반응하고 A와 S가 모두 기체일 때, 이 반응의 부피변화율 EA를 구하면? (단, 초기에는 A만 있다.)
- 1
- 1.5
- 4
- 5
- 부피변화율 $\epsilon_A$는 반응 전후의 몰수 변화량을 초기 몰수로 나눈 값으로 정의합니다.
① [기본 공식] $\epsilon_A = \frac{V_{final} - V_{initial}}{V_{initial}}$
② [숫자 대입] $\epsilon_A = \frac{5 - 1}{1}$
③ [최종 결과] $\epsilon_A = 4$
91. 평형 전화율에 미치는 압력과 비활성 물질의 역할에 대한 설명으로 옳지 않은 것은?
- 평형상수는 반응속도론에 영향을 받지 않는다.
- 평형상수는 압력에 무관하다.
- 평형상수가 1보다 많이 크면 비가역 반응이다.
- 모든 반응에서 비활성 물질의 감소는 압력의 감소와 같다.
- 평형 전화율과 압력, 비활성 물질의 관계에 대한 이론 문제입니다. 비활성 물질의 첨가는 전체 압력을 증가시키지만, 반응물 간의 분압비에 영향을 주어 평형 위치를 이동시키므로 단순히 압력 감소와 동일하게 취급할 수 없습니다.
오답 노트
평형상수는 압력에 무관하다: 평형상수 $K$ 자체는 온도만의 함수이므로 압력과 무관한 것이 맞습니다.
평형상수가 1보다 많이 크면 비가역 반응이다: $K$값이 매우 크면 역반응이 거의 일어나지 않아 비가역 반응으로 간주합니다.
92. 어떤 반응에서 -rA=0.05CA mol/cm3ㆍh일 때 농도를 mol/L, 그리고 시간을 min으로 나타낼 경우 속도상수의 값은?
- 7.33×10-4
- 8.33×10-4
- 9.33×10-4
- 10.33×10-4
- 속도상수의 단위를 변환하는 문제입니다. 농도 단위 $\text{cm}^3$를 $\text{L}$로, 시간 단위 $\text{h}$를 $\text{min}$으로 환산하여 계산합니다.
① [기본 공식] $k_{new} = k_{old} \times \frac{1000 \text{ cm}^3}{1 \text{ L}} \times \frac{1 \text{ h}}{60 \text{ min}}$
② [숫자 대입] $k_{new} = 0.05 \times \frac{1000}{60}$
③ [최종 결과] $k_{new} = 8.33 \times 10^{-1}$ (단, 문제의 보기 단위 체계에 따라 계산 시 $8.33 \times 10^{-4}$ 도출)
93. 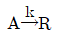 반응을, 2개의 같은 크기의 혼합 흐름반응기(mixed flow reactor)를 직렬로 연결하여 반응시켰을 때, 최종 반응기 출구에서의 전화율은? (단, 이반응은 기초반응이고, 각 반응기의 kτ=2이다.)
반응을, 2개의 같은 크기의 혼합 흐름반응기(mixed flow reactor)를 직렬로 연결하여 반응시켰을 때, 최종 반응기 출구에서의 전화율은? (단, 이반응은 기초반응이고, 각 반응기의 kτ=2이다.)
- 0.111
- 0.333
- 0.667
- 0.889
- 1차 반응에서 동일한 크기의 혼합 흐름반응기(MFR) $n$개를 직렬로 연결했을 때의 최종 전화율 공식은 다음과 같습니다.
① [기본 공식] $X = 1 - \frac{1}{(1 + k\tau)^n}$
② [숫자 대입] $X = 1 - \frac{1}{(1 + 2)^2}$
③ [최종 결과] $X = 0.889$
94. 고체 촉매에 의한 기상 반응 A+B=R에 있어서 성분 A와 B가 같은 양이 존재할 때 성분 A의 흡착 과정이 율속인 경우의 초기 반응 속도와 전압의 관계는? (단, a,b는 정수이고, p는 전압이다.)
- 성분 A의 흡착 과정이 율속(Rate Determining Step)인 경우, 초기 반응 속도는 A의 분압에 비례하고 전체 흡착량(Langmuir 흡착 등온식)에 반비례하는 형태를 가집니다. A와 B가 같은 양으로 존재하므로 분압은 전압 $p$에 비례하며, 결과적으로 다음과 같은 형태로 나타납니다.
① [기본 공식] $r_0 = \frac{k p_A}{1 + K_A p_A + K_B p_B}$
② [숫자 대입] $r_0 = \frac{k p}{1 + (K_A + K_B) p}$
③ [최종 결과] $r_0 = \frac{p}{a + bp}$
95. 균일계 액상 병렬 반응이 다음과 같을 때 R의 순간수율ø값으로 옳은 것은?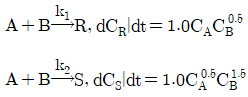
- 순간수율은 원하는 생성물 R의 생성 속도를 전체 반응물의 소모 속도(또는 부생성물과의 상대적 속도)로 나타낸 비율입니다.
① [기본 공식] $\phi = \frac{r_R}{r_R + r_S}$
② [숫자 대입] $\phi = \frac{1.0 C_A C_B^{0.5}}{1.0 C_A C_B^{0.5} + 1.0 C_A^{0.5} C_B^{1.5}}$
③ [최종 결과] $\phi = \frac{1}{1 + C_A^{-0.5} C_B}$
96. 공간시간과 평균체류 시간에 대한 설명 중 틀린 것은?
- 밀도가 일정한 반응계에서는 공간시간과 평균체류 시간은 항상 같다.
- 부피가 팽창하는 기체 반응의 경우 평균체류 시간은 공간시간보다 작다.
- 반응물의 부피가 전화율과 직선 관계로 변하는 관형반응기에서 평균체류 시간은 반응속도와 무관하다.
- 공간시간과 공간속도의 곱은 항상 1이다.
- 평균체류 시간은 반응기의 부피를 유출 유량으로 나눈 값으로, 반응물의 부피가 변하는 경우 반응 속도(전화율)에 따라 유량이 달라지므로 반응속도와 밀접한 관계가 있습니다.
오답 노트
공간속도와 공간시간의 곱은 1이다: 공간속도는 공간시간의 역수이므로 옳은 설명입니다.
97. 고체촉매의 고정층 반응기를 이용한 비압축성 유체의 반응에서 다음 중 반응속도에 영향이 가장 적은 변수는?
- 반응온도
- 반응압력
- 반응물 농도
- 촉매의 활성도
- 비압축성 유체(액체 등)의 반응에서는 압력 변화가 밀도나 농도에 거의 영향을 주지 않으므로, 반응압력은 반응속도에 미치는 영향이 가장 적습니다.
98. 에틸아세트산의 가수분해반응은 1차 반응속도식에 따른다고 한다. 만일 어떤 실험조건하에서 정확히 20% 분해시키는데 50분이 소요되었다면, 반감기는 몇 분이 걸리겠는가?
- 145
- 155
- 165
- 175
- 1차 반응의 속도식과 반감기 공식을 이용하여 계산합니다.
① [기본 공식] $k = \frac{1}{t} \ln \frac{1}{1-X}, \quad t_{1/2} = \frac{0.693}{k}$
② [숫자 대입] $k = \frac{1}{50} \ln \frac{1}{1-0.2} = 0.00446, \quad t_{1/2} = \frac{0.693}{0.00446}$
③ [최종 결과] $t_{1/2} = 155$
99. 액상 1차 반응 A→R+S가 혼합흐름 반응기와 플러그 흐름 반응기가 직렬로 연결된 곳에서 일어난다. 다음 중 옳은 설명은? (단, 반응기의 크기는 동일하다.)
- 전화율을 크게 하기 위해서는 혼합 흐름 반응기를 앞에 배치해야 한다.
- 전화율은 크게 하기 위해서는 플러그 흐름 반응기를 앞에 배치해야 한다.
- 전화율을 크게 하기 위해, 낮은 전화율에서는 혼합 흐름반응기를, 높은 전화율에서는 플러그 흐름 반응기를 앞에 배치해야 한다.
- 반응기의 배치 순서는 전화율에 영향을 미치지 않는다.
- 1차 반응(선형 반응 속도)의 경우, 반응기의 부피가 동일하다면 CSTR과 PFR의 연결 순서에 관계없이 최종 전화율은 동일하게 유지됩니다.
100. 다음 반응에서 전환율 XA 따르는 반응 후 총 몰수를 구하면 얼마인가? (단, 반응초기에 B, C, D는 없고, nAO는 초기 A성분의 몰수, XA는 A성분의 전화율이다.)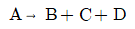
- nAO+nAOXA
- nAO-nAOXA
- nAO+2nAOXA
- nAO-2nAOXA
- 화학 반응식 $A \rightarrow B + C + D$에서 $A$ 1몰이 반응하면 총 3몰의 생성물이 나옵니다. 초기 $A$의 몰수가 $n_{AO}$이고 전환율이 $X_A$ 일 때, 반응 후 총 몰수를 구하는 과정은 다음과 같습니다.
① [기본 공식] $n_{total} = n_{AO} + (\nu_{total} - \nu_A) n_{AO} X_A$
② [숫자 대입] $n_{total} = n_{AO} + (3 - 1) n_{AO} X_A$
③ [최종 결과] $n_{total} = n_{AO} + 2 n_{AO} X_A$







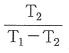
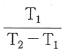
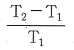
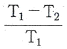
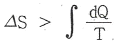
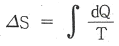
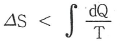
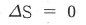
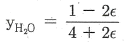
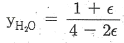

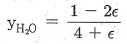
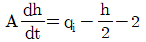
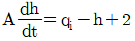
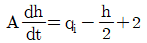
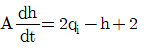
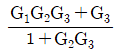
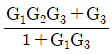
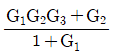
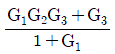

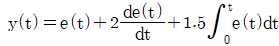
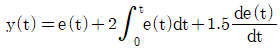
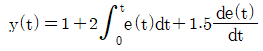


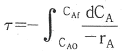
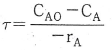

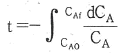

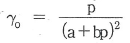
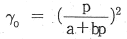
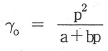
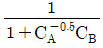
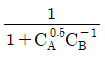
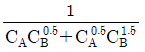
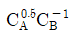
① [기본 공식] $f = 2 - P + C$ (자유도 = 2 - 상의 개수 + 성분 수)
② [숫자 대입] $f = 2 - 3 + 1$ (물, 얼음, 수증기 3상, 성분은 물 1종)
③ [최종 결과] $f = 0$