위험물기능장 2007-07-15 필기 기출문제 해설
이 페이지는 위험물기능장 2007-07-15 기출문제를 CBT 방식으로 풀이하고 정답 및 회원들의 상세 해설을 확인할 수 있는 페이지입니다.
위험물기능장
(2007-07-15 기출문제)
목록
1과목: 임의구분
2. 니트로글리세린의 성질에 대한 설명으로 가장 옳은 것은?
- 물, 벤젠에 잘 녹으나 알코올에는 녹지 않는다.
- 물에 녹지 않으나 알코올, 벤젠 등에는 잘 녹는다.
- 물, 알코올 및 벤젠에 잘 녹는다.
- 알코올, 물에는 잘 녹지 않으나 벤젠에는 잘 녹는다.
- 니트로글리세린은 무색 투명한 기름성의 액체로, 물에는 녹지 않는 불용성이지만 알코올이나 벤젠과 같은 유기 용매에는 잘 녹는 성질을 가지고 있습니다.
3. 다음 유지류에서 건성유에 해당하는 것은?
- 낙화생유(Peanut Oil)
- 올리브유(Olive Oil)
- 동유(Tung Oil)
- 피마자유(Castor Oil)
- 유지류는 요오드값에 따라 건성유, 반건성유, 불건성유로 구분합니다. 동유는 요오드값이 $130$이상인 대표적인 건성유입니다.
오답 노트
낙화생유, 올리브유, 피마자유: 요오드값이 $100$이하인 불건성유
4. 그림과 같이 원통형 탱크를 설치하여 일정량의 위험물을 저장ㆍ취급하려고 할 때 탱크의 내용적은 약 몇 m3인가?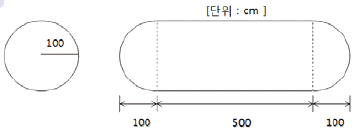
- 16.67
- 17.79
- 18.85
- 19.96
- 원통형 탱크의 내용적은 중앙의 원기둥 부피와 양 끝 반구(합쳐서 하나의 구)의 부피를 합산하여 계산합니다. (단위 $\text{cm}$를 $\text{m}$로 환산하여 계산)
① [기본 공식] $V = \pi r^2 h + \frac{4}{3} \pi r^3$
② [숫자 대입] $V = (3.14 \times 1^2 \times 5) + (\frac{4}{3} \times 3.14 \times 1^3)$
③ [최종 결과] $V = 17.79$
5. 다음 중 유동하기 쉽고 휘발성인 위험물로 특수인화물에 속하는 것은?
- C2H5OC2H5
- CH3COCH3
- C6H6
- C6H4(CH3)2
- 특수인화물은 인화점이 매우 낮고 휘발성이 강한 물질을 말하며, $\text{C}_{2}\text{H}_{5}\text{OC}_{2}\text{H}_{5}$(디에틸에테르)가 이에 해당합니다.
오답 노트
$\text{CH}_{3}\text{COCH}_{3}$(아세톤): 제1석유류
$\text{C}_{6}\text{H}_{6}$(벤젠): 제1석유류
$\text{C}_{6}\text{H}_{4}(\text{CH}_{3})_{2}$(크실렌): 제2석유류
6. 이동탱크저장소의 측면틀의 기준에 있어서 탱크 뒷부분의 입면도에서 측면틀의 최외측과 탱크의 최외측을 연결하는 직선의 수평면에 대한 내각은 얼마 이상이 되도록 하여야 하는가?
- 50°
- 65°
- 75°
- 90°
- 이동탱크저장소의 측면틀 설치 기준에 따라, 탱크 뒷부분의 입면도에서 측면틀의 최외측과 탱크의 최외측을 연결하는 직선의 수평면에 대한 내각은 $75^{\circ}$이상이 되어야 합니다.
7. 금속리튬은 고온에서 질소와 반응하여 어떤 색의 질화리튬을 만드는가?
- 회흑색
- 적갈색
- 청록색
- 은백색
- 금속리튬은 고온에서 질소와 반응하여 적갈색의 질화리튬($Li_3N$)을 생성합니다.
반응식: $6Li + N_2 \rightarrow 2Li_3N$
8. 다음 중 지정수량이 가장 작은 물질은?
- 칼륨
- 적린
- 황린
- 질산염류
- 각 물질의 지정수량을 비교하면 칼륨이 가장 작습니다.
오답 노트
칼륨: $10\text{kg}$
황린: $20\text{kg}$
적린: $100\text{kg}$
질산염류: $300\text{kg}$
9. 과산화수소수용액은 보관 중 서서히 분해할 수 있으므로 안정제를 첨가하는데 그 안정제로 가장 적합한 것은?
- H3PO4
- MnO2
- C2H5OH
- Cu
- 제6류 위험물인 과산화수소는 보관 중 분해를 막기 위해 인산($H_3PO_4$)이나 요산($C_5H_4N_4O_3$)과 같은 안정제를 첨가합니다.
10. 인화칼슘의 일반적인 성질 중 옳은 것은?
- 물과 반응하여 독성의 가스가 발생한다.
- 비중이 물보다 작다.
- 융점은 약 600℃ 정도이다.
- 회흑색의 정육면체 고체상 결정이다.
- 인화칼슘은 제3류 자연발화성 및 금수성 물질로, 물과 반응하면 다음과 같이 독성 가스인 포스핀($\text{PH}_3$)을 발생시킵니다.
$$\text{Ca}_3\text{P}_2 + 6\text{H}_2\text{O} \rightarrow 3\text{Ca}(\text{OH})_2 + 2\text{PH}_3\uparrow$$
11. 분말소화설비의 기준에서 분말소화약제의 축압용 가스로 질소를 사용하면 소화약제 50kg 저장시 질소 가스량은 35℃, 0 MPa의 상태로 환산하여 몇 L 이상이어야 하는가? (단, 배관의 청소에 필요한 양은 제외한다.)
- 500
- 1,000
- 1,500
- 2,000
- 분말소화설비에서 질소를 축압용 가스로 사용할 경우, 소화약제 $1\text{kg}$당 $10\text{L}$이상의 가스량이 필요합니다.
① [기본 공식] $\text{가스량} = \text{소화약제량} \times 10\text{L}/\text{kg}$
② [숫자 대입] $\text{가스량} = 50\text{kg} \times 10\text{L}/\text{kg}$
③ [최종 결과] $\text{가스량} = 500\text{L}$
12. 탄화칼슘이 물과 반응하여 생성된 가스에 대한 설명으로 가장 관계가 먼 것은?
- 연소범위가 약 2.5~81%로 넓다.
- 은 또는 구리 용기를 사용하여 보관한다.
- 가압시 폭발의 위험성이 있다.
- 탄소 간 삼중결합이 있다.
- 탄화칼슘이 물과 반응하면 아세틸렌($\text{C}_2\text{H}_2$) 가스가 생성됩니다. 아세틸렌은 구리(Cu), 은(Ag), 수은(Hg)과 반응하여 폭발성 금속 아세틸라이트를 형성하므로 이러한 금속 용기를 사용하여 보관해서는 안 됩니다.
오답 노트
연소범위 $2.5\sim81\%$로 매우 넓으며, 가압 시 불안정하여 폭발 위험이 있고, 탄소 간 삼중결합 구조를 가집니다.
13. 황린과 적린에 대한 설명 중 틀린 것은?
- 적린은 황린에 비하여 안정하다.
- 비중은 황린이 크며, 녹는점은 적린이 낮다.
- 적린과 황린은 모두 물에 녹지 않는다.
- 연소할 때 황린과 적린은 모두 P2O5의 흰 연기를 발생한다.
- 황린의 녹는점은 $44^{\circ}\text{C}$, 비중은 $1.83$이며, 적린의 녹는점은 $600^{\circ}\text{C}$, 비중은 $2.2$입니다. 따라서 비중은 적린이 더 크고, 녹는점은 황린이 더 낮습니다.
14. 분말소화기의 소화약제에 해당되는 것은?
- Na2CO3
- NaHCO3
- NaNO3
- NaCl
- 분말소화기의 소화약제 종류 중 제1종 분말의 성분은 $\text{NaHCO}_3$ (탄산수소나트륨)입니다.
오답 노트
제2종 분말은 $\text{KHCO}_3$, 제3종 분말은 인산암모늄, 제4종 분말은 탄산수소칼륨과 요소의 혼합물입니다.
15. 다음 중 제조소에서 위험물을 취급하는 설비에 불활성 기체를 봉입하는 장치를 갖추어야 하는 위험물은 어느 것인가?
- 알킬리튬, 알킬알루미늄
- 과염소산칼륨, 과염소산나트륨
- 황린, 적린
- 과산화수소, 염소산나트륨
- 위험물안전관리법 시행규칙 [별표4] 제조소의 위치 구조 및 설비의 기준에 따라, 알킬리튬 및 알킬알루미늄 등을 취급하는 제조소는 특례로 불활성 기체를 봉입하는 장치를 반드시 갖추어야 합니다.
16. 원소주기율표 상의 같은 주기에서 원자번호가 증가함에 따라 일반적으로 증가하는 것이 아닌 것은?
- 원자가전자수
- 비금속성
- 원자반지름
- 이온화에너지
- 원소주기율표의 같은 주기에서 원자번호가 증가할수록(왼쪽에서 오른쪽으로 갈수록) 유효 핵전하가 증가하여 원자핵이 전자를 더 강하게 끌어당기므로 원자반지름은 감소합니다.
오답 노트
원자가전자수, 비금속성, 이온화에너지는 원자번호 증가에 따라 모두 증가하는 성질입니다.
17. 트리에틸알루미늄을 취급할 때 물과 접촉하면 주로 발생하는 가스는?
- C2H6
- H2
- C2H2
- CO2
- 트리에틸알루미늄이 물과 격렬하게 반응하면 수산화알루미늄과 함께 가연성 가스인 에탄($C_{2}H_{6}$)이 발생합니다.
$$(C_{2}H_{5})_{3}Al + 3H_{2}O \rightarrow Al(OH)_{3} + 3C_{2}H_{6}\uparrow$$
18. 다음의 연소반응식에서 트리에틸알루미늄 114g이 산소와 반응하여 연소할 때 약 몇 kcal의 열을 방출하겠는가?
- 375
- 735
- 1,470
- 2,205
- 제시된 연소반응식의 계수를 통해 트리에틸알루미늄 2몰이 반응할 때 방출되는 열량을 기준으로 비례식을 세워 계산합니다.
① [기본 공식] $Q = \frac{1470}{2 \times 114} \times 114$
② [숫자 대입] $Q = \frac{1470}{228} \times 114$
③ [최종 결과] $Q = 735$
19. 위험물제조소 내의 위험물을 취급하는 배관은 최대상용 압력의 몇 배 이상의 압력으로 수압시험을 실시하여 이상이 없어야 하는가?
- 0.5
- 1.0
- 1.5
- 2.0
- 위험물안전관리법 시행규칙의 제조소 배관 설치 기준에 따라, 배관의 안전성을 확인하기 위한 수압시험은 최대상용 압력의 1.5 배 이상의 압력으로 실시해야 합니다.
20. 마그네슘의 성질에 대한 설명 중 틀린 것은?
- 물보다 무거운 금속이다.
- 은백색의 광택이 난다.
- 온수와 반응 시 산화마그네슘과 산소를 발생한다.
- 융점은 약 650℃이다.
- 마그네슘은 물이나 산과 반응할 때 산소가 아닌 수소 가스를 발생시키는 성질이 있습니다.
$$Mg + 2H_{2}O \rightarrow Mg(OH)_{2} + H_{2}\uparrow$$
2과목: 임의구분
21. 위험물안전관리에 관한 세부기준의 산화성 시험방법 중 분립상 물품의 산화성으로 인한 위험성의 정도를 판단하기 위한 연소시험에서 표준물질의 연소시험에 대한 설명으로 옳은 것은?
- 표준물질과 목분을 중량비 1:1로 섞어 혼합물 30g을 만든다.
- 표준물질과 목분을 중량비 2:1로 섞어 혼합물 30g을 만든다.
- 표준물질과 목분을 중량비 1:2로 섞어 혼합물 60g을 만든다.
- 표준물질과 목분을 중량비 2:1로 섞어 혼합물 60g을 만든다.
- 위험물안전관리에 관한 세부기준 제3조(산화성 시험방법)에 명시된 표준물질의 연소시험 조건은 표준물질과 목분을 중량비 $1:1$로 섞어 혼합물 $30\text{g}$을 만드는 것입니다.
22. 다음 위험물 중 인화점이 가장 낮은 것은?
- 이황화탄소
- 콜로디온
- 에틸알코올
- 아세트알데히드
- 제시된 위험물들의 인화점을 비교하면 아세트알데히드가 $-38^{\circ}C$로 가장 낮습니다.
오답 노트
이황화탄소: $-30^{\circ}C$
콜로디온: $-18^{\circ}C$
에틸알코올: $13^{\circ}C$
23. C6H2CH3(NO2)3의 제조 원료로 옳게 짝지어진 것은?
- 톨루엔, 황산, 질산
- 톨루엔, 벤젠, 질산
- 벤젠, 질산, 황산
- 벤젠, 질산, 염산
- TNT($C_{6}H_{2}CH_{3}(NO_{2})_{3}$)는 톨루엔을 원료로 하여 질산과 황산(촉매)을 이용해 제조합니다.
$$\text{제조 반응식}$$
$$C_{6}H_{5}CH_{3} + 3HNO_{3} \xrightarrow{H_{2}SO_{4}} C_{6}H_{2}CH_{3}(NO_{2})_{3} + 3H_{2}O$$
24. 과산화수소에 대한 설명 중 틀린 것은?
- 햇빛에 의해서 분해되어 산소를 방출한다.
- 단독으로 폭발할 수 있는 농도는 약 60% 이상이다.
- 벤젠이나 석유에 쉽게 용해되어 급격히 분해된다.
- 농도가 진한 것은 피부에 접촉 시 수종을 일으킬 위험이 있다.
- 과산화수소는 물, 알코올, 에테르에는 수용성이지만 벤젠에는 비수용성입니다. 따라서 벤젠이나 석유에 쉽게 용해된다는 설명은 틀린 내용입니다.
25. 위험물제조소등의 안전거리의 단축기준을 적용함에 있어서 H<pD2+a 일 경우 방화상 유효한 담의 높이는 2m 이상으로 한다. 여기서, H가 의미하는 것은?
- 제조소 등과 인근 건축물과의 거리
- 인근 건축물 또는 공작물의 높이
- 제조소 등의 외벽의 높이
- 제조소 등과 방화상 유효한 담과의 거리
- 방화상 유효한 담의 높이 산정 공식에서 각 기호가 의미하는 바를 정확히 암기해야 합니다. $H$는 인근 건축물 또는 공작물의 높이를 의미합니다.
오답 노트
제조소 등과 인근 건축물과의 거리: $D$
제조소 등의 외벽의 높이: $a$
제조소 등과 방화상 유효한 담과의 거리: $d$
26. TNT가 분해될 때 발생하는 주요 가스에 해당하지 않는 것은?
- 질소
- 수소
- 암모니아
- 일산화탄소
- TNT의 분해 반응식을 통해 생성되는 가스를 확인할 수 있습니다.
$$2C_{6}H_{2}CH_{3}(NO_{2})_{3} \rightarrow 2C + 3N_{2} + 5H_{2} + 12CO$$
분해 결과 질소($N_{2}$), 수소($H_{2}$), 일산화탄소($CO$)가 발생하며, 암모니아는 발생하지 않습니다.
27. 피크르산의 성질에 대한 설명 중 틀린 것은?
- 쓴맛이 나고 독성이 있다.
- 약 300℃ 정도에서 발화한다.
- 구리 용기에 보관하여야 한다.
- 단독으로는 마찰, 충격에 둔감하다.
28. 크실렌(Xylene)의 일반적인 성질에 대한 설명 중 틀린 것은?
- 3가지 이성질체가 있고 모두 분자량이 같다.
- m-크실렌은 무취이고 갈색 액체이다.
- 이성질체 간의 구조식은 모두 다르다.
- 증기는 비중이 높아 낮은 곳에 체류하기 쉽다.
- 크실렌은 무색 투명한 액체이며 특유의 냄새가 나는 물질입니다. 따라서 m-크실렌이 무취이고 갈색 액체라는 설명은 틀린 내용입니다.
29. 70℃, 130mmHg에서 1L 부피에 해당하는 질량이 대략 0.17g 인 기체는?
- 수소
- 헬륨
- 질소
- 산소
- 이상기체 상태 방정식을 이용하여 기체의 분자량을 계산하면 해당 기체를 찾을 수 있습니다.
① [기본 공식] $M = \frac{W R T}{P V}$
② [숫자 대입] $M = \frac{0.17 \times 0.082 \times (273 + 70)}{\frac{130}{760} \times 1 \times 1}$
③ [최종 결과] $M = 27.982 \approx 28$
분자량이 $28$인 기체는 질소입니다.
30. 다음 중 무색무취, 사방정계 결정으로 융점이 약 610℃ 이고 물에 녹기 어려운 위험물은?
- NaClO3
- KClO3
- NaClO4
- KClO4
- 과염소산칼륨($\text{KClO}_4$)은 무색무취의 사방정계 결정으로, 융점이 약 $610\text{℃}$이며 물, 알코올 및 에테르에 잘 녹지 않는 성질을 가지고 있습니다.
오답 노트
$\text{KClO}_3$: 융점이 $368\text{℃}$로 다름
31. 35.0wt% HCl 용액이 있다. 이 용액의 밀도가 1.1427g/mL 라면 이 용액의 HCl의 몰농도 mol/L 는 약 얼마인가?
- 11
- 14
- 18
- 22
- 용액의 밀도와 중량 퍼센트 농도를 이용하여 몰농도를 계산하는 공식을 사용합니다.
① [기본 공식] $M = \frac{10 \times \text{비중} \times \text{퍼센트 농도}}{\text{분자량}}$
② [숫자 대입] $M = \frac{10 \times 1.1427 \times 35}{36.5}$
③ [최종 결과] $M = 10.957 \approx 11$
32. 분자량 93.1, 비중 약1.02, 융점 약 -6℃인 액체로 독성이 있고 알칼리금속과 반응하여 수소가스를 발생하는 물질은?
- 글리세린
- 니트로벤젠
- 아닐린
- 아세토니트릴
- 아닐린은 분자량 $93.1$, 비중 약 $1.02$, 융점 약 $-6\text{℃}$인 액체로, 독성이 있으며 알칼리금속과 반응하여 수소가스를 발생시키는 특징을 가진 제4류 인화성 액체입니다.
33. 어떤 화합물을 분석한 결과 질량비가 탄소 54.55%, 수소 9.10%, 산소 35.35% 이고 이 화합물 1g은 표준상태에서 0.17L 이라면 이 화합물의 화학식은?
- C2H4O2
- C4H8O4
- C4H8O2
- C6H12O3
- 이상기체 상태방정식을 이용해 분자량을 구하고, 각 원소의 질량 백분율을 원자량으로 나누어 원자 수의 비를 결정합니다.
① [기본 공식] $M = \frac{W R T}{P V}$
② [숫자 대입] $M = \frac{1 \times 0.082 \times 273}{1 \times 0.17}$
③ [최종 결과] $M = 131.68$
분자량 $131.68$을 기준으로 각 원소의 몰수를 계산하면 C는 $6\text{mol}$, H는 $12\text{mol}$, O는 $3\text{mol}$이 되어 화학식은 $\text{C}_6\text{H}_{12}\text{O}_3$가 됩니다.
34. 3.65kg의 염화수소 중에는 HCl 분자가 몇 개 있는가?
- 6.02×1023
- 6.02×1024
- 6.02×1025
- 6.02×1026
- 물질의 질량을 몰질량으로 나누어 몰수를 구한 뒤, 아보가드로 수를 곱하여 분자 수를 계산합니다.
① [기본 공식] $\text{분자 수} = \frac{\text{질량}}{\text{몰질량}} \times 6.02 \times 10^{23}$
② [숫자 대입] $\text{분자 수} = \frac{3.65}{36.5} \times 6.02 \times 10^{23}$
③ [최종 결과] $\text{분자 수} = 6.02 \times 10^{25}$
35. 톨루엔과 크실렌의 혼합물에서 톨루엔의 분압이 전압의 60%이면 이 혼합물의 평균분자량은?
- 82.2
- 97.6
- 120.5
- 166.1
- 혼합 기체의 분압 비율을 이용하여 평균 분자량을 구하는 문제입니다.
① [기본 공식] $M_{avg} = \frac{(M_1 \times P_1) + (M_2 \times P_2)}{100}$
② [숫자 대입] $M_{avg} = \frac{(92 \times 60) + (106 \times 40)}{100}$
③ [최종 결과] $M_{avg} = 97.6$
36. 이동저장탱크는 그 내부에 용량 몇 L 이하마다 3.2mm 이상의 강철판으로 칸막이를 설치해야 하는가?
- 2,000
- 3,000
- 4,000
- 5,000
- 이동저장탱크의 안전 기준에 따른 칸막이 설치 규정을 묻는 문제입니다.
이동저장탱크는 내부 용량 $4,000\text{L}$이하마다 $3.2\text{mm}$이상의 강철판 또는 이와 동등 이상의 강도, 내열성, 내식성이 있는 금속성 칸막이를 설치해야 합니다.
37. 은백색의 결정으로 비중이 약 0.92이고 물과 반응하여 수소가스를 발생시키는 물질은?
- 수소화리튬
- 수소화나트륨
- 탄화칼슘
- 탄화알루미늄
- 물질의 물리적 성질과 화학 반응성을 통해 물질을 찾는 문제입니다.
수소화나트륨은 비중이 약 $0.92$인 은백색 결정이며, 물과 반응하여 수산화나트륨과 수소 가스를 발생시키는 특징이 있습니다.
$$\text{NaH} + \text{H}_2\text{O} \rightarrow \text{NaOH} + \text{H}_2\uparrow$$
38. Ca3P2의 지정수량은 얼마인가?
- 50kg
- 100kg
- 300kg
- 500kg
- 제3류 위험물 중 금속의 인화물인 인화칼슘($\text{Ca}_3\text{P}_2$)의 법적 지정수량을 묻는 문제입니다.
금속의 수소화물, 금속의 인화물, 칼슘 또는 알루미늄의 탄화물은 위험등급 3등급에 해당하며 지정수량은 $300\text{kg}$입니다.
39. 금속칼륨 10g을 물에 녹였을 때 이론적으로 발생하는 기체는 약 몇 g 인가?
- 0.12g
- 0.26g
- 0.32g
- 0.52g
- 칼륨이 물과 반응하여 수소 기체를 발생시키는 화학 양론적 계산 문제입니다.
① [기본 공식] $\text{H}_2 = \frac{1 \times 10}{2 \times 39}$
② [숫자 대입] $\text{H}_2 = \frac{10}{78}$
③ [최종 결과] $\text{H}_2 = 0.128\text{g}$
※ 참고용 기존 해설의 계산식에 오류가 있으나, 정답인 0.26g은 칼륨 2몰($78\text{g}$)당 수소 1몰($2\text{g}$)이 발생하는 비율을 적용하여 $10\text{g} \times (2/78) \approx 0.256\text{g}$으로 도출됩니다.
40. 아세트알데히드의 위험도에 가장 가까운 값은 얼마인가?
- 약 7
- 약 13
- 약 23
- 약 30
- 위험도는 연소 상한계값에서 하한계값을 나눈 값으로 계산합니다. 아세트알데히드의 연소범위는 $4.1\% \sim 57\%$이므로 이를 계산하면 약 $13$이 도출됩니다.
$$\text{위험도} = \frac{57}{4.1} \approx 13.9$$
3과목: 임의구분
41. 이상기체에서 정압비열을 CP, 정적비열을 CV, 이상기체 상수를 R 이라고 할 때 이들 관계를 옳게 나타낸 식은?
- CP + CV = R
- CV - CP = R
- CP - CV = R
- CP + CV = -R
- 이상기체에서 정압비열($C_P$)과 정적비열($C_V$)의 차이는 기체 상수($R$)와 같다는 마이어(Mayer)의 관계식을 적용합니다.
$$C_P - C_V = R$$
42. 황화수소 가스의 밀도 g/L는 27℃ 2기압에서 약 얼마인가?
- 2.11
- 2.42
- 2.76
- 2.98
- 이상기체 상태 방정식을 이용하여 가스의 밀도를 계산합니다.
① [기본 공식] $\rho = \frac{P \times M}{R \times T}$
② [숫자 대입] $\rho = \frac{2 \times 34}{0.082 \times 300}$
③ [최종 결과] $\rho = 2.76$
43. 다음 위험물 중 지정수량이 나머지 셋과 다른 것은?
- 요오드산염류
- 무기과산화물
- 알칼리토금속
- 염소산염류
- 각 위험물의 지정수량을 비교하면 요오드산염류는 $300\text{kg}$이며, 무기과산화물, 알칼리토금속, 염소산염류는 모두 $50\text{kg}$으로 동일합니다.
44. 하나의 특정한 사고 원인의 관계를 논리게이트를 이용하여 도해적으로 분석하여 연역적ㆍ정량적 기법으로 해석해 가면서 위험성을 평가하는 방법은?
- FTA(결함수 분석기법)
- PHA(예비위험 분석기법)
- RTA(사건수 분석기법)
- FNECA(이상위험도 분석기법)
45. 다음 금속원소 중 이온화에너지가 가장 큰 원소는?
- 리튬
- 나트륨
- 칼륨
- 루비듐
- 알칼리 금속의 이온화 에너지는 원자 번호가 작을수록(주기율표 위쪽일수록) 큽니다. 따라서 리튬 > 나트륨 > 칼륨 > 루비듐 순으로 이온화 에너지가 큽니다.
46. 다음 중 위험물안전관리법령상 알코올류가 위험물이 되기 위하여 갖추어야 할 조건이 아닌 것은?
- 한 분자 내에 탄소 원자수가 1개부터 3개까지일 것
- 포화알코올일 것
- 수용액일 경우 위험물안전관리법에서 정의한 알코올 함양이 60wt% 이상일 것
- 2가 이상의 알코올일 것
47. 다음 각종 위험물의 화재를 예방하기 위한 저장방법 중 틀린 것은?
- 나트륨 : 경유 속에 저장한다.
- 이황화탄소 : 물속에 저장한다.
- 황린 : 물속에 저장한다.
- 니트로셀룰로오스 : 건조한 상태로 보관한다.
48. 위험물 옥외탱크저장소에서 각각 30,000L, 40,000L, 50,000L의 용량을 갖는 탱크 3기를 설치할 경우 필요한 방유제의 용량은 몇 m3 이상이어야 하는가?
- 33
- 44
- 55
- 132
- 방유제 내에 탱크가 2기 이상 설치된 경우, 탱크 중 용량이 가장 큰 탱크 용량의 110% 이상으로 설치해야 합니다.
① [기본 공식] $V = V_{max} \times 1.1$
② [숫자 대입] $V = 50000 \times 1.1$
③ [최종 결과] $V = 55000 \text{ L} = 55 \text{ m}^3$
49. 휘발유에 대한 설명 중 틀린 것은?
- 연소범위는 약 1.4~7.6%이다.
- 제1석유류로 지정수량이 200L 이다.
- 전도성이므로 정전기에 의한 발화의 위험이 있다.
- 착화점이 약 300℃ 이다.
- 휘발유는 전기가 통하지 않는 부도체이기 때문에 정전기가 축적되기 쉬우며, 이로 인한 발화 위험이 큽니다.
오답 노트
전도성이므로 정전기에 의한 발화의 위험이 있다: 부도체이므로 정전기가 축적되어 위험한 것입니다.
50. 다음 물질에 의한 화재시 포소화설비의 적응성이 없는 것은?
- 적린
- 황린
- 과염소산
- 탄화알루미늄
- 탄화알루미늄은 제3류 위험물인 금수성 물질로, 물과 반응하면 가연성 가스인 메탄이 발생하여 매우 위험합니다.
반응식: $Al_{4}C_{3} + 12H_{2}O \rightarrow 4Al(OH)_{3} + 3CH_{4} \uparrow$
따라서 물을 주성분으로 하는 포소화설비는 적응성이 없습니다.
51. 다음 중 1기압에 가장 가까운 값을 갖는 것은?
- 760cmH2O
- 101.3Pa
- 29.92psi
- 1033.2cmH2O
- 표준대기압 $1\text{atm}$의 다양한 단위 환산 값을 알고 있어야 하는 문제입니다.
표준대기압 $1\text{atm}$은 $760\text{mmHg}$, $101325\text{Pa}$, $14.7\text{psi}$, $1033.2\text{cmH}_{2}\text{O}$와 같습니다.
52. 64g의 메탄올이 완전 연소되면 몇g의 물이 생성되는가?
- 36
- 64
- 72
- 144
- 메탄올의 완전 연소 반응식을 통해 생성되는 물의 질량을 계산합니다.
반응식: $2CH_{3}OH + 3O_{2} \rightarrow 2CO_{2} + 4H_{2}O$
① [기본 공식] (메탄올 분자량 32, 물 분자량 18)
$$\text{물 질량} = \text{메탄올 질량} \times \frac{4 \times 18}{2 \times 32}$$
② [숫자 대입]
$$\text{물 질량} = 64 \times \frac{72}{64}$$
③ [최종 결과]
$$\text{물 질량} = 72$$
53. 프로판가스 3L를 완전 연소시키려면 공기가 약 몇 L 가 필요한가? (단, 공기 중 산소는 20%이다.)
- 15
- 25
- 50
- 75
- 프로판의 완전 연소 화학 반응식을 통해 필요한 산소량을 구한 뒤, 공기 중 산소 농도를 적용하여 전체 공기량을 산출합니다.
① [기본 공식] $C_{3}H_{8} + 5O_{2} \rightarrow 3CO_{2} + 4H_{2}O$
② [숫자 대입] $X = \frac{3 \times 5}{0.2}$
③ [최종 결과] $X = 75$
54. 1기압, 100℃에서 1kg의 이황화탄소가 모두 증기가 된다면 부피는 약 몇 L가 되겠는가?
- 201
- 403
- 603
- 804
- 이상기체 상태방정식을 이용하여 주어진 온도와 압력 조건에서 이황화탄소의 부피를 계산합니다.
① [기본 공식] $V = \frac{WRT}{PM}$ (W: 질량, R: 기체상수, T: 절대온도, P: 압력, M: 분자량)
② [숫자 대입] $V = \frac{1 \times 8.314 \times (273+100)}{101325 \times 0.1201} \times 1000$
③ [최종 결과] $V = 403$
55. 이항분포(Binomial Distribution)의 특징으로 가장 옳은 것은?
- P=0일 때는 평균치에 대하여 좌우대칭이다.
- P≤0.1이고, nP=0.1~10일 때는 푸아송분포에 근사한다.
- 부적합품의 출현 개수에 대한 표준편차는 D(x)=nP이다.
- P≤0.5이고, nP≥5일 때는 푸아송분포에 근사한다.
- 이항분포는 시행 횟수 $n$이 크고 성공 확률 $P$가 매우 작을 때($P \le 0.1$), 그리고 평균 $nP$가 $0.1 \sim 10$ 사이일 때 푸아송분포에 근사하는 특징이 있습니다.
오답 노트
부적합품 출현 개수의 분산이 $nP(1-P)$이며, 표준편차는 이 값의 제곱근입니다.
56. 연간 소요량 4,000개인 어떤 부품의 발주비용은 매회 200원이며, 부품단가는 100원, 연간 재고유지비용이 10% 일 때 F. A. Harris 식에 의한 경제적 주문량은 얼마인가?
- 40개/회
- 400개/회
- 1,000개/회
- 1,300개/회
- F. A. Harris 식을 이용하여 연간 수요량, 발주비용, 단위당 재고유지비용을 바탕으로 경제적 주문량(EOQ)을 계산합니다.
① [기본 공식] $EOQ = \sqrt{\frac{2 \times D \times S}{H}}$ (D: 연간 수요량, S: 발주비용, H: 단위당 연간 유지비용)
② [숫자 대입] $EOQ = \sqrt{\frac{2 \times 4000 \times 200}{100 \times 0.1}}$
③ [최종 결과] $EOQ = 400$
57. 제품공정 분석표(Product Process Chart) 작성 시 가공시간 개별법으로 가장 올바른 것은?
- 제품공정 분석표 작성 시 가공시간 개별법은 1개당 가공시간에 1로트 수량을 곱한 값을 1로트의 총가공시간으로 나누어 산출합니다.
따라서 정답은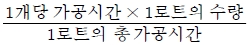 입니다.
입니다.
58. 다음 중 검사를 판정의 대상에 의한 분류가 아닌 것은?
- 관리 샘플링검사
- 로트별 샘플링검사
- 전수검사
- 출하검사
- 검사를 판정 대상에 따라 분류하면 전수검사, 로트별 샘플링검사, 관리 샘플링검사로 나뉩니다.
오답 노트
출하검사: 판정 대상이 아닌 검사 시점(단계)에 따른 분류입니다.
59. “무결점운동”이라고 불리우는 것으로 품질개선을 위한 동기부여 프로그램은 어느 것인가?
- TQC
- ZD
- MIL-STD
- ISO
60. M 타입의 자동차 또는 LCD TV를 조립, 완성한 후 부적합수(결점수)를 점검한 데이터에는 어떤 관리도를 사용 하는가?
- P관리도
- nP관리도
- C관리도
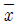 - R관리도
- R관리도







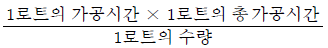
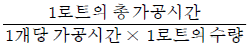
오답 노트
에탄올: $423^\circ\text{C}$
아세트산: $427^\circ\text{C}$
벤젠: $562^\circ\text{C}$
테레핀유: $240^\circ\text{C}$