1과목: 과목 구분 없음
1. 표는 25°C에서 물질 A~D에 대한 표준생성엔탈피(△Hf°)이다. 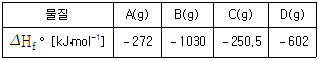
25°C에서 2mol의 A와 충분한 양의 B를 반응시킬 때, 다음 반응에 대한 표준반응엔탈피[kJ]는?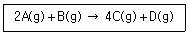
- -30
- -15
- 25
- 449.5
2. 베르누이식 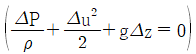 의 가정이 아닌 것은? (단, P는 압력, ρ는 밀도, u는 유체의 평균 유속, g는 중력가속도, z는 높이이다)
의 가정이 아닌 것은? (단, P는 압력, ρ는 밀도, u는 유체의 평균 유속, g는 중력가속도, z는 높이이다)
- 마찰 손실이 없음
- 축일이 없음
- 정상상태
- 압축성 유체
3. 화학공정의 개발 및 건설 과정을 시작부터 순서대로 바르게 나열한 것은?
- 기초연구→공정개발연구→공정 설계→플랜트 설계→플랜트 건설
- 공정개발연구→기초연구→공정 설계→플랜트 설계→플랜트 건설
- 기초연구→플랜트 설계→공정개발연구→공정 설계→플랜트 건설
- 공정 설계→기초연구→공정개발연구→플랜트 설계→플랜트 건설
4. 일정 시점에 기업이 보유하고 있는 자산, 부채, 자본의 구성 상태를 나타내는 재무제표는?
- 재무상태표
- 포괄손익계산서
- 현금흐름표
- 자본변동표
5. 100kPa, 60°C에서 상대습도가 80%인 습한 공기가 100molㆍh-1로 제습기에 들어간다. 제습기가 공기 중 수분의 62.5%를 응축시킬 때, 응축기를 나가는 기체 중 수증기의 몰분율은? (단, 60°C에서 포화수증기압은 20kPa이다)
- 1/30
- 1/15
- 1/3
- 2/3
6. 그림은 회분식 반응기에서 일어나는 메테인(CH4)의 완전연소 반응이다. 반응물이 100mol의 메테인과 300mol의 산소일 때, 반응 후 남은 산소와 생성된 물의 몰수의 합(n2+n4)[mol]은? (단, 메테인의 전화율(fractional conversion)은 80%이다)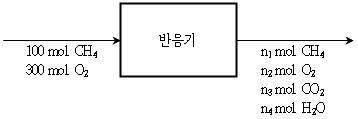
- 160
- 240
- 300
- 380
7. 내경 1cm인 원통형 파이프1과 내경 2cm인 원통형 파이프2가 직렬로 연결된 상태에서 물이 파이프 내부를 정상상태 흐름으로 흐를 때, 파이프1에서의 물의 평균유속은 파이프2에서의 물의 평균유속의 몇 배인가?
- 0.25
- 2
- 4
- 8
8. 황사현상이 심한 날 대기 중에 떠 있는 부유 분진량을 측정하기 위하여 대기흡입유량이 1.0m3ㆍmin-1인 분진 포집기를 이용하여 24시간 동안 포집한 분진의 양이 720mg일 때, 대기 중 부유 분진의 농도[μgㆍm-3]는?
- 300
- 400
- 500
- 600
9. 유체에 대한 설명으로 옳지 않은 것은?
- 전단응력(shear stress)은 전단력을 전단면적으로 나눈 값이다.
- 운동점도(kinematic viscosity)는 유체의 점도를 밀도로 나눈 값이다.
- 뉴튼 유체(Newtonian fluid)는 전단응력과 속도구배가 비례관계이다.
- 빙햄 유체(Bingham fluid)는 전단응력이 작아질수록 점도가 0에 수렴한다.
10. 판형 열교환기의 한쪽 벽면을 내부식성 소재로 코팅하고자 한다. 코팅제의 코팅 두께는 2μm이고 열교환기 금속 재질의 두께는 1cm일 때, 코팅으로 인한 단위 면적당 열전도 저항의 증가율[%]은? (단, 정상상태 조건에서 벽을 통한 1차원 전도이며, 열교환기 금속 재질과 코팅제 소재의 열전도도는 각각 10Wㆍm-1ㆍK-1, 2.0×10-2Wㆍm-1ㆍK-1이다)
- 5
- 10
- 15
- 20
11. 레이놀즈(Reynolds)수의 물리적 의미는?
- 마찰력/점성력
- 관성력/점성력
- 압력/관성력
- 부력/점성력
12. 열전달의 방법 중 복사(radiation)에 대한 설명으로 옳지 않은 것은?
- 복사 열전달에는 전달물질이 필요 없다.
- 흑체에서 단위 면적당 복사 에너지 방출 속도는 절대 온도의 네제곱에 비례한다.
- 복사에 의한 에너지 전달량은 에너지가 교환되는 두 면이 완전진공에 의해 분리되어 있을 때 최소가 된다.
- 흑체는 들어오는 복사 에너지를 반사하거나 투과하지 않는다.
13. 정압 비열의 정의는? (단, H는 단위 질량당 엔탈피, P는 압력, T는 절대 온도, V는 단위 질량당 부피이다)
14. 벤젠과 톨루엔의 혼합물이 기-액 평형을 이루고 있다. 기상에서 벤젠의 몰분율이 0.6일 때, 액상에서 톨루엔의 몰분율은? (단, 기체는 이상기체, 액상은 이상용액이며, 벤젠과 톨루엔의 증기압은 각각 1bar, 0.4bar이다)
- 0.5
- 0.625
- 0.75
- 0.875
15. 아세톤(acetone)과 메틸에틸케톤(methyl ethyl ketone)의 혼합물이 기-액 평형을 이루고 있는 계의 경우와 같은 자유도(degree of freedom) 수를 갖는 것만을 모두 고르면?
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄴ, ㄹ
16. 부피가 50.0cm3인 빈 비중병의 질량이 13.0g이다. 이 비중병에 분체를 가득 채운 후 측정한 질량은 37.0g이다. 분체로 가득 찬 비중병에 증류수를 넘치기 직전까지 넣었을 때 측정한 증류수의 부피가 30.0cm3이다. 이 분체의 겉보기밀도가 0.90gㆍcm-3일 때, 공극률은? (단, 분체로 가득 찬 비중병에 증류수를 넣을 때 증류수를 조금씩 천천히 넣어 분체 내부에 있는 기포를 완전히 제거하였고, 비중병으로부터 넘쳐 나온 분체는 전혀 없다)
- 0.20
- 0.25
- 0.30
- 0.35
17. 일정한 온도에서 성분 A와 성분 B로 이루어진 라울(Raoult)의 법칙을 따르는 혼합물이 기-액 평형에 있다. 성분 B에 대한 성분 A의 상대 휘발도 αAB를 나타낸 것으로 옳은 것은? (단, 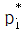 는 성분 i의 증기압, xi는 성분 i의 액상에서의 몰분율, yi는 성분 i의 기상에서의 몰분율을 나타낸다)
는 성분 i의 증기압, xi는 성분 i의 액상에서의 몰분율, yi는 성분 i의 기상에서의 몰분율을 나타낸다)
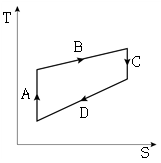
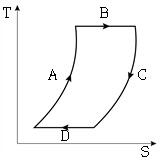
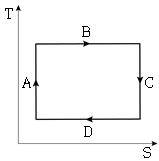
18. 4단계의 가역공정(단열압축(A)→등온팽창(B)→단열팽창(C)→등온압축(D))으로 구성된 카르노사이클(Carnot cycle)의 T-S선도로 옳은 것은? (단, T는 절대 온도, S는 단위 몰당 엔트로피이다)
19. 지름이 2cm인 수평 원통관을 통하여 레이놀즈수가 240인 조건으로 유체를 수송하던 중, 관이 파손되어 새로운 관으로 교체하였다. 교체된 관의 지름이 4cm이고, 동일한 유체를 같은 부피 유량만큼 수송할 때, 레이놀즈수는?
- 120
- 160
- 240
- 480
20. 20°C 공기 중에 부피 500mL의 직육면체 철판이 단열 바닥재 위에 놓여 있다. 철판이 220°C로 유지될 때, 철판으로부터 대류로 인한 열전달 속도[W]는? (단, 대류 열전달 계수는 10Wㆍm-2ㆍ°C-1이고 단열 바닥재에 놓여 있는 철판 접촉면의 가로, 세로 길이는 각각 20cm, 25cm이다. 열은 정상상태로 전달되며 공기의 온도는 일정하다)
- 100
- 118
- 200
- 218






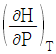
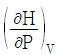
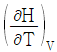
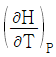
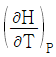 즉, $(\frac{\partial H}{\partial T})_{P}$ 입니다.
즉, $(\frac{\partial H}{\partial T})_{P}$ 입니다.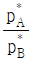
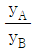
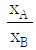
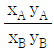
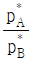 가 정답입니다.
가 정답입니다.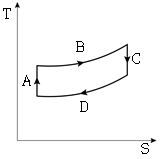
 가 정답입니다.
가 정답입니다.
① [기본 공식] $\Delta H^{\circ} = \sum n \Delta H_{f, \text{products}}^{\circ} - \sum m \Delta H_{f, \text{reactants}}^{\circ}$
② [숫자 대입] $\Delta H^{\circ} = [4(-250.5) + (-602)] - [2(-272) + (-1030)]$
③ [최종 결과] $\Delta H^{\circ} = -30$