1과목: 화학분석 과정관리
1. 보기의 물질을 물과 사염화탄소로 용해시키려 할 때 물에 더욱 잘 녹을 것이라고 예상되는 물질을 모두 나타낸 것은?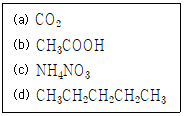
- (a), (b)
- (b), (c)
- (a), (b), (c)
- (b), (c), (d)
2. 광학 스펙트럼의 설명으로 틀린 것은?
- 연속 스펙트럼은 고체를 백열상태로 가열했을 때 발생한다.
- 분자 흡수는 전자전이, 진동 및 회전에 의해 일어나므로 띠스펙트럼이나 연속스펙트럼을 나타낸다.
- 스펙트럼에는 선스펙트럼, 띠스펙트럼 및 연속 스펙트럼이 있는데 자외선-가시선 영역의 원자 분광법에서는 주로 띠스펙트럼을 이용하여 분석한다.
- 들뜬 입자에서 발생되는 복사선은 보통 방출 스펙트럼에 의해서 특정되며, 이는 방출된 복사선의 상대세기를 파장이나 진동수의 함수로서 나타낸다.
3. 혼성 궤도함수(hybrid orbital)에 대한 설명으로 틀린 것은?
- 탄소 원자의 한 개의 s 궤도함수와 세 개의 p 궤도함수가 혼성하여 네 개의 새로운 궤도 함수를 형성하는 것을 sp3혼성 궤도함수라 한다.
- sp3혼성 궤도함수를 이루는 메테인은 C-H 결합각이 109.5도인 정사면체 구조이다.
- 벤젠(C6H6)을 분자궤도함수로 나타내면 각 탄소는 sp2혼성 궤도함수를 이루며 평면구조를 나타낸다.
- 사이클로헥세인(C6H12)을 분자궤도함수로 나타내면 각 탄소는 sp 혼성 궤도함수를 이룬다.
4. 다음 중 기기잡음이 아닌 것은?
- 열적잡음(Johnson noise)
- 산탄잡음(shot noise)
- 습도잡음(humidity noise)
- 깜빡이 잡음(flicker noise)
5. 다음 중 광학분광법에서 이용하지 않는 현상은?
- 형광
- 흡수
- 발광
- 흡착
6. 유기화합물의 명칭이 잘못 연결된 것은?
 : 사이클로뷰테인
: 사이클로뷰테인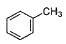 : 톨루엔
: 톨루엔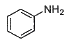 : 아닐린
: 아닐린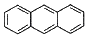 : 페난트렌
: 페난트렌
7. 다음 물질을 전해질의 세기가 강한 것부터 약해지는 순서로 나열한 것은?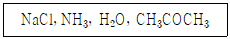
- NaCl > CH3COCH3 > NH3 > H2O
- NaCl > NH3 > H2O > CH3COCH3
- CH3COCH3 > NH3 > NaCl > H2O
- CH3COCH3 > NaCl > NH3 > H2O
8. 다음 단위체 중 첨가 중합체를 만드는 것은?
- C2H6
- C2H4
- HOCH2CH2OH
- HOCH2CH3
9. IR spectroscopy로 분석 시 1640 cm-1 근처에서약한 흡수를 보이는 물질의 화학식이 C4H8 일 때 이 물질이 갖는 이성질체수는?
- 2개
- 3개
- 4개
- 5개
10. 에탄올 50mL를 물 100mL과 혼합한 에탄올 수용액의 질량백분율은? (단, 에탄올의 비중은 0.79 이다.)
- 28.3
- 33.3
- 50.0
- 40.5
11. X-선 기기를 파장-분산형 기기와 에너지-분산형 기기로 분류할 때 구분기준은?
- 스펙트럼 분해 방법
- 스펙트럼 패턴
- 스펙트럼 영역
- 스펙트럼 구조
12. 비활성 기체로 채워진 관 안의 두 전극 사이에 발생한 기체 이온과 전자를 이용하는 분광법은?
- 원자 형광 분광법
- 글로우 방전 분광법
- 플라즈마 방출 분광법
- 레이저 유도 파괴 분광법
13. 어떤 화합물의 질량백분율 성분비를 분석했더니, 탄소 58.5%, 수소 4.1%, 질소 11.4%, 산소 26.0%와 같았다. 이 화합물의 실험식은? (단, 원자량은 C 12, H 1, N 14, O 16이다.)
- C2H5NO2
- C3H7NO2
- C5H5NO2
- C6H5NO2
14. 다음 중 1차 표준물질이 되기 위한 조건이 아닌 것은?
- 정제하기 쉬워야 한다.
- 흡수, 풍화, 공기 산화 등의 성질이 없어야 한다.
- 반응이 정량적으로 진행되어야 한다.
- 당량 중량이 적어서 측정 오차를 줄일 수 있어야 한다.
15. 주기율표에 대한 일반적인 설명 중 가장 거리가 먼 것은?
- 1A족 원소를 알칼리금속이라고 한다.
- 2A족 원소를 전이금속이라고 한다.
- 세로열에 있는 원소들이 유사한 성질을 가진다.
- 주기율표는 원자번호가 증가하는 순서로 원소를 배치하는 것이다.
16. 이온반지름의 크기를 잘못 비교한 것은?
- Mg2+ > Ca2+
- F- < O2-
- Al3+ < Mg2+
- O2-< S2-
17. H2 4g과 N2 10g, O2 40g으로 구성된 혼합가스가 있다. 이 가스가 25℃, 10리터의 용기에 들어 있을 때 용기가 받는 압력(atm)은?
- 7.39
- 8.82
- 89.41
- 213.72
18. 몰랄농도가 3.24m인 K2SO4 수용액 내 K2SO4의 몰분율은? (단, 원자량은 K 39.10, O 16.00, H 1.008, S 32.06 이다.)
- 0.551
- 0.36
- 0.0552
- 0.036
19. 전자가 보어모델(Bohr Model)의 n=5 궤도에서 n=3 궤도로 전이할 때 수소원자의 방출되는 빛의 파장(nm)은? (단, 뤼드베리 상수는 1.9678 ×10-2 nm-1 이다.)
- 434.5
- 486.1
- 714.6
- 954.6
20. 다음 화합물 중 octet rule을 만족하지 않는 것은?
- H2O의 O
- CO2의 C
- PCl5의 P
- NO3-의 N
2과목: 화학물질 특성분석
21. NH4+ 의 Ka= 5.69×10-10일 때 NH3의 염기 해리 상수(Kb)는? (단, Kw= 1.00 × 10-14 이다.)
- 5.69 × 10-7
- 1.76 × 10-7
- 5.69 × 10-5
- 1.76 × 10-5
22. 전지의 두 전극에서 반응이 자발적으로 진행되려는 경향을 갖고 있어 외부 도체를 통하여 산화전극에서 환원전극으로 전자가 흐르는 전지 즉, 자발적인 화학반응으로부터 전기를 발생시키는 전지는?
- 전해 전지
- 표준 전지
- 자발 전지
- 갈바니 전지
23. 전기화학 전지에 관한 패러데이의 연구에 대한 설명 중 옳지 않은 것은?
- 전극에서 생성되거나 소모된 물질의 양은 전지를 통해 흐른 전하의 양에 반비례한다.
- 일정한 전하량이 전지를 통하여 흐르게 되면 여러 물질들이 이에 상응하는 당량만큼 전극에서 생성되거나 소모된다.
- 패러데이 법칙은 전기화학 과정에서의 화햑양론을 요약한 것이다.
- 패러데이 상수(F)는 96485.32 C/mol 이다.
24. 시료 중 칼슘을 정량하기 위해 시료 3.00g을 전처리하여 EDTA로 칼슘을 적정하였더니 15.20mL의 EDTA가 소요되었다. 아연금속 0.50g을 산에 녹인 후 1.00L로 묽혀서 만든 용액 10.00mL로 EDTA를 표정하였고, 이때 EDTA는 12.50mL가 소요되었다. 시료 중 칼슘의 농도(ppm)는? (단, 아연과 칼슘의 원자량은 각각 65.37 g/mol, 40.08 g/mol 이다.)
- 12.426
- 124.26
- 1242.6
- 12426
25. van Deemter식과 각 항의 의미가 아래와 같을 때, 다음 설명 중 틀린 것은?
- A는 다중이동 통로에 대한 영향을 말한다.
- B/u는 세로확산에 대한 영향을 말한다.
- Cu 물질이동에 의한 영향을 말한다.
- H는 분리단의 수를 나타내는 항이다.
26. 산화수에 관한 설명 중 틀린 것은?
- 원소 상태의 원자는 산화수가 0이다.
- 일원자 이온의 원자는 전하와 동일한 산화수를 갖는다.
- 과산화물에서 산소원자는 –1의 산화수를 갖는다.
- C, N, O, Cl과 같은 비금속과 결합할 때 수소는 –1의 산화수를 갖는다.
27. 불꽃 원자 분광법에서 화학적 방해의 주요요인이 아닌 것은?
- 해리 평형
- 이온화 평형
- 시료 원자의 구조
- 용액 중에 존재하는 다른 양이온
28. C-Cl 신축진동을 관측하기 위한 적외선 분광분석기의 창(window) 물질로 적합하지 않은 것은?
- KBr
- CaF2
- NaCl
- mineral oil + KBr
29. ppm과 ppb의 관계가 옳게 표현된 것은?
- 1 ppm = 1000 ppb
- 1 ppm = 10 ppb
- 1 ppm = 1 ppb
- 1 ppm = 0.001 ppb
30. 0.100 M CH3COOH 용액 50.0mL를 0.0500 M NaOH로 적정할 때 가장 적합한 지시약은?
- 메틸 오렌지
- 페놀프탈레인
- 브로모크레졸 그린
- 메틸 레드
31. 용질의 농도가 0.1M로 모두 동일한 다음 수용액 중 이온 세기(ionic strength)가 가장 큰 것은?
- NaCl(aq)
- Na2SO4(aq)
- Al(NO3)3(aq)
- MgSO4(aq)
32. 어떤 염의 물에 대한 용해도가 70℃에서 60g, 30℃에서 20g일 때, 다음 설명 중 옳은 것은?
- 70℃에서 포화용액 100g에 녹아 있는 염의 양은 60g 이다.
- 30℃에서 포화용액 100g에 녹아 있는 염의 양은 20g 이다.
- 70℃에서 포화용액 30℃로 식힐 때 불포화용액이 형성된다.
- 70℃에서 포화용액 100g을 30℃로 식힐 때 석출되는 염의양은 25g 이다.
33. 다음 중 환원제로 사용되는 물질은?
- 과염소산
- 과망간산칼륨
- 포름알데하이드
- 과산화수소
34. 0.1M 약염기 B 100mL 수용액에 0.1 M HCl 50mL 수용액을 가했을 때의 pH는? (단, Kb= 2.6 × 10-6 이고 Kw = 1.0 × 10-14 이다.)
- 5.59
- 7.00
- 8.41
- 9.18
35. 원자 흡수 분광법에서 연속광원 바탕보정법에 사용되는 자외선 영역의 연속광원은?
- 중수소등
- 텅스텐등
- 니크롬선등
- 속빈음극등
36. 다음의 두 평형에서 전하 균형식(charge balance equation)을 옳게 표현한 것은?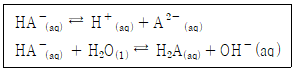
- [H+] = [HA-]+ [A2-]+[OH-]
- [H+] = [HA-]+ 2[A2-]+[OH-]
- [H+] = [HA-]+ 4[A2-]+[OH-]
- [H+] = 2[HA-]+ [A2-]+[OH-]
37. Cu(s) + 2Fe3+ ⇄ 2Fe2++ Cu2+ 반응의 25℃에서 평형상수는? (단, E°는 25℃에서의 표준 환원 전위이다.)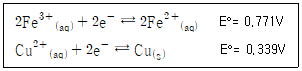
- 1 × 1014
- 2 × 1014
- 3 × 1014
- 4 × 1014
38. 0.100 M BH22+ 용액 20.0mL를 0.20M NaOH용액으로 적정하는 실험에 대한 설명으로 옳은 것은? (단, BH22+의 산해리 상수 Ka1과 Ka2는 각각 1.00 ×10-4, 1.00 × 10-8 이고 물의 이온화곱상수는 1.00 × 10-14 이다.)
- NaOH(aq) 5.00mL를 가했을 때 용액에는 BH22+와 BH+가 1:1의 몰비로 존재한다.
- NaOH(aq) 10.0mL를 가했을 때 용액의 pH는 5.0 이다.
- NaOH(aq) 15.00mL를 가했을 때 용액에서 B와 BH+가 4:6의 몰수비로 존재한다.
- NaOH(aq) 20.0mL를 가했을 때 용액의 pH를 결정하는 주 화학종은 BH+이다.
39. 아래와 같은 화학반응식의 평형 이동에 관한 설명 중 틀린 것은?
- 반응계를 냉각할 경우 평형은 오른쪽으로 이동한다.
- 반응계에 Ar(g)를 가하면 평형은 왼쪽을 이동한다.
- CO(g)를 첨가할 경우 평형은 오른쪽으로 이동한다.
- O2(g)를 제거할 경우 평형은 왼쪽으로 이동한다.
40. 이양성자성 산(BH22+)의 산 해리 상수가 각각 pKa1 = 4, pK2a = 9일 때 [BH+] = [BH22+]를 만족하는 pH는?
- 4
- 5
- 6.5
- 9
3과목: 화학물질 구조분석
41. 열무게분석법(ThermoGravimetric Analysis; TGA)에서 전기로를 질소와 아르곤으로 분위기를 만드는 주된 이유는?
- 시료의 환원 억제
- 시료의 산화 억제
- 시료의 확산 억제
- 시료의 산란 억제
42. Naclear Magnetic Resonance(NMR)의 화학적 이동에 영향을 미치는 인자가 아닌 것은?
- 혼성 효과(Hybridization effect)
- 도플러 효과(Doppler effect)
- 수소결합 효과(Hydrogen bond effect)
- 전기음성도 효과(Electronegativity effect)
43. 기체-고체 크로마토그래피(GSC)에 대한 설명으로 틀린 것은?
- 고체표면에 기체물질이 흡착되는 현상을 이용한다.
- 분포상수는 보통 GLC의 경우 보다 적다.
- 기체-액체 컬럼에 머물지 않는 화학종을 분리하는데 유용하다.
- 충전 컬럼과 열린관 컬럼 두 가지 모두 사용된다.
44. 폭이 매우 좁은 KBr셀 만을 적외선 분광기에 걸고 적외선 스펙트럼을 얻었다. 시료가 없기 때문에 적외선 흡수 밴드는 보이지 않고, 그림과 같이 파도 모양의 간섭파를 스펙트럼에 얻었다. 이 셀의 폭(mm)으로 가장 알맞은 것은?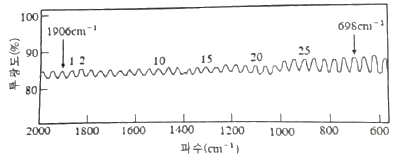
- 0.1242
- 12.42
- 24.82
- 248.4
45. 질량분석기에서 분석을 위해서는 분석물이 이온화되어야 한다. 이온화 방법은 분석물의 화학결합이 끊어지는 Hard Ionization 방법과 화학결합이 그대로 있는 Soft Ionization 방법이 있다. 다음 중 가장 Hard Ionization에 가까운 것은?
- 전자 충돌 이온화(Electron Impact Ionization)
- 전기 분무 이온화(ESI, Electrospray Ionization)
- 메트릭스 보조 레이저 탈착 이온화(MALDI, Matrix Assisted Laser Desorption Ionization)
- 화학 이온화(CI, Chemical Ionization)
46. 적외선 흡수분광기의 검출기로 사용할 수 있는 열검출기(thermal detector)가 아닌 것은?
- 열전기쌍(thermocouple)
- 써미스터(thermistor)
- 볼로미터(bolometer)
- 다이오드 어레이(doode array)
47. 카드뮴 전극이 0.010M Cd2+ 용액에 담가진 반쪽전지의 전위(V)는? (단, 온도는 25℃이고 Cd2+/Cd의 표준환원전위는 –0.403 V 이다.)
- -0.40
- -0.46
- -0.50
- -0.56
48. 전기화학분석에 관한 설명에서 올바른 것은?
- 전지화학 전지의 전위는 환원반응이 일어나는 환원전극의 전극전위에서 산화반응이 일어나는 산화전극의 전극전위를 빼주어 계산한다.
- IUPAC 규약에 의해서 전극전위를 산화반응에 대한 것은 산화전극전위라고 하고 환원반응에 대한 것은 환원전극전위로 나타내어 사용하기로 한다.
- 각 산화-환원 반응에 대한 전극전위는 0℃에서 표준수소전극전위를 0V로 놓고 이에 대한 상대적인 산화-환원력의 척도로 나타낸 것이다.
- 형식전위(formal potential)는 활성도 효과와 부반응으로부터 오는 오차를 보상하기 위하여 반응용액에 존재하는 성분들의 농도가 1F(포말 농도)에서의 표준전위를 말한다.
49. 폴라로그래피에서 펄스법의 감도가 직류법보다 좋은 이유는?
- 펄스법에서는 페러데이 전류와 충전전류의 차이가클 때 전류를 측정하기 때문
- 펄스법은 빠른 속도로 측정하기 때문
- 직류법에서는 빠르게 펄스법에서는 느리게 전압을 주사하기 때문
- 펄스법에서는 비페러데이 전류가 최대이기 때문
50. 열무게분석법(ThermoGravimetric Analysis; TGA)으로 얻을 수 있는 정보가 아닌 것은?
- 분해반응
- 산화반응
- 기화 및 승화
- 고분자 분자량
51. 시차주사열량법(Diggerential Scanning Calorimetry; DSC)에 대한 설명 중 틀린 것은?
- 온도변화에 따른 무게변화를 측정
- 시료물질과 기준물질의 열량차이를 시료온도 함수로 측정
- 열흐름 DSC는 열흐름의 차이를 온도를 직선적으로 증가하면서 측정
- 전력보상 DSC는 시료물질과 기준물질을 두 개의 다른 가열기로 가열
52. 자기장분석 질량분석기(Magenetic sector analyzer) 중 이중 초점 분석기에 대한 설명으로 틀린 것은?
- 이온다발의 방향과 에너지의 벗어나는 정도를 모두 최소화하기 위해 고안된 장치이다.
- 두 개의 sector 중 하나는 정전기적 sector이고, 다른 하나는 자기적 sector이다.
- 정전기적 sector는 전기장을 걸어주어 질량 대 전하비를 분리하고, 자기적 sector는 자기장을 걸어주어 운동에너지분포를 좁은 범위로 제한한다.
- 이론적으로 질량을 변화시켜 스캐닝하는 방법은 자기장, 가속전압 및 sector의 곡률반경을 변경하는 것이다.
53. 원자 및 분자 질량(atomic & molecular mass)에 대한 설명으로 틀린 것은?
- 원소들의 원자 질량은 탄소-12의 질량을 12 amu 또는 Dalton으로 놓고 그것에 대한 상대 질량을 의미한다.
- 원자량은 자연에 존재하는 동위원소의 존재비와 질량으로 해서 평균한 질량을 말한다.
- 화학식량은 자연에 가장 많이 존재하는 대표적인 동위원소의 질량을 화학식에 나타난 모든 원소의 합으로 나타낸 것이다.
- 동위원소는 원자번호는 같으나 질량이 다른 원소를 의미하며 화학적 성질은 같다.
54. 시차주사열량법(Differential Scanning Calorimetry; DSC)은 전이엔탈피와 온도 혹은 반응열을 측정할 수 있으므로 아주 유용하다. 다음 중 DSC의 응용 분야로서 가장 거리가 먼 것은?
- 상전이과정 측정
- 결정화온도 측정
- 고분자물 경화여부 측정
- 휘발성 유기성분 분석
55. Nuclear Magnetic Resonance(NMR)에서 이용하는 파장은?
- 적외선(infrared)
- 자외선(ultraviolet)
- 라디오파(radio wave)
- 마이크로웨이브(microwave)
56. Gas Chromatograp(GC) 검출기 중 할로겐 원소에 대한 선택성이 큰 검출기는?
- 전자포착검출기(ECD, Electron Capture Detector)
- 열전도검출기(TCD, Thermal Conductivity Detector)
- 불꽃이온화 검출기(FID, Flame Ionization Detector)
- 열이온검출기(TID, Thermionic Detector)
57. 얇은층 크로마토그래피(TLC)의 일반적인 용도가 아닌 것은?
- 혼합물 중에 포함된 성분의 수를 결정
- 화학반응 중에 생성되는 중간체 확인
- 혼합물의 화학결합 존재여부 확인
- 화합물의 순도 확인
58. 아주 큰 분자량을 갖는 극성 생화학 고분자의 분자량에 대한 정보를 알 수 있는 가장 유용한 이온화법은?
- 장 이온화(FI, Field Ionization)
- 화학 이온화(CI, Chemical Ionization)
- 전자 충돌 이온화(Electron Impact Ionization)
- 메트릭스 보조 레어저 탈착 이온화(MALDI, Matrix Assisted Laser Desorption Ionization)
59. 니켈(Ni2+)과 카드뮴(Cd2+)이 각각 0.1M인 혼합용액에서 니켈만 전기화학적으로 석출하고자 한다. 카드뮴이온은 석출되지 않고, 니켈이온이 0.01%만 남도록 하는 전압(V)은?
- -0.2
- -0.3
- -0.4
- -0.5
60. TLC에서 Rf값을 구하는 식은?
- 분석물의 이동거리 ÷ 용매의 최대 이동거리
- 분석물의 이동거리 ÷ 표준물질의 최대 이동거리
- 용매의 최대 이동거리 ÷ 분석물의 이동거리
- 표준물질의 최대 이동거리 ÷ 분석물의 이동거리
4과목: 시험법 밸리데이션
61. 분석기기의 성능점검주기를 선정할 때 고려할 사항을 보기에서 모두 나열한 것은?
- A, B
- A, C, D
- A, B, C, E
- A, B, C, D, E ,F
62. 시험법이 정밀성, 정확성, 직선성이 적절한 수준임을 밝혀진 상태에서 검체 내 시험 대상물의양 또는 농도의 상한 및 하한 농도사이의 구간을 범위(Range)라고 정의한다. 다음 중 최소로 규정하는 범위로 틀린 것은?
- 원료 의약품의 정량시험 : 시험 농도의 80 ~ 120%
- 완제 의약품의 정량시험 : 시험 농도의 90 ~ 110%
- 함량 균일성 시험 : 시험 농도의 70 ~ 130%
- 용출시험 : 용출시험기준 범위의 ±20%
63. 생체시료효과에 대한 설명 중 틀린 것은?
- 생체시료효과란 생체시료 내의 물질이 직접 또는 간접적으로 분석물질 또는 내부표준물질의 반응에 미치는 영향을 말한다.
- 생체시료효과를 분석하기 위해서는 6개의 서로 다른 생체시료를 가지고 분석하나, 구하기 힘든 생체시료의 경우 6개 보다 적은 수를 사용할 수 있다.
- 생체시료효과상수를 계산하기 위한 실험데이터를 활용하기 위해서는 품질관리시료의 농도값의 변동계수가 20%이내이어야 한다.
- 생체시료효과상수는 생체시료의 유무에 따른 분석결과의 비율로서 계산한다.
64. 일반적으로 전처리과정에서 대상성분의 함량이 낮은 경우 더욱 고려해야 하는 검체의 특성은?
- 안정성
- 균질성
- 흡습성
- 용해도
65. 시료분석 시의 정도관리 요소 중 바탕값(black)의 종류와 내용이 옳게 연결된 것은?
- 현장바탕시료(field black sample)는 시료채취 과정에서 시료와 동일한 채취과정의 조작을 수행하는 시료를 말한다.
- 운송바탕시료(trip balck sample)는 시험 수행과정에서 사용하는 시약과 정제수의 오염과 실험절차의 오염, 이상 유무를 확인하기 위한 목적에 사용한다.
- 정제수 바탕시료(reagent black sample)는 시료채취과정의 오염과 채취용기의 오염 등 현장 이상유무를 확인하기 위함이다.
- 시험바탕시료(method blanks)는 시약 조제, 시료 희석, 세척 등에 사용하는 시료를 말한다.
66. 수용액의 pH 측정에 관한 설명으로 틀린 것은?
- 전극이 필요하다.
- 광원이 필요하다.
- 표준 완충 용액이 필요하다.
- 수용액의 수소 이온 농도를 측정한다.
67. 분석결과의 정밀성과 가장 밀접한 것은?
- 검출한계
- 특이성
- 변동계수
- 직선성
68. 불꽃원자화기의 소모품 중 네뷸라이저(nebulizer)의 역할로 옳은 것은?
- 역화 방지
- 연소 기체 혼합
- 에어로솔 생성
- 연소로 인해 생성된 수분 제거
69. 표준 편차에 대해 올바르게 설명한 것은?
- 표준 편차가 작을수록 정밀도가 더 크다.
- 표준 편차가 클수록 정밀도가 더 크다.
- 표준 편차와 정밀도는 상호 관계가 없다.
- 표준 편차는 정확도와 가장 큰 상호 관계를 갖는다.
70. 화학 분석의 일반적 단계를 설명한 내용 중 틀린 것은?
- 시료 채취는 분석할 대표 물질을 선택하는 과정이다.
- 시료 준비는 대표 시료를 녹여 화학 분석에 적합한 시료로 바꾸는 과정이다.
- 분석은 분취량에 들어 있는 분석물질의 농도를 측정하는 과정이다.
- 보고와 해석은 대략적으로 작성하고, 결론도출에서 명료하고 완전하며 책임질 수 있는 자료를 작성한다.
71. 유효숫자를 고려하여 아래를 계산할 때, 얻어지는 값은?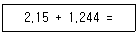
- 3
- 3.4
- 3.39
- 3.394
72. 분석업무지시서에서 확인 가능한 검체 처리과정으로 틀린 것은?
- 검체 검증 분석의 시기 : 검체의 안정성이 확보된 기간 내에서 최초 분석과 같은 날, 서로 다른 배치에서 실시
- 검체 검증 분석의 검체 수 : 전체 검체 수가 1000개 이하인 경우, 검체 검증 분석은 검체 수의 10%에 해당하는 수 만큼 검체를 선정
- 검체 검증 분석의 검체 수 : 전체 검체 수가 1000개 초과인 경우, 1000개의 10%에 해당하는 수와 1000개를 제외한 나머지의 5%에 해당하는 수만큼 검체를 선정
- 검체 검증 분석의 판정 기준 편차(%) :

73. 투과율 눈금 교정 시 인증표준물질을 이용하여 6회 반복 측정한 실험결과 값으로부터 우연불확정도와 전체불확정도를 구하여 측정값으로 옳게 표시한 것은? (단, 평균값 ≒ 18.32%, 표준편차 = 0.011%, 인증표준물질의 불확도 = 0.1%, t값 = 2.65 이다.)
- 18.32% ± 0.1%
- 18.32% ± 0.2%
- 18.32% ± 0.3%
- 18.32% ± 0.4%
74. Linearity시험 결과 도표의 해석으로 틀린 것은? (단, 기준 농도는 L3로 한다.)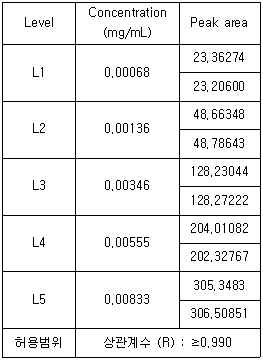
- Linearity 결과 합격이다.
- 농도범위는 분석 농도의 20 ~ 240% 이다.
- 농도와 area에 대한 linear regression을 실시하여 Y=36598.7X-1.0의 형태로 직선식을 구할 수 있다.
- 위 시험결과를 최소자승법에 의한 희귀선의 계산을 통해 평가했을 때, R값은 0.999이다.
75. 분석물질의 직선성을 시험한 결과 도표를 완성할 때, 값이 틀린 것은? (단, 농도 범위는 분석농도의 80~120% 이다.)
- A : 0.08
- B : 2012
- C : 0.9999
- D : 0.9
76. 약전에 수재(收載)되어있는 분석법의 정밀성 평가 항목이 아닌 것은?
- 반복성
- 직선성
- 실내재현성
- 실간재현성
77. 최저 정량 한계에서 추출한 시료의 신호 대 잡음비를 계산한 값을 무엇이라 하는가?
- 정확성
- 회수율
- 감도
- 정밀성
78. 대한민국약전 의거한 근적외부스펙트럼측정법 분광분석기의 적격성 평가에 대한 설명 중 틀린 것은?
- 수행적격성 평가란 분석장비가 지속적으로 작동되는지 확인하는 것을 의미한다.
- 수행적격성 평가는 최소 6개월에 한번씩 실시한다.
- 설치적격성 평가 시 하드웨어 일련번호, 소프트웨어의 버전 등을 기록하는 작업이 포함된다.
- 설치적격성 평가는 장치의 설치 환경에 의한 기기의 정확성과 재현성을 검증하는 것을 의미한다.
79. 평균값과 표준편차를 얻기 위한 시험으로 계통오차를 제거하지 못하는 시험법은?
- 공시험
- 조절시험
- 맹시험
- 평행시험
80. ICH에서 공지한 대표적인 밸리데이션 항목에 포함되지 않는 것은?
- 재현성
- 특이성
- 직선성
- 정량한계
5과목: 환경·안전관리
81. 분말소화기의 종류와 소화약제의 연결로 틀린 것은?
- 제1종 - 탄산수소나트륨
- 제2종 - 탄산수소칼륨
- 제3종 - 제1인산암모늄
- 제4종 – 요소와 탄산수소나트륨
82. 다음의 유해화학물질의 건강유해성의 표시 그림문자가 나타내지 않는 사항은?
- 호흡기 과민성
- 발암성
- 생식독성
- 급성독성
83. GHS 그림문자 표기 물질에 해당하는 것은?
- 산화성 물질
- 급성 독성 물질
- 물반응성 물질
- 호흡기 과민성 물질
84. 실험실에서 화재가 발생한 경우 적절한 조치가 아닌 것으로만 묶인 것은?
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄷ, ㄹ
- ㄱ, ㄹ
85. 위험물에 대한 소화방법으로 옳지 않은 것은?
- 염소산나트륨과 같은 제1류 위험물의 경우 물을 주수하는 냉각소화가 효과적이다.
- 제2류 위험물인 금속분, 철분, 마그네슘, 적린, 유황은 물에 의한 냉각소화가 적당하다.
- 제3류 위험물 중 황린은 물을 주수하는 소화가 가능하다.
- 제4류 위험물은 일반적으로 질식소화가 적합하다.
86. 가연성 물질이 연소되기 위한 조건으로 가장 거리가 먼 것은?
- 산소와 반응해야 한다.
- 연소반응이 지속되기 위해서 산화반응이 발열반응이어야 한다.
- 열전도율이 커야 한다.
- 연소반응이 지속되기 위해 반응열이 충분히 방출되어야 한다.
87. 물질안전보건자료의 작성 원칙이 아닌 것은?
- 한글로 작성하는 것을 원칙으로 하며, 외국 기관명 등 고유명사는 영어로 표기한다.
- 여러 형태의 자료를 활용하여 작성 시 제공되는 자료의 출처를 모두 기재할 필요가 없다.
- 외국어로 작성된 MSDS를 번역하고자 하는 경우에는 자료의 신뢰성이 확보될 수 있도록 최초의 작성 기관명 및 시기를 함께 기재한다.
- 함유량의 ±5% 범위 내에서 함유량의 범위로 함유량을 대신하여 표시할 수 있다.
88. 폐기물관리법령에 따라 “사업장폐기물배출자”가 폐기물처리를 스스로 처리하지 않고 폐기물처리업자등에게 위탁할 때 그 위탁을 받은 자로부터 수탁처리능력확인서를 제출받아야 하는 경우는?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.)
- 지정폐기물인 오니를 월 평균 500kg 배출하는 경우
- 지정폐기물이 아닌 오니를 월 평균 500kg 배출하는 경우
- 지정폐기물인 폐유기용제를 월 평균 100kg 배출하는 경우
- 지정폐기물인 폐유독물질을 배출하는 경우
89. ㉠과 ㉡의 설명을 모두 만족하는 화학반응은?
- 화합반응
- 산화환원반응
- 이중 치환반응
- 분해반응
90. 화학물질관리법령에 따라 검사 결과 취급시설의 구조물이 균열·부식 등으로 안정상의 위해가 우려된다고 인정되는 경우 검사 결과를 받은 날로부터 며칠 이내에 특별안전진단을 받아야 하는가?
- 10일
- 15일
- 20일
- 30일
91. 분자량이 70.9인 상온에서 황록색을 띠는 기체의 NFPA 건강위험성 코드 등급은?
- 1등급
- 2등급
- 3등급
- 4등급
92. 실험실에서 활용되는 다양한 화학 물질에 대한 설명으로 틀린 것은?
- 실험실 청소에 활용되는 표백제는 하이포염소산나트륨(NaClO) 성분으로 구성되어 있으며, 암모니아와 섞으면 독가스가 형성되어 취급에 주의를 요한다.
- 불산은 이온화 반응에서 약간만 이온화되는 약산으로 인체 위험도가 낮은 화학물질이다.
- 염산은 이온화 반응에서 거의 100% 이온화되므로 강산이다.
- 아세트산은 이온화 과정에서 1% 정도만 이온화되므로 약산이다.
93. 환경유해인자에 노출되는 기준에 대한 설명 중 틀린 것은?
- 소음기준은 1일 동안 노출시간이 길어지거나 노출회수가 많아질수록 소음강도수준(dB(A))은 커진다.
- 시간가중평균노출기준(TWA)은 1일 8시간 작업을 기준으로 한다.
- 단시간 노출 기준(STEL)의 단시간이란 1회에 15분간 유해인자에 노출되는 것을 기준으로 한다.
- 최고 노출 기준(C)은 1일 작업 시간 동안 잠시라도 노출되어서는 아니 되는 기준을 말한다.
94. 위험물안전관리법령에 따른 위험물취급소의 종류에 해당하지 않는 것은?
- 이동취급소
- 판매취급소
- 일반취급소
- 이송취급소
95. 실험실 폐액 처리 시 주의사항으로 틀린 것은?
- 원액 폐기 시 용기 변형이 우려되므로 별도로 희석 처리 후 폐기한다.
- 화기 및 열원에 안전한 지정 보관 장소를 정하고, 다른 장소로의 이동을 금지한다.
- 직사광선을 피하고 통풍이 잘되는 곳에 보관하고, 복도 및 계단 등에 방치를 금한다.
- 폐액통을 밀봉할 때에는 폐액을 혼합하여 용기를 가득 채운 후 압축 밀봉한다.
96. 화학 물질을 취급할 때 주의해야 할 사항으로 적절한 것은?
- 모든 용기에는 약품의 명칭을 기재하는 것이 원칙이나 증류수처럼 무해한 약품은 기재하지 않는다.
- 사용할 물질의 성상, 특히 화재·폭발·중독의 위험성을 잘 조사한 후가 아니라면 위험한 물질을 취급해서는 안 된다.
- 모든 약품의 맛 또는 냄새 맡는 행위를 절대로 금하고, 입으로 피펫을 빨아서 정확도를 높인다.
- 약품의 용기에 그 명칭을 표기하는 것은 사용자가 약품의 사용을 빨리 하게 하려는 목적이 전부다.
97. 대기오염방지시설 중 오염물질이 통과하는 관로(덕트)에 1.225 kg/m3의 밀도를 갖는 공기가 20m/s 의 속도로 통과할 때 동압(mmH2O)은?
- 15
- 20
- 25
- 30
98. 실험실 환경에 대한 설명으로 틀린 것은?
- 환기 장치 가동 시 실험자가 소음으로 지장을 받지 않도록 가능한 한 60dB이하가 되도록 해야 한다.
- 분석용 가스 저장능력은 가스의 종류와 무관하게 저장분의 1.0배 이하로 하여야 한다.
- 분석실 내 배수관의 재질은 가능한 한 산성이나 알칼리성 물질에 잘 부식되지 않는 재질을 선택하여야 한다.
- 기기 분석실에 안정적인 전원을 공급할 수 있도록 무정전 전원 장치(UPS) 또는 전압 조정 장치(AVR)를 설치해야 한다.
99. 실험복 및 개인보호구 착의 순서로 옳은 것은?
- 긴 소매 실험복 → 마스크 → 보안면 → 실험장갑
- 긴 소매 실험복 → 보안면 → 실험장갑 → 마스크
- 마스크 → 긴 소매 실험복 → 보안면 → 실험장갑
- 실험장갑 → 긴 소매 실험복 → 마스크 → 보안면
100. 다음 중 아세틸렌의 수소 첨가 반응에 해당하는 것은?
- C2H2(g) + H2(g) → C2H4(g)
- C2H4(g) + H2(g) → C2H6(g)
- 2C2H2(g) + 5O2(g) → 4CO2(g) + 2H2O(L)
- CaC2(s) + 2H2O(L) → C2H2(g) + Ca(OH)2(aq)






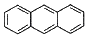 는 벤젠 고리 3개가 직선으로 연결된 안트라센의 구조입니다. 페난트렌은 벤젠 고리 3개가 굽어 있는 형태를 가집니다.
는 벤젠 고리 3개가 직선으로 연결된 안트라센의 구조입니다. 페난트렌은 벤젠 고리 3개가 굽어 있는 형태를 가집니다. 의 A, B, C, D, E, F 항목 모두가 고려 사항에 해당합니다.
의 A, B, C, D, E, F 항목 모두가 고려 사항에 해당합니다. 그림문자는 건강유해성(발암성, 생식독성, 호흡기 과민성 등)을 나타내는 심볼입니다.
그림문자는 건강유해성(발암성, 생식독성, 호흡기 과민성 등)을 나타내는 심볼입니다. 그림문자는 불꽃 아래에 직선(물 표면)이 그려져 있는 형태로, 물과 반응하여 인화성 가스를 발생시키는 물반응성 물질을 의미합니다.
그림문자는 불꽃 아래에 직선(물 표면)이 그려져 있는 형태로, 물과 반응하여 인화성 가스를 발생시키는 물반응성 물질을 의미합니다.
제시된 물질 중 $\text{CH}_3\text{COOH}$ (아세트산)와 $\text{NH}_4\text{NO}_3$ (질산암모늄)은 극성 및 이온성 물질이므로 물에 더 잘 녹습니다.
오답 노트
$\text{CO}_2$, $\text{CH}_3\text{CH}_2\text{CH}_2\text{CH}_2\text{CH}_3$: 무극성 물질로 사염화탄소에 더 잘 녹음