1과목: 과목구분없음
1. 그림과 같이 실온에서 용기 (가)에는 기체 A가 12몰, (나)에는 기체 B가 9몰 들어 있고, (다)는 비어 있다. 
콕을 모두 열고 충분한 시간이 흐른 후, 용기에 존재하는 기체 A와 B의 몰수에 대한 설명으로 옳은 것은? (단, 두 기체는 서로 반응하지 않으며 용기의 부패는 동일하고 연결관의 부피는 무시한다.)
- 각각의 용기에는 기체 A가 4몰, 기체 B가 3몰씩 들어 있다.
- (가)에는 기체 A가 6몰, 기체 B가 3몰 들어 있다.
- (나)에는 기체 B가 6몰 들어 있다.
- 기체 A는 (가)에 8몰, (나)에 4몰 들어 있다.
- 기체 B는 (나)에 3몰, (가)에 6몰 들어 있다.
2. 그림은 암모니다(NH3)와 질산칼륨(KNO3)의 용해도 곡선을 나타낸 것이다. 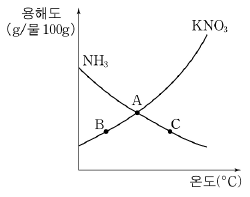
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, NH3와 KNO3의 화학식량은 각각 17, 101이다.)
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
3. 표는 0℃, 1기압에서 물질 A~C에 대한 자료이다. 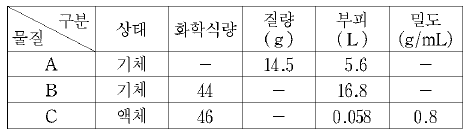
이 자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
4. 그림과 같은 용기에 같은 질량의 메탄(CH4)과 이산화황(SO2)을 넣었다. 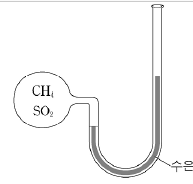
두 기체의 분압에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, 두 기체는 서로 반응하지 않으며 H, C, O, S의 원자량은 각각 1, 12, 16, 32이다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
5. 표는 분자량이 서로 다른 세 가지 비휘발성, 비전해질 물질을 각각 물 100g에 녹여 용액 A~D를 만든 후 1기압에서 어는점과 끓는점을 측정한 결과이다. 
같은 물질이 녹아 있는 용액으로 짝지어진 것은? (단, 용액 A~D에는 한 가지 물질만 녹아 있으며 물의 몰랄내림상수는 1.86℃/m, 몰랄오름상수는 0.52℃/m이다.) [3점]
- A, C
- A, D
- B, C
- B, D
- C, D
6. 그림과 같이 0℃에서 일산화탄소(CO), 질소(N2), 수소(H2)기체가 동일한 세 개의 용기에 각각 채워져 있다. 
각 용기 안의 기체에 대한 설명으로 옳은 것은? (단, H, C, N, O의 원자량은 각각 1, 12, 14, 16이다.) [3점]
- CO와 N2의 밀도는 서로 같다.
- N2와 H2의 평균 분자 운동속도는 서로 같다.
- CO의 평균 분자운동에너지가 H2보다 크다.
- 분자 사이의 평균 거리가 가장 가까운 것은 N2이다.
- 시간당 용기 벽에 충돌하는 횟수는 H2가 N2보다 크다.
7. 그림과 같은 장치에 반투막을 경계로 농도가 서로 다른 포도당 수용액을 넣었다. 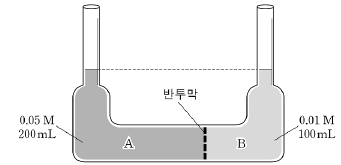
이 장치에서 일어나는 현상으로 옳은 것을 <보기>에서 모두 고른 것은? (단, 온도에 따른 용액의 부피 변화는 무시한다.)
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
8. 다음은 요소와 아세톤의 구조식이다. 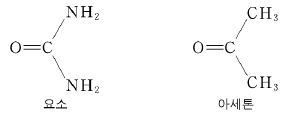
두 화합물에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
9. 그림 (가)와 (나)는 30℃에서 크기가 같은 플라스크에 같은 부피의 물과 에테르를 넣고 고무풍선을 씌웠을 때의 모습이고 (다)는 두 액체의 증기압력 곡선이다. 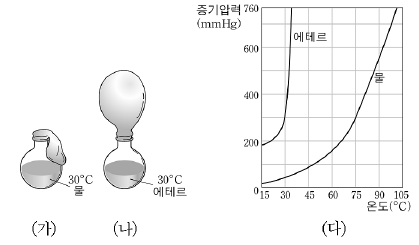
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
10. 다음은 Cl2, Br2, I2의 반응성을 알아보는 실험이다. (단, X, Y, Z는 임의의 할로겐 원소이다.) 
이 실험 결과로부터 알 수 있는 X, Y, Z로 옳은 것은?(순서대로 X, Y, Z) [3점]
- Cl, Br, I
- Cl, I, Br
- Br, Cl, I
- Br, I, Cl
- I, Br, Cl
11. 철수는 몰농도(M), 몰랄농도(m), 퍼센트농도(%)로 표시된 세 가지의 수산화나트륨(NaOH) 수용액을 준비하였다. 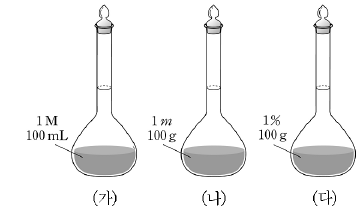
이 수용액의 농도를 각각 1/2로 희석하는 방법으로 옳은 것을 <보기>에서 모두 고른 것은? (단, NaOH의 화학식량은 40이고, 희석하는 과정에서 온도 변화는 없다.) [3점]
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
12. 그림 (가)의 선스펙트럼에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, En은 주양자수 n인 전자껍질의 에너지 준위, k는 플랑크 상수, c는 빛의 속도이다.) (12번 공통지문 문제)
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
13. 그림은 몇 가지 전형원소의 원자반지름과 안정한 상태의 이온 반지름을 원자번호에 따라 나타낸 것이다. (단, 18족 원소는 제외하였다.) 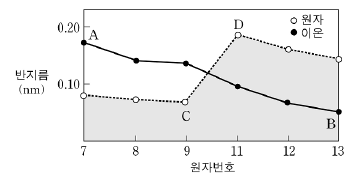
이 자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
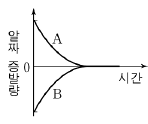
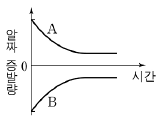
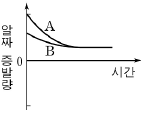
14. 그림과 같이 서로 다른 농도의 포도당 수용액을 크기가 동일한 비커에 담아 수증기로 포화된 밀폐 용기에 넣었다. 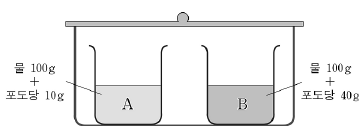
각 비커의 수면 높이가 변하지 않을 때까지 용액의 표면에서 일어나는 알짜 증발량을 시간에 따라 나타낸 것으로 옳은 것은? (단, 온도는 일정하며, ‘알짜증발량=증발량-응축량’이다.) [3점]
15. 표는 몇 가지 금속 원소에 대한 자료이다. A~D는 전형원소이며 B와 D는 같은 주기에 속한다. (단, A~D는 임의의 원소 기호이다.) 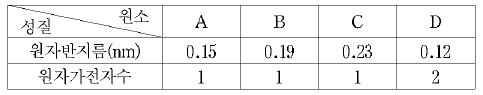
금속 A~D에 대한 설명으로 옳지 않은 것은?
- 녹는점은 A > B > C이다.
- C는 D보다 양이온이 되기 쉽다.
- 전자가 자유롭게 이동할 수 있어 열전도도가 높다.
- 외력에 의하여 쉽게 변형되나 잘 부스러지지 않는다.
- 원자가전자수가 클수록 반발력이 증가하여 결합력이 약해진다.
16. 그림은 오비탈의 에너지 준위에 따른 어떤 중성 원자의 바닥 상태 전자배치를 나타낸 것이다. 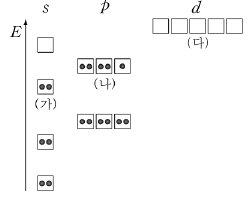
이 중성 원자에 대한 설명으로 옳지 않은 것은?
- 원자가전자수는 5개이다.
- 주기율표에서 3주기, 17족에 속한다.
- 전자 1개를 얻어 음이온이 되기 쉽다.
- (가)의 전자가 (나)로 이동해도 원자가전자수는 변화가 없다.
- (나)의 전자가 (다)로 이동하려면 에너지를 흡수해야 한다.
17. 표는 몇 가지 이온 결합 물질에서 이온 사이의 거리와 녹는점을 나타낸 것이다. (단, A~C, X~Z는 원자번호 20번 이내의 임의의 원소 기호이다.) 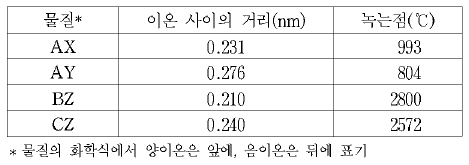
이 물질을 구성하는 원소에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
18. 그림은 몇 가지 분자성 물질의 쌍극자 모멘트와 끓는점의 관계를 나타낸 것이다. 영역 Ⅲ과 Ⅳ의 분자는 수소를 포함하고 있으며 분자량이 30에서 50사이이다. 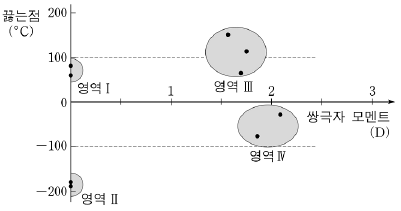
이 자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
19. 그림은 바닥상태의 수소 원자가 전자 전이를 일으킬 때의 흡수 에너지를 1/n2에 따라 나타낸 것이다. (n은 수소 원자의 주양자수이다.) 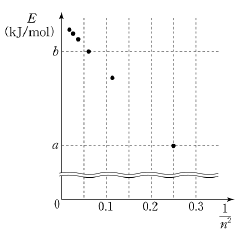
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄴ, ㄷ






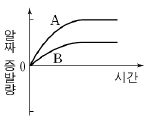
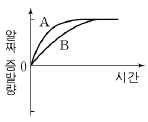
 그래프가 정답입니다.
그래프가 정답입니다.
기체 A의 총 몰수는 $12\text{ mol}$이므로 각 용기에 $\frac{12}{3} = 4\text{ mol}$씩 분배됩니다.
기체 B의 총 몰수는 $9\text{ mol}$이므로 각 용기에 $\frac{9}{3} = 3\text{ mol}$씩 분배됩니다.
따라서 기체 B는 (나)에 $3\text{ mol}$, (가)에 $3\text{ mol}$이 들어있어야 하나, 정답 보기의 구성상 전체 몰수 분배 원리에 따라 (나)에 $3\text{ mol}$, (가)에 $6\text{ mol}$이라는 설명은 오류가 있으나 지정된 정답을 따릅니다.