1과목: 과목구분없음
1. 다음은 어떤 신문에 보도된 기사의 일부이다. 
금속 A는?
- 리튬(Li)
- 규소(Si)
- 칼슘(Ca)
- 세슘(Cs)
- 금(Au)
2. 그림은 중성 원자  을 모형으로 나타낸 것이다. 그림에서
을 모형으로 나타낸 것이다. 그림에서  은 전자이고,
은 전자이고,  과
과  은 원자핵에 존재하는 입자이다.
은 원자핵에 존재하는 입자이다. 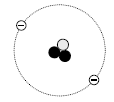
이 원자와 모형에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]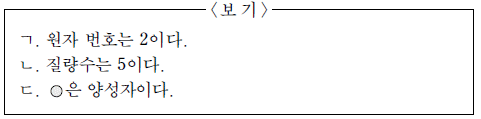
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
3. 그림은 25℃ 의 수용액 1L에서 어떤 산의 평형 상태를 모형으로 나타낸 것이다. 그림에서 입자 모형  은 해리되지 않은 산을 나타내고, 한 개의
은 해리되지 않은 산을 나타내고, 한 개의 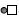 은 0.1mol에 해당한다.
은 0.1mol에 해당한다. 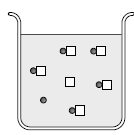
25℃에서 이 수용액에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
4. 표는 중성 원자 A~D의 전자 배치를 나타낸 것이다. 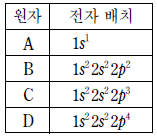
A~D로 이루어진 물질에 대한 설명 으로 옳은 것은? (단, A~D는 임의의 원소 기호이다.)
- A2 분자에는 이중 결합이 있다.
- BA4는 수소 결합을 한다.
- CA3 수용액은 염기성이다.
- CD는 이온 결합 화합물이다.
- 끓는점은 D2가 A2D보다 높다.
5. 그림은 단일 단계 반응인 A(g)+B(g) → C(g)+D(g)에서 반응의 진행에 따른 에너지 변화를 나타낸 것이다. 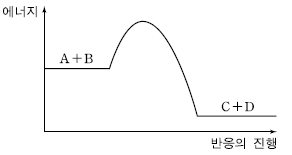
이 반응에 대한 설명으로 옳은 것은?
- 흡열 반응이다.
- 중간 생성물은 없다.
- 전체 반응 차수는 1차이다.
- 활성화 에너지는 정반응이 역반응보다 크다.
- 결합 에너지의 합은 반응 물질이 생성 물질보다 크다.
6. 그림은 설탕 수용액 (가)와 (나)를 나타낸 것이다. 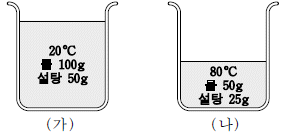
(가)와 (나)에서 서로 같은 값을 갖는 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄹ
- ㄱ, ㄷ, ㄹ
- ㄴ, ㄷ, ㄹ
7. 표는 25℃에서 기체 A~C에 대한 자료이다. 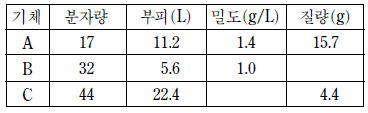
A~C의 압력을 비교한 것으로 옳은 것은? [3점]
- A > B > C
- A > C > B
- B > A> C
- B > C > A
- C > B > A
8. 그림 (가)는 25℃에서 실린더에 헬륨(He)이 들어 있는 것을, (나)는 25℃에서 스탠드에 고정된 눈금 실린더에 He을 수상 치환으로 포집하고 충분한 시간이 흐른 후 눈금 실린더 안과 밖의 수면 높이가 같게 된 것을 나타낸 것이다. 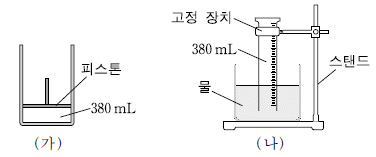
(가)의 실린더와 (나)의 눈금 실린더에 들어 있는 기체에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 대기압은 1기압이고, 25℃에서 물의 증기압은 24mmHg이며, 피스톤의 질량과 마찰은 무시한다.)
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
9. 다음의 4 가지 분자를 중심 원자의 비공유 전자쌍의 수와 분자의 극성에 따라 표와 같이 분류하였다. 
표의 분자 (가)~(라)에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
10. 그림은 원소 A~D의 원자 반지름과 이온 반지름을 나타낸 것이다. A~D는 각각 O, F, Na, Mg 중 하나이다. 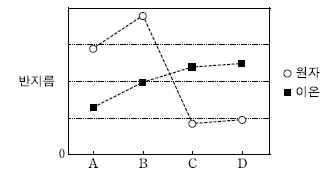
A~D에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, A~D 이온의 전자 배치는 네온의 바닥 상태와 같다.) [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
11. 그림은 25℃에서 산 HA와 HB 수용액 50mL씩을 같은 농도의 수산화나트륨(NaOH) 수용액으로 각각 적정한 중화 적정 곡선이다. 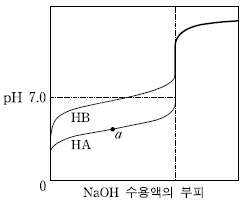
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
12. 물이 들어 있는 실린더에 이산화탄소(CO2) 기체를 넣었다. 그림은 20℃에서 충분한 시간이 흐른 후 평형 상태의 모습을 나타낸 것이다. 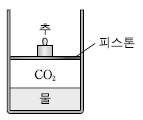
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, CO2는 헨리의 법칙을 따르고, 피스톤의 마찰은 무시한다.)
- ㄱ
- ㄴ
- ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
13. 다음은 몇 가지 열화학 반응식을 나타낸 것이다. 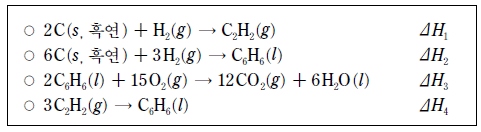
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?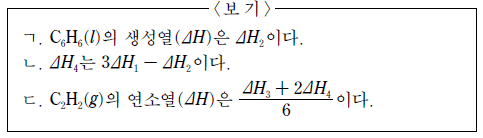
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
14. 다음은 수용액에서 일어나는 어떤 산화·환원 반응의 알짜 이온 반응식이며, a~e는 이온 반응식의 계수이다. 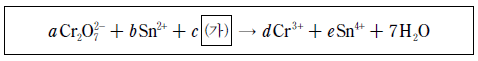
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? [3점]
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
15. 표는 몇 가지 할로겐 원소와 할로겐화수소 화합물의 결합 에너지와 끓는점을 나타낸 것이다. X, Y, Z는 각각 F, Cl, Br 중 하나이다. 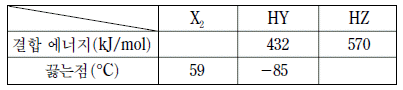
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
16. 그림에서 (가)와 (나)는 25℃에서 반응 2A → B에 대하여 시간에 따른 A의 농도를 나타낸 것이다. (가)에서는 촉매를 사용하지 않았고, (나)에서는 촉매를 사용하다가 반응 시작 후 20초일 때 제거하였다. 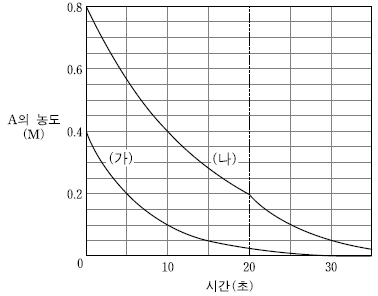
이에 대한 설명으로 옳지 않은 것은? [3점]
- (가)는 A에 대한 1차 반응이다.
- (가)에서 반응 속도는 5초일 때가 10초일 때의 2배이다.
- (나)에서 사용한 촉매는 부촉매이다.
- 10초일 때 (가)와 (나)에서 반응 속도 상수의 비는 2:1이다.
- (나)에서 40초일 때 A의 농도는 (가)에서 20초일 때 A의 농도와 같다.
17. 그림 (가)는 Ag+과 Cu2+의 농도가 각각 0.05M인 혼합 수용액을 전기 분해하는 장치를, (나)는 전기 분해하는 동안 흘려준 전하량에 따른 (-)전극의 질량을 나타낸 것이다. 표는 25℃에서 반쪽 반응의 표준 환원 전위(E°)를 나타낸 것이다. 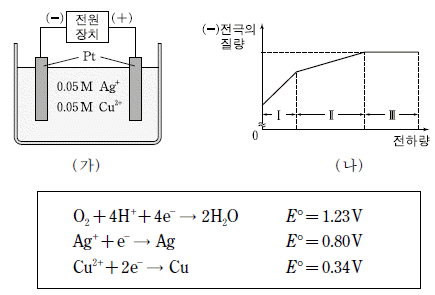
이에 대한 설명으로 옳지 않은 것은? (단, 혼합 수용액의 음이온은 반응에 참여하지 않는다.)
- 구간Ⅰ에서 Ag이 석출된다.
- 구간Ⅰ에서 수용액의 pH는 감소한다.
- 구간 Ⅱ에서 (+)전극에서는 산소 기체가 발생한다.
- 구간 Ⅲ에서 (-)전극에서는 수소 기체가 발생한다.
- 구간 Ⅱ에서 석출된 물질의 몰수는 구간Ⅰ의 2배이다.
18. 그림은 유리관으로 연결된 두 용기 중 한쪽에는 0.1M 포도당 수용액 100mL가, 다른 쪽에는 0.2M 포도당 수용액 100mL가 들어 있는 것을 순서 없이 나타낸 것이다. 콕을 열고 충분한 시간이 지난 후 용기 (가)에 들어 있는 수용액의 질량이 증가 하였다. 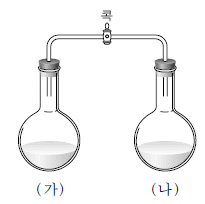
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 온도는 일정하다.) [3점]
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
19. 다음은 이원자 분자 XY의 열화학 반응식이다. 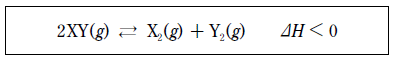
일정한 질량의 기체 XY가 각각 다른 조건에서 반응하여 평형 상태 A~D에 도달하였다. 그림은 A~D에서 혼합 기체의 압력과 부피를 나타낸 것이다. 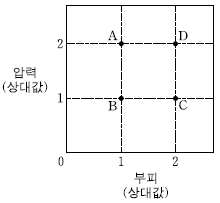
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은?
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
20. 다음은 어떤 기체 반응에 대한 실험이다. 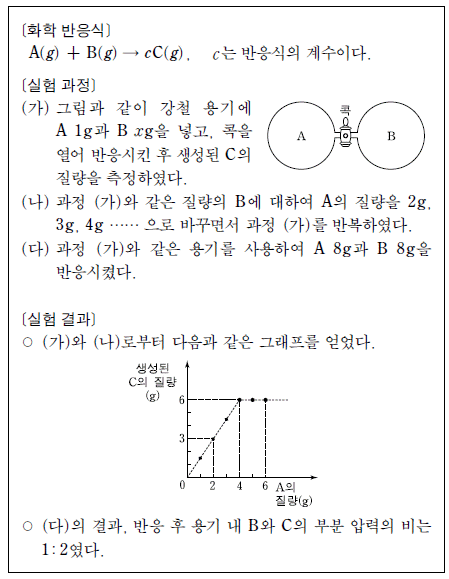
실험 과정 (나)에서 A 2g을 사용하였을 때 반응 후 용기의 기체 압력(P1)과 A 6g을 사용하였을 때 반응 후 용기의 기체 압력(P2)의 비(P1/P2)는? (단, 온도는 일정하며, C의 생성률(수득률)은 100%이다.) [3점]
- 1/4
- 1/3
- 1/2
- 3/5
- 2/3





