9급 지방직 공무원 화학 2016-06-18 필기 기출문제 해설
이 페이지는 9급 지방직 공무원 화학 2016-06-18 기출문제를 CBT 방식으로 풀이하고 정답 및 회원들의 상세 해설을 확인할 수 있는 페이지입니다.
9급 지방직 공무원 화학
(2016-06-18 기출문제)
목록
1과목: 과목 구분 없음
1. 다음 중 개수가 가장 많은 것은?
- 순수한 다이아몬드 12g 중의 탄소 원자
- 산소 기체 32g 중의 산소 분자
- 염화암모늄 1몰을 상온에서 물에 완전히 녹였을 때 생성되는 암모늄이온
- 순수한 물 18g 안에 포함된 모든 원자
2. 원소들의 전기음성도 크기의 비교가 올바른 것은?
- C < H
- S < P
- S < O
- Cl < Br
- 전기음성도는 같은 족에서 원자 번호가 작을수록(위로 갈수록) 큽니다. S와 O는 같은 16족 원소이며, O가 S보다 위에 위치하므로 전기음성도가 더 큽니다.
오답 노트
C < H: 탄소(C)가 수소(H)보다 전기음성도가 큼
S < P: 황(S)이 인(P)보다 전기음성도가 큼
Cl < Br: 염소(Cl)가 브롬(Br)보다 전기음성도가 큼
3. 1MFe(NO3)2 수용액에서 음이온의 농도는? (단, Fe(NO3)2는 수용액에서 100% 해리된다)
- 1M
- 2M
- 3M
- 4M
- $\text{Fe}(\text{NO}_3)_2$가 수용액에서 100% 해리되면, 1몰의 $\text{Fe}(\text{NO}_3)_2$당 2몰의 $\text{NO}_3^-$이온이 생성됩니다.
① [기본 공식] $\text{음이온 농도} = \text{화합물 농도} \times \text{음이온 수}$
② [숫자 대입] $\text{음이온 농도} = 1\text{M} \times 2$
③ [최종 결과] $\text{음이온 농도} = 2\text{M}$
4. 밑줄 친 원자(C, Cr, N, S)의 산화수가 옳지 않은 것은?
- HCO3-, +4
- Cr2O72-, +6
- NH4+, +5
- SO42-, +6
- 화합물이나 이온에서 각 원자의 산화수 합은 전체 전하량과 같아야 합니다.
$\text{NH}_{4}^{+}$이온에서 수소($\text{H}$)의 산화수는 $+1$이며, 질소($\text{N}$)의 산화수를 $x$라고 할 때 전체 전하량은 $+1$이 되어야 합니다.
$$x + (1 \times 4) = +1$$
$$x = -3$$
따라서 질소의 산화수는 $-3$이므로 $+5$라는 설명은 옳지 않습니다.
5. 90g의 글루코오스(C6H12O6)와 과량의 산소(O2)를 반응시켜 이산화탄소(CO2)와 물(H2O)이 생성되는 반응에 대한 설명으로 옳지 않은 것은? (단, H, C, O의 몰 질량[g/mol]은 각각 1, 12, 16이다)
- x와 y에 해당하는 계수는 모두 6이다.
- 90g 글루코오스가 완전히 반응하는데 필요한 O2의 질량은 96g이다.
- 90g 글루코오스가 완전히 반응해서 생성되는 CO2의 질량은 88g이다.
- 90g 글루코오스가 완전히 반응해서 생성되는 H2O의 질량은 54g이다.
- 글루코오스의 완전 연소 반응식 $\text{C}_6\text{H}_{12}\text{O}_6 + 6\text{O}_2 \rightarrow 6\text{CO}_2 + 6\text{H}_2\text{O}$를 바탕으로 화학 양론을 계산합니다. 글루코오스의 몰 질량은 $180\text{g/mol}$이므로 $90\text{g}$은 $0.5\text{mol}$입니다.
생성되는 $\text{CO}_2$의 질량 계산:
① [기본 공식] $\text{mass} = \text{mol} \times \text{molar mass}$
② [숫자 대입] $\text{mass} = (0.5 \times 6) \times 44$
③ [최종 결과] $\text{mass} = 132$
따라서 $\text{CO}_2$의 질량은 $132\text{g}$이어야 하므로 $88\text{g}$이라는 설명은 틀렸습니다.
6. 묽은 설탕 수용액에 설탕을 더 녹일 때 일어나는 변화를 설명한 것으로 옳은 것은?
- 용액의 증기압이 높아진다.
- 용액의 끓는점이 낮아진다.
- 용액의 어는점이 높아진다.
- 용액의 삼투압이 높아진다.
- 용질의 농도가 증가하면 총괄성 효과가 커집니다. 삼투압은 용액의 몰 농도에 비례하여 증가합니다.
오답 노트
용액의 증기압이 높아진다: 농도가 높을수록 증기압 내림 현상으로 인해 증기압은 낮아짐
용액의 끓는점이 낮아진다: 끓는점 오름 현상으로 인해 끓는점은 높아짐
용액의 어는점이 높아진다: 어는점 내림 현상으로 인해 어는점은 낮아짐
7. 다음의 화합물 중에서 원소 X가 산소(O)일 가능성이 가장 낮은 것은? (단, O의 몰 질량[g/mol]은 16이다)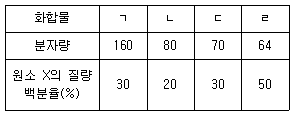
- ㄱ
- ㄴ
- ㄷ
- ㄹ
- 화합물의 분자량과 질량 백분율을 이용하여 원소의 몰 질량을 계산하는 문제입니다.
원소 $\text{X}$가 산소($\text{O}$)라면, 해당 화합물 내 $\text{X}$의 총 질량이 산소의 몰 질량인 $16$의 배수가 되어야 합니다.
각 화합물 내 $\text{X}$의 질량 계산: $\text{분자량} \times \frac{\text{질량 백분율}}{100}$
ㄱ. $160 \times 0.3 = 48$ ($16 \times 3$, 가능)
ㄴ. $80 \times 0.2 = 16$ ($16 \times 1$, 가능)
ㄷ. $70 \times 0.3 = 21$ ($16$의 배수 아님, 불가능)
ㄹ. $64 \times 0.5 = 32$ ($16 \times 2$, 가능)
8. 대기 오염 물질인 기체 A, B, C가 <보기 1>과 같을 때 <보기 2>의 설명 중 옳은 것만을 모두 고른 것은?
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
- 기체의 특성을 통해 물질을 식별하고 성질을 분석하는 문제입니다.
제시된 조건에 따라 $\text{A} = \text{CO}$ (일산화탄소), $\text{B} = \text{SO}_x$ (황산화물), $\text{C} = \text{O}_3$ (오존)임을 알 수 있습니다.
ㄱ. $\text{CO}$는 헤모글로빈과의 결합력이 산소보다 훨씬 강해 쉽게 해리되지 않으므로 옳습니다.
ㄴ. $\text{SO}_x$는 비금속 산화물로, 물에 녹으면 산성 수용액을 형성하므로 옳습니다.
ㄷ. $\text{O}_3$를 구성하는 원소는 산소($\text{O}$) 한 가지뿐이므로 틀렸습니다.
9. 다음 중 분자 구조가 나머지와 다른 것은?
- BeCl2
- CO2
- XeF2
- SO2
- 분자의 기하학적 구조를 구분하는 문제입니다.
$\text{BeCl}_2$, $\text{CO}_2$, $\text{XeF}_2$는 모두 중심 원자에 비공유 전자쌍이 없거나(Be, C) 대칭적으로 배치되어(Xe) 직선형 구조를 가집니다.
반면 $\text{SO}_2$는 중심 원자인 황(S)에 비공유 전자쌍이 존재하여 전자쌍 반발 원리에 의해 굽은형 구조를 가집니다.
10. van der Waals 상태방정식 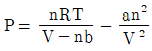 에 대한 설명으로 옳은 것만을 모두 고른 것은? (단, P, V, n, R, T는 각각 압력, 부피, 몰수, 기체상수, 온도이다)
에 대한 설명으로 옳은 것만을 모두 고른 것은? (단, P, V, n, R, T는 각각 압력, 부피, 몰수, 기체상수, 온도이다)
- ㄱ, ㄷ
- ㄴ, ㄹ
- ㄱ, ㄷ, ㄹ
- ㄱ, ㄴ, ㄷ, ㄹ
- 반데르발스 상태방정식 $P = \frac{nRT}{V - nb} - \frac{an^2}{V^2}$에서 각 상수의 의미와 특성을 분석합니다.
ㄱ. $a$는 분자 간 인력을 보정하는 상수로, 인력이 클수록 $a$값이 큽니다.
ㄴ. $b$는 분자 자체의 부피(반발력과 관련)를 보정하는 상수로, 분자 크기가 클수록 $b$값이 큽니다.
ㄷ. $H_2O(g)$는 $H_2S(g)$보다 수소 결합 등의 인력이 훨씬 강하므로 $a$값이 더 큽니다.
ㄹ. $Cl_2(g)$ 분자가 $H_2(g)$ 분자보다 크기가 훨씬 크므로 $b$값이 더 큽니다.
11. 다음 반응에 대한 평형상수는?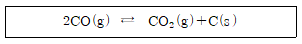
- K=[CO2]/[CO]2
- K=[CO]2/[CO2]
- K=[CO2][C]/[CO]2
- K=[CO]2/[CO2][C]
- 평형상수 식을 세울 때, 고체($s$)나 순수한 액체는 농도 변화가 거의 없으므로 식에서 제외하고 기체($g$) 성분만 고려합니다.
반응식 $2CO(g) \rightleftharpoons CO_2(g) + C(s)$에서 고체인 $C(s)$를 제외하면 평형상수 $K$는 다음과 같습니다.
$$K = \frac{[CO_2]}{[CO]^2}$$
12. 질량 백분율이 N 64%, O 36%인 화합물의 실험식은? (단, N, O의 몰 질량[g/mol]은 각각 14, 16이다)
- N2O
- NO
- NO2
- N2O5
- 화합물 100g이 있다고 가정하여 각 원소의 몰수 비를 통해 가장 간단한 정수비인 실험식을 구합니다.
① [기본 공식] $\text{몰수} = \frac{\text{질량}}{\text{몰 질량}}$
② [숫자 대입] $N : O = \frac{64}{14} : \frac{36}{16} = 4.57 : 2.25$
③ [최종 결과] $N : O = 2 : 1$
따라서 실험식은 $N_2O$ 입니다.
13. 25°C에서 [OH-]=2.0×10-5M일 때, 이 용액의 pH값은? (단, log2=0.30이다)
- 2.70
- 4.70
- 9.30
- 11.30
- 수소이온농도지수 $pH$를 구하기 위해 먼저 $pOH$를 계산한 후, $pH + pOH = 14$ 관계식을 이용합니다.
① [기본 공식] $pOH = -\log[OH^-]$
② [숫자 대입] $pOH = -\log(2.0 \times 10^{-5}) = 5 - \log 2 = 5 - 0.30$
③ [최종 결과] $pOH = 4.70$
따라서 $pH = 14 - 4.70 = 9.30$ 입니다.
14. 온도가 400K이고 질량이 6.00kg인 기름을 담은 단열 용기에 온도가 300K이고 질량이 1.00kg인 금속공을 넣은 후 열평형에 도달했을 때, 금속공의 최종 온도[K]는? (단, 용기나 주위로 열 손실은 없으며, 금속공과 기름의 비열[J/(kg·K)]은 각각 1.00과 0.50로 가정한다)
- 350
- 375
- 400
- 450
- 단열 용기 내에서 고온의 기름이 잃은 열량은 저온의 금속공이 얻은 열량과 같습니다. 열평형 온도 $T_f$를 구하는 에너지 보존 법칙을 적용합니다.
① [기본 공식]
$$m_1 c_1 (T_1 - T_f) = m_2 c_2 (T_f - T_2)$$
② [숫자 대입]
$$6.00 \times 0.50 \times (400 - T_f) = 1.00 \times 1.00 \times (T_f - 300)$$
③ [최종 결과]
$$T_f = 375$$
15. 아래 반응에서 산화되는 원소는?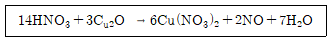
- H
- N
- O
- Cu
- 반응식 $14\text{HNO}_3 + 3\text{Cu}_2\text{O} \rightarrow 6\text{Cu}(\text{NO}_3)_2 + 2\text{NO} + 7\text{H}_2\text{O}$에서 각 원소의 산화수를 분석합니다.
반응물 $\text{Cu}_2\text{O}$에서 $\text{Cu}$의 산화수는 $+1$이며, 생성물 $\text{Cu}(\text{NO}_3)_2$에서 $\text{Cu}$의 산화수는 $+2$로 증가하였습니다. 산화수가 증가한 원소가 산화된 것이므로 정답은 $\text{Cu}$입니다.
16. 다음 그림은 어떤 반응의 자유에너지 변화(△G)를 온도(T)에 따라 나타낸 것이다. 이에 대한 설명으로 옳은 것만을 모두 고른 것은? (단, △H는 일정하다)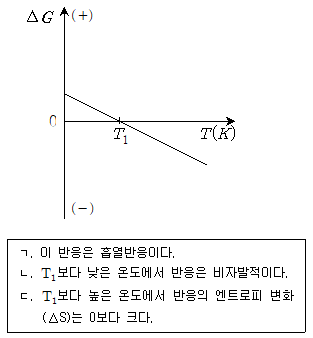
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
- 자유에너지 변화 $\Delta G$와 온도 $T$의 관계를 분석하면 다음과 같습니다.
ㄱ. 온도가 상승함에 따라 $\Delta G$가 감소하여 자발적 반응($\Delta G < 0$)으로 변하므로, 이는 $\Delta H > 0$인 흡열반응입니다.
ㄴ. 그래프에서 $T_1$보다 낮은 온도 영역에서는 $\Delta G$ 값이 0보다 크므로 비자발적 반응입니다.
ㄷ. $\Delta G = \Delta H - T\Delta S$ 식에서 기울기가 음수($\text{-}\Delta S$)이므로, $\Delta S$는 0보다 큽니다.
따라서 ㄱ, ㄴ, ㄷ 모두 옳습니다.
17. 이온성 고체에 대한 설명으로 옳은 것은?
- 격자에너지는 NaCl이 NaI보다 크다.
- 격자에너지는 NaF가 LiF보다 크다.
- 격자에너지는 KCl이 CaCl2보다 크다.
- 이온성 고체는 표준생성엔탈피(△Hfo)가 0보다 크다.
- 격자에너지는 이온 반지름이 작을수록, 전하량이 클수록 증가합니다. $\text{NaCl}$의 $\text{Cl}$이 $\text{NaI}$의 $\text{I}$보다 반지름이 작으므로 격자에너지는 $\text{NaCl}$이 더 큽니다.
오답 노트
NaF가 LiF보다 크다: $\text{Li}$가 $\text{Na}$보다 반지름이 작아 $\text{LiF}$가 더 큼
KCl이 $\text{CaCl}_2$보다 크다: $\text{Ca}^{2+}$가 $\text{K}^+$보다 전하량이 커서 $\text{CaCl}_2$가 더 큼
표준생성엔탈피가 0보다 크다: 이온성 고체는 일반적으로 매우 안정하여 $\Delta H_f^o$가 0보다 작음
18. 철(Fe)로 된 수도관의 부식을 방지하기 위하여 마그네슘(Mg)을 수도관에 부착하였다. 산화되기 쉬운 정도만을 고려할 때, 마그네슘 대신에 사용할 수 없는 금속은?
- 아연(Zn)
- 니켈(Ni)
- 칼슘(Ca)
- 알루미늄(Al)
- 철(Fe)의 부식을 방지하기 위해서는 철보다 반응성이 커서 대신 산화되는 금속(희생 양극법)을 사용해야 합니다. 니켈(Ni)은 철보다 반응성이 낮아 철 대신 산화될 수 없으므로 사용할 수 없습니다.
19. 다음 반응은 300K의 밀폐된 용기에서 평형상태를 이루고 있다. 이에 대한 설명으로 옳은 것만을 모두 고른 것은? (단, 모든 기체는 이상기체이다)
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄹ
- ㄷ, ㄹ
- 반응식 $\text{A}_2(\text{g}) + \text{B}_2(\text{g}) \rightleftharpoons 2\text{AB}(\text{g})$ $\Delta\text{H} = 150\text{kJ/mol}$은 흡열 반응입니다.
온도가 낮아지면 르샤틀리에 원리에 의해 열을 발생하는 역반응 방향으로 이동하며, $\text{B}_2$ 기체를 추가하면 이를 소모하는 정반응 방향으로 이동합니다.
오답 노트
부피 감소: 반응 전후 기체 분자 수 변화가 없으므로 평형 이동 없음
촉매 추가: 반응 속도만 빠르게 할 뿐 평형의 위치는 변화시키지 않음
20. 다음은 화합물 AB의 전자 배치를 모형으로 나타낸 것이다. 이에 대한 설명으로 옳은 것은? (단, A, B는 각각 임의의 금속, 비금속 원소이다)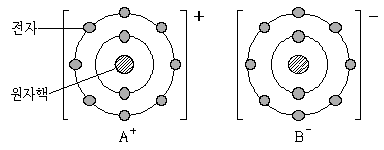
- 화합물 AB의 몰 질량은 20g/mol이다.
- 원자 A의 원자가 전자는 1개이다.
- B2는 이중 결합을 갖는다.
- 원자 반지름은 B가 A보다 더 크다.
- 제시된 모형에서 $\text{A}^+$는 전자를 하나 잃어 옥텟 규칙을 만족한 상태이므로, 중성 원자 A의 원자가 전자는 1개입니다.
오답 노트
몰 질량: A와 B의 정확한 원소 종류를 알 수 없어 계산 불가
$\text{B}_2$ 결합: B는 7족 원소(F 등)로 단일 결합을 형성함
원자 반지름: 금속인 A가 비금속인 B보다 반지름이 더 큼






- 순수한 다이아몬드 12g: $\frac{12}{12} = 1\text{ mol}$ (탄소 원자)
- 산소 기체 32g: $\frac{32}{32} = 1\text{ mol}$ (산소 분자)
- 염화암모늄 1몰: $1\text{ mol}$ (암모늄 이온)
- 순수한 물 18g: $\frac{18}{18} = 1\text{ mol}$ (물 분자) $\rightarrow$ 물 분자 1개당 원자가 3개($H_2O$)이므로 총 원자 수는 $3\text{ mol}$
따라서 원자 수가 $3\text{ mol}$인 순수한 물 18g 안에 포함된 모든 원자가 가장 많습니다.