1과목: 과목구분없음
1. 표는 몇 가지 고체 물질의 온도에 따른 용해도(g/물100g)를 나타낸 것이다. 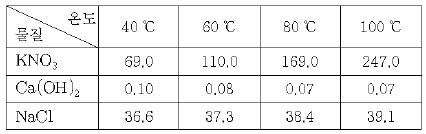
자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
2. 부피가 같은 두 개의 용기에 수소(H2)기체와 산소(O2)기체가 그림과 같이 들어있다. 콕을 열어 기체를 혼합시킨 다음 점화 장치를 이용하여 두 기체를 완전히 반응시켰다. 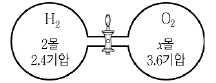
실험에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, 반응 전·후 기체의 온도는 400K를 유지하였으며 연결관의 부피는 무시한다.) [3점]
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
3. 그림은 일정한 온도에서 1몰의 이상기체와 1몰의 이산화황(SO2)에 대한 압력과 부피와의 관계를 나타낸 것이다. 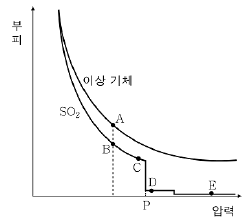
자료에 대한 설명으로 옳지 않은 것은? [3점]
- SO2몰을 사용하면 P점의 값은 2배가 된다.
- A점보다 B점의 부피가 작은 것은 분자간 인력 때문이다.
- B점과 C점에서 물질의 상태는 같다.
- C점에서 D점으로 가는 동안 상태 변화가 일어난다.
- E점이 D점보다 분자간 거리가 가깝다.
4. 그림은 서로 다른 온도에서 에탄올의 증기압을 측정한 실험 결과를 나타낸 것이다. 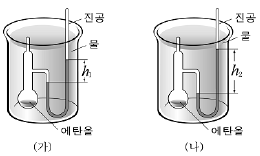
(가)와 (나)에 들어있는 에탄올에 대해 비교한 내용으로 옳지 않은 것은?
- 온도 : 가 < 나
- 증발 속도 : 가 < 나
- 응축 속오 : 가 > 나
- 증기 분자수 : 가 < 나
- 액체 상태에서의 분자간 인력 : 가 > 나
5. 그림의 비커에 들어 있는 용액에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? 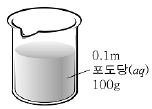
(단, 포도당의 분자량은 180이고, 물의 몰랄 오름 상수는 0.52℃/m이다.)
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
6. 다음은 용매와 용액의 증기압을 비교하기 위한 실험이다. 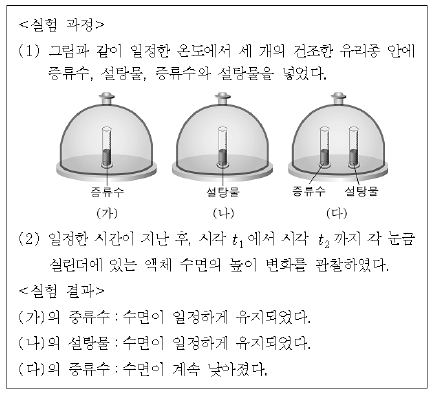
시각 t2에서 유리종 (가)~(다)의 수증기 압력과 관련된 옳은 설명을 <보기>에서 모두 고른 것은? (단, 설탕물의 처음 농도는 같다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
7. 그림은 원자 번호가 연속된 일부 원소들의 제1이온화 에너지(E1)와 제2이온화 에너지(E2)를 원자번호 순서에 따라 나타낸 것이다. (단, A~C는 원소를 나타낸 임의의 기호이다.) 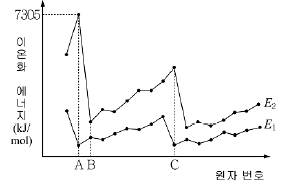
위 자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
8. 그림은 몇 가지 입자들의 모형을 나타낸 것이다. 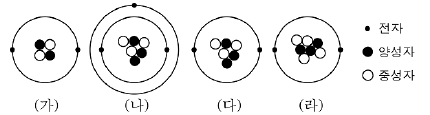
입자 (가)~(라)에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
9. 그림은 A의 분자량을 알아보기 위해 삼투압을 측정하는 실험 장치이다. 
이 실험에서 용질 A의 분자량이 실제보다 크게 측정되는 원인이 될수 있는 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
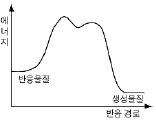
10. 그림은 분자 A2, B2, AB가 생성되는 과정에서 두 원자의 핵간 거리에 따른 에너지의 변화를 나타낸 것이다. 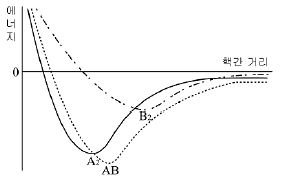
자료로부터 알수 있는 옳은 내용을 <보기>에서 모두 고른 것은? (단, A, B는 원소를 나타내는 임의의 기호이다.)
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
11. 그림 (가)는 수소 원자의 2s오비탈에서 전자가 발견될 확률과 경계면을 그림 (나)는 수소 원자의 2p의 경계면을 나타낸 것이다. 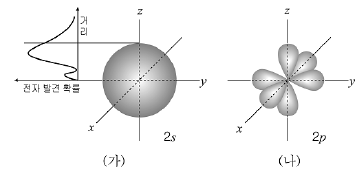
자료에 대한 설명으로 옳지 않은 것은? [3점]
- 에너지 준위는 2s와 2p가 같다.
- 2px와 2py 오비랄의 크기는 같다.
- 2px에서 전자가 발견될 확률은 원점 대칭이다.
- 2s 오비랄의 경계면에서 전자가 발견될 확률이 가장 높다.
- 2p에 전자가 존재할 수 있는 오비랄의 수는 2s의 3배이다.
12. 표는 에탄(C2H6)과 에틴(C2H2)에 관련된 몇 가지 열화학 반응식을 나열한 것이다. 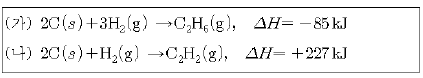
자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
13. 그림과 같이 pH가 다른 세 가지 용액이 있다. 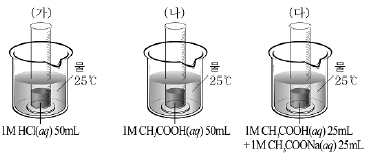
위 용액과 관련된 옳은 설명을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
14. 표는 몇 가지 물질들의 성질을 조사한 자료이다. 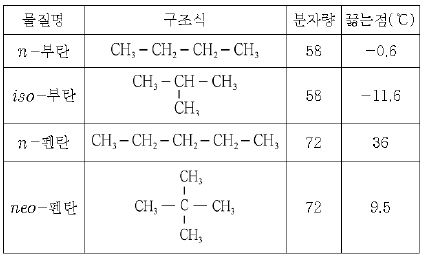
자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
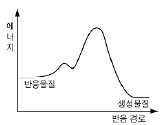
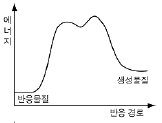
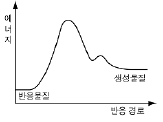
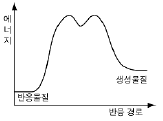
15. 다음은 RBr + H2O → ROH + H+ + Br-, △H < 0의 반응 메커니즘을 나타낸 것이다. 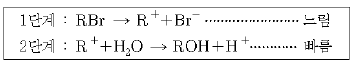
위 반응이 일어날 때 경로에 따른 에너지 변화를 가장 적절하게 나타낸 것은? (단, R은 알킬기를 의미한다.)
16. 그림은 NF3, CF4, SF6의 분자 구조를 나타낸 것이다. 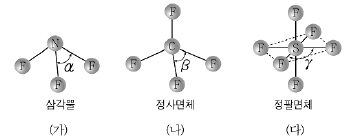
결합각 α ~ γ 중 가장 큰 것(A)과 무극성 분자(B)를 모두 골라 옳게 짝지은 것은? (순서대로 A, B)
17. 그림은 A(g)로부터 B(g)와 C(g)가 생성되는 반응에서 반응 용기 속에 들어있는 각 물질의 상대적인 농도 변화를 반응 시간에 따라 나타낸 것이다. 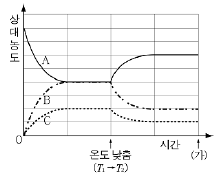
자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, A, B, C는 물질을 나타내는 임의의 기호이며 평형상수를 계산할 때 화학 반응식의 계수는 가장 간단한 정수비를 사용한다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
18. 그림은 백금 전극을 사용하여 Na2SO4(aq)과 CuCl2(aq)를 전기 분해하는 장치이다. 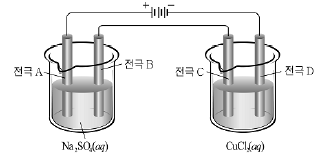
장치에 1F의 전하량을 통해 주었을 때 그 결과에 대한 설명으로 옳은 것은? [3점]
- 전극 A에서 발생된 기체의 부피는 0℃, 1기압에서 11.2L이다.
- 전극 B와 C에서 발생된 기체의 부피는 1 : 2이다.
- 전극 D에서 얻어진 금속 구리는 0.5몰이다.
- 전극 B에서는 산화 반응이 일어났다.
- 전극 A주변 용액의 pH는 커졌다.
19. 다음은 산과 염기의 중화 반응에 대한 실험이다. 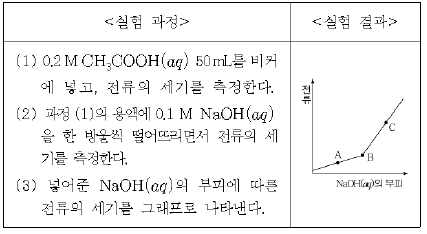
A~C점에서의 혼합용액에 대한 설명으로 옳은 것은? (단, CH3COOH(aq)과 NaOH(aq)의 처음 온도는 같다.) [3점]
- 생성된 물의 몰 수가 가장 큰 것은 A점의 용액이다.
- B점까지의 가해진 NaOH(aq)의 부피는 50mL이다.
- 용액의 온도가 가장 높은 것은 C점의 용액이다.
- 같은 부피에 들어있는 이온의 수는 A보다 B점의 용액이 적다.
- B점의 용액에 BTB용액을 떨어뜨리면 파란색이 나타난다.
20. 표는 수용액 상태에서 A와 B가 반응해서 C가 만들어지는 동안에 반응 용기 속에 들어있는 물질 A, B, C의 처음 농도와 60초 후의 농도를 측정한 결과이다. 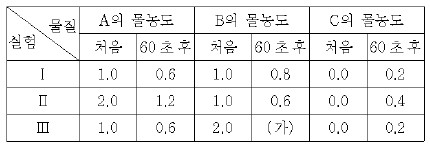
자료에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, A, B, C는 임의의 기호이며 반응이 일어나는 동안 온도는 일정하다.) [3점]
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ






 입니다.
입니다.

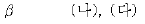
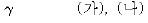
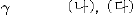
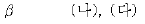 가 정답입니다.
가 정답입니다.
오답 노트
ㄱ. $40\text{°C}$ $\text{NaCl}$ 포화 용액의 농도는 $\frac{36.6}{100 + 36.6} \times 100 \approx 26.8\%$이므로 $36.6\%$가 아닙니다.
ㄴ. $60\text{°C}$ $\text{KNO}_3$ 포화 용액 $210\text{g}$은 용질 $110\text{g}$과 용매 $100\text{g}$으로 구성됩니다. 이를 $40\text{°C}$로 냉각하면 용해도가 $69.0\text{g}$으로 감소하므로 석출량은 다음과 같습니다.
① [석출량] = [처음 용질량] - [냉각 후 용해도]
② [석출량] = $110 - 69.0$
③ [석출량] = $41.0\text{g}$
ㄷ. $\text{KNO}_3$는 온도가 낮아질수록 용해도가 크게 감소하지만, $\text{Ca(OH)}_2$는 온도 변화에 따른 용해도 변화가 매우 작고 낮으므로 냉각 시 $\text{KNO}_3$가 주로 석출됩니다.