1과목: 과목구분없음
1. 그림은 동일한 두 비커에 어떤 순수한 액체 A와 B를 각각 같은 부피로 넣고 실온에 둔 후 일정한 시간이 경과하였을 때 A의 부피가 B보다 더 많이 줄어든 것을 나타낸 모습이다. 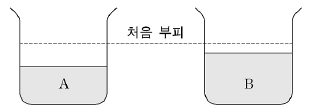
액체 A와 B의 성질을 비교한 것으로 옳은 것을 <보기>에서 고른 것은?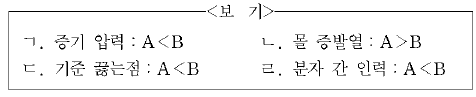
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄴ, ㄹ
- ㄷ, ㄹ
2. 그림은 몇 가지 수소 화합물의 분자량과 끓는점을 나타낸 것이다. 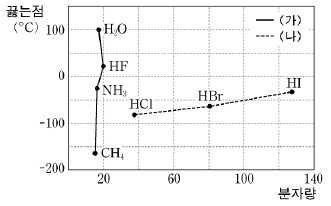
수소 화합물의 끓는점에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
3. 그림은 헬륨(He)과 아르곤(Ar)을 양쪽 용기에 각각 채우고 가운데 용기와 연결관을 진공으로 만든 상태를 나타낸 것이다. 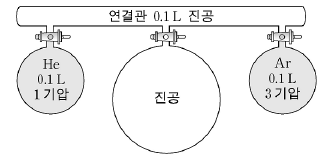
콕을 모두 열고 충분한 시간이 경과한 후 전체 압력이 0.4기압이 되었다면, 가운데 용기의 부피(V)와 헬륨이 부분 압력(PHe)으로 옳은 것은? (단, He과 Ar은 이상기체의 법칙을 따른다.) (순서대로 V, PHe)
- 0.7L, 0.1기압
- 0.7L, 0.3기압
- 0.8L, 0.1기압
- 0.8L, 0.2기압
- 0.8L, 0.3기압
4. 그림은 1기압에서 각각 1몰의 기체 A와 B의 온도에 따른 PV/RT 값을 나타낸 것이다. 
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
5. 표는 1기압에서 어떤 원소의 두 가지 동소체에 관한 자료이다. 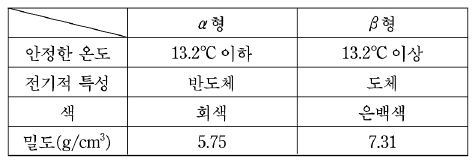
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
6. 그림은 산소 원자의 전자 배치를 전자껍질 모형 (가)와 오비탈 모형 (나)를 이용해 나타낸 것이다. 
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
7. 그림은 수소 방전관에서 나오는 가시광선 스펙트럼의 선의 위치를 나타낸 것이다. 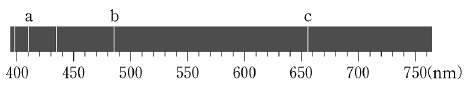
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
8. 그림과 같이 농도가 서로 다른 수산화나트륨(NaOH)수용액 (가)와 (나)를 부피 플라스크에 넣은 후 증류수를 가하여 1L의 용액 (다)를 만들었다. 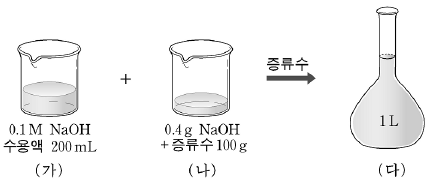
수용액 (다)의 몰 농도(M)는? (단, NaOH의 화학식량은 40이다.)
- 0.01M
- 0.02M
- 0.03M
- 0.04M
- 0.05M
9. 표는 3~4주기에 있는 임의의 원소 (가)~(다)의 자료를 나타낸 것이다. 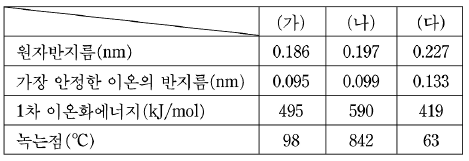
위의 자료에서 원소 (가)-(다)를 원자번호가 작은 것부터 커지는 순서대로 바르게 배열한 것은? [3점]
- 가-나-다
- 가-다-가
- 나-가-다
- 다-가-나
- 다-나-가
10. 그림은 5개의 분자를 어떤 기준에 따라 분류하는 과정을 나타낸 것이다. 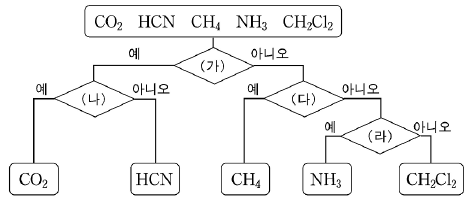
위의 (가)~(라)에 들어갈 기준으로 옳은 것을 <보기>에서 골라 순서대로 바르게 나타낸 것은? (순서대로 가, 나, 다, 라) [3점]
- ㄱ, ㄴ, ㄷ, ㄹ
- ㄴ, ㄹ, ㄹ, ㄷ
- ㄷ, ㄱ, ㄱ, ㄹ
- ㄷ, ㄹ, ㄱ, ㄹ
- ㄹ, ㄱ, ㄷ, ㄴ
11. 그림 (가)는 실온에서  반응의 혼합 기체가 a기압으로 평형을 이루고 있는 것을 (나)는 (가) 부피의 1/2이 되도록 피스톤을 고정시킨 후 새로운 평형 상태에 도달한 것을 나타낸 것이다.
반응의 혼합 기체가 a기압으로 평형을 이루고 있는 것을 (나)는 (가) 부피의 1/2이 되도록 피스톤을 고정시킨 후 새로운 평형 상태에 도달한 것을 나타낸 것이다. 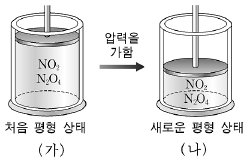
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, (가)와 (나)의 온도는 같다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
12. 다음은 비휘발성이고 비전해질인 A와 B 수용액의 어는점을 나타낸 것이다. 
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? (단, 물의 어는점 내림 상수 Kf=1.86℃/m이고 용질 A와 B는 서로 반응하지 않는다.) [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
13. 다음은 메탄의 브롬화 반응에 관련된 화학반응식과 그에 따른 반응열을 나타낸 것이다. 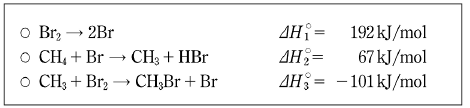
이 반응에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄴ
- ㄷ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
14. 다음은 이온 결정(NaCl, KCl)이 물에 용해되는 과정의 입자 모형과 몇 가지 에너지 변화값을 나타낸 것이다. 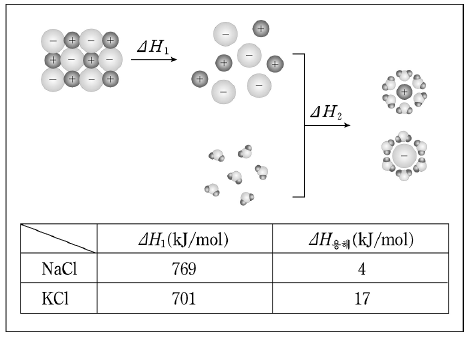
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄷ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
15. 다음은 일산화이질소(N2O) 기체의 분해 반응과 시간에 따른 N2O의 농도를 나타낸 것이다. k1과 k2는 각 단계의 반응 속도 상수이다. 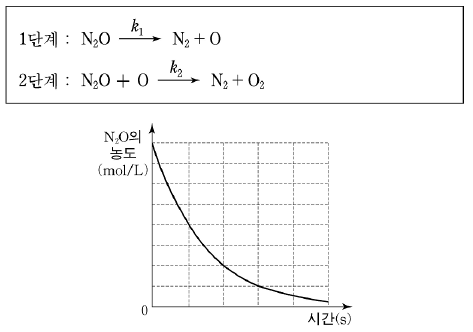
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
16. 다음은 25℃, 1기압에서 어떤 반응의 화학반응식과 몇 가지 물질의 반응열을 나타낸 것이다. 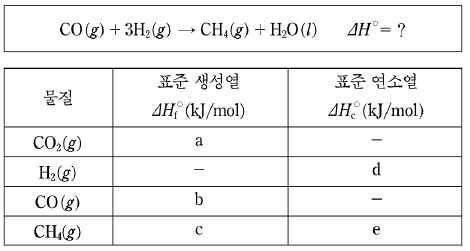
위 반응의 반응열(⊿H°)을 구하기 위해 주어진 자료에서 꼭 필요한 값을 모두 고른 것은? [3점]
- a, b, c
- b, c, d
- b, d, e
- a, b, c, e
- a, c, d, e
17. 다음은 0.1M 아세트산(CH3OOH) 수용액 100mL와 0.1M 아세트산나트륨(CH3OONa) 수용액 100mL를 혼합하여 만든 완충 용액에서 각 물질의 이온화 반응식을 나타낸 것이다. 
이에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은?
- ㄱ
- ㄴ
- ㄷ
- ㄱ, ㄷ
- ㄱ, ㄴ, ㄷ
18. 다음은 0.1M 수산화나트륨 수용액 20mL에 농도가 서로 다른 산을 가하면서 각각의 전류의 세기를 측정한 것이다. A는 묽은 염산을 B는 묽은 황산을 가할 때 얻어진 결과이다. 
위 실험에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄱ, ㄴ
- ㄱ, ㄷ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
19. 그림은 화학 전지 장치를 나타낸 것이고, 표는 이 반응의 표준 환원 전위 값을 나타낸 것이다. 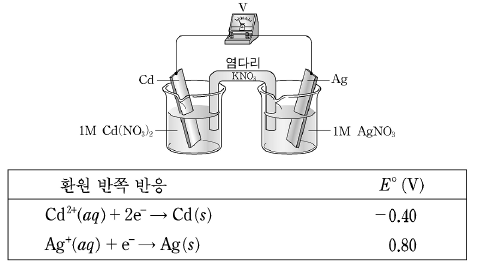
이 화학 전지에 대한 설명으로 옳은 것을 <보기>에서 모두 고른 것은? [3점]
- ㄱ
- ㄴ
- ㄱ, ㄴ
- ㄴ, ㄷ
- ㄱ, ㄴ, ㄷ
20. 그림은 염화구리(Ⅱ)수용액이 든 U자관에 구리 막대와 직류 전원 장치를 연결한 것을 표는 몇 가지 반응의 표준 환원 전위 값을 나타낸 것이다. 
위 장치의 스위치를 닫고 충분한 시간이 경과한 후, (-)극과 (+)극 구리 막대의 질량 변화로 옳은 것은? (순서대로 (-)극, (+)극)
- 감소, 증가
- 일정, 감소
- 일정, 일정
- 증가, 일정
- 증가, 감소






증발이 잘 된다는 것은 분자 간 인력이 약하고 증기압이 높다는 것을 의미합니다.
ㄷ. 액체 A가 더 많이 증발했으므로 A의 증기압이 B보다 큽니다. (옳음)
ㄹ. 증발이 잘 되는 A의 분자 간 인력이 B보다 작습니다. (옳음)
오답 노트
ㄱ. A의 증기압이 더 크므로 끓는점은 A가 더 낮습니다.
ㄴ. A의 분자 간 인력이 더 작으므로 표면 장력은 A가 더 작습니다.