1과목: 과목 구분 없음
1. 다음 중 기체상수 R의 단위로 가장 옳지 않은 것은?
- kg⋅m⋅K-1⋅mol-1
- L⋅atm⋅K-1⋅mol-1
- cal⋅K-1⋅mol-1
- lbf⋅ft⋅R-1⋅lbmol-1
2. 아래는 회분식반응기에서 일어나는 반응이다. 만일 반응기 내에 100mol의 A가 공급되어, 최종 생성물로서 10mol의 A와 160mol의 B 및 10mol의 C가 생성되었다고 할 때, 다음 중 옳은 것은?
- A의 전화율은 0.8이다.
- B의 수율은 90%이다.
- C에 대한 B의 선택도는 16molB/molC이다.
- 원하는 반응의 반응진행도(extent of reaction)는 90mol이다.
3. 반응식이 2NOCl →2NO + Cl2인 2차 반응에서, 반응속도상수가 0.01L/mol⋅s이고 NOCl의 초기 농도가 0.02mol/L라면, 20분 후 NOCl의 농도(mol/L)는 얼마인가? (단, 소수점 넷째자리에서 반올림한다.)
- 0.008mol/L
- 0.010mol/L
- 0.012mol/L
- 0.016mol/L
4. 다음 <보기>에서 농도에 대한 설명으로 옳은 것을 모두 고르면?
- 가, 나, 다
- 가, 다, 라
- 나, 다, 라
- 가, 나, 다, 라
5. NH3를 생산하기 위해 20gmol의 H2 기체와 10gmol의 N2 기체를 반응기에 공급하였다. 반응 전화율이 30%일 경우, 반응기에서 배출되는 NH3, H2, N2 기체 질량(g)의 총 합은 얼마인가? (단, 원자량은 N=14, H=1이다.)
- 180g
- 320g
- 550g
- 710g
6. 아래와 같이 관 내에 유체가 흐르고 있을 때 열린 마노미터는 16cmHg를 가리키고 있다. 관내 유체의 절대압력(cmHg)을 구하면? (단, 대기압은 1atm이다.)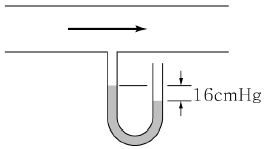
- 16cmHg
- 60cmHg
- 84cmHg
- 92cmHg
7. 관직경이 2mm, 운동 점도(kinematic viscosity)가 0.1cm2/s, Reynolds수가 2000일 때 유체의 부피유량(cm3/s)을 구하면? (단, π=3으로 계산한다.)
- 3cm3/s
- 30cm3/s
- 300cm3/s
- 3000cm3/s
8. 물의 높이가 항상 일정하게 유지되는 저수조에 구멍을 뚫었을 때, 그 구멍에서 유출되는 물의 유속(V)과 수면으로부터 구멍까지의 거리(Z)와의 관계를 바르게 나타낸 것은? (단, 압력차 및 마찰손실은 없다고 가정한다.)
- V는 Z1/2에 비례한다.
- V는 Z2에 비례한다.
- V는 lnZ에 비례한다.
- V는 Z와 관계없이 일정하다.
9. 다음 <보기>에서 열교환기에 대한 설명으로 옳은 것을 모두 고르면?
- 가, 다
- 나, 다
- 가, 다, 라
- 나, 다, 라
10. 이중관 열교환기의 내부관에 원유가 흐르면서 90°F에서 200°F로 가열된다. 외부관에서는 등유가 향류흐름형태로 흐르면서 400°F에서 110°F로 냉각된다. 열전달속도가 180,000Btu/hr, 열전달 면적이 23ft2인 경우 총괄열전달계수(Btu/hr⋅ft2⋅°F)는 얼마인가? (단, 장치 내에서 총괄열전달계수와 비열은 일정하다고 가정하며, ln10=2.3으로 계산한다.)
- 1
- 10
- 100
- 1000
11. 상률(phase rule)을 적용할 때, 다음 평형계의 자유도가 가장 작은 경우는?
- 얼음과 물의 혼합물
- 응축수와 평형상태에 있는 습한 공기(건조공기는 한 개의 성분으로 간주한다.)
- 총 4가지 성분의 탄화수소 기-액 혼합물
- 단일 반응 H2 + Br2 ⇄2HBr이 평형에 도달하여 H2, Br2 및 HBr 가스가 혼합되어 있는 계
12. 초기 균일 온도 80℃, 반지름이 1cm인 유리구슬을 0℃의 얼음물에 넣은 후, 5분 후에 구슬의 평균 온도가 20℃까지 떨어졌다. 만일 이 유리구슬의 반지름이 2cm로 커지면 동일한 조건 하에서 구슬의 평균 온도가 80℃에서 20℃까지 떨어지는데 걸리는 시간은? (이때 Bi값은 무한대라고 가정한다.)
- 5분
- 10분
- 20분
- 40분
13. 평판으로의 층류 열전달의 경우, 다음 중 국부 Nu수(Nux)를 바르게 표현한 식은 무엇인가? (단, hx : 국부 열전달계수, k : 열전도도, x : 평판 입구로부터 임의의 거리, y : x지점에서의 열경계층 두께)
- Nux = hxy/k
- Nux = k/hxy
- Nux = y/x
- Nux = x/y
14. 다음의 블록선도에서 입력 A에 대한 출력 B의 전달함수로 옳은 것은?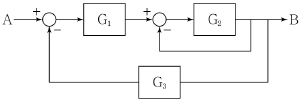
- G1G2/(1+G2+G1G2G3)
- G2/(1+G1G2+G1G2G3)
- G1G2/(1+G1G2G3)
- G2G2/(1+G1G2G3)
15. 환경오염 방지를 위해 2mol% 아세톤과 98mol% 공기가 포함되어 있는 화학공장의 배출가스를 아세톤 제거용 흡수탑에 통과시킨다. 흡수탑은 1.0×105Pa, 25℃에서 물을 향류로 흘려보내 아세톤을 제거한다. 이때, 2mol% 아세톤을 함유한 배출가스와 평형을 이룬 수용액상에서의 아세톤의 몰분율은? (단, 아세톤이 녹아 들어가는 수용액과 배출가스 간 아세톤 분포는 Raoult과 Dalton법칙이 적용되며, 25℃에서 아세톤의 증기압은 5.0×104Pa이다.)
- 0.002
- 0.004
- 0.02
- 0.04
16. 다음 <보기>에서 여과(filtration) 조작에 대한 설명으로 옳은 것을 모두 고르면?
- 가, 나, 다
- 가, 라, 마
- 가, 다, 마
- 다, 라, 마
17. 벤젠 45mol%, 톨루엔 55mol%인 원료를 증류하여 분리하고자 한다. 분리하여 얻고자 하는 벤젠의 농도가 95mol%일 때, 원료가 끓는점(bubble point)에서 공급이 되는 경우에 최소 환류비는? (단, 벤젠 45mol%와 평형에 있는 증기의 벤젠 조성은 70mol%로 가정한다.)
- 0.5
- 1.0
- 1.5
- 2.0
18. 다음 중 습도에 대한 설명으로 가장 옳지 않은 것은?
- 불포화 상태인 습한 공기를 냉각시킬 때, 수증기압이 포화 증기압과 같아지는 온도가 이슬점이다.
- 건조공기 1kg에 포함되어 있는 수증기량(kg)을 절대습도라고 한다.
- 공기 중의 수증기압과 그 온도에서의 포화수증기압의 비를 상대습도라고 한다.
- 건조공기 1mol에 포함되어 있는 수증기몰수(mol)의 백분율을 퍼센트습도라고 한다.
19. 다음 <보기>에서 운동량 전달에 사용되는 무차원 변수에 대한 설명으로 옳은 것을 모두 고르면?
- 가
- 가, 나
- 가, 나, 다
- 가, 나, 다, 라
20. 아래의 표준상태 엔탈피 값을 이용하여 <보기> 반응의 표준상태 엔탈피(kJ/mol)를 구하면?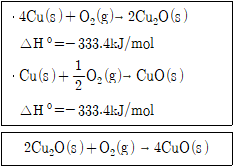
- 143.7kJ/mol
- 287.4kJ/mol
- -143.7kJ/mol
- -287.4kJ/mol







 에서 수은주 높이가 관내 압력보다 낮게 형성되어 있으므로, 관내 압력이 대기압보다 낮은 진공 상태임을 알 수 있습니다.
에서 수은주 높이가 관내 압력보다 낮게 형성되어 있으므로, 관내 압력이 대기압보다 낮은 진공 상태임을 알 수 있습니다.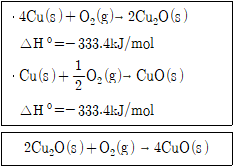
오답 노트
kg⋅m⋅K-1⋅mol-1: 분자가 질량 $\times$ 길이로, 압력 $\times$ 부피(에너지 단위)를 나타내지 못하므로 틀린 단위입니다.